
����Ŀ����֪��I2��2S2O32-=S4O62-��2I��;CuI�Dz�����ˮ�İ�ɫ������
������ʵ��ܶȻ��������±���
���� | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2��10��20 | 2.6��10��39 | 1.7��10��7 | 1.3��10��12 |
��1��ij����CuCl2��Һ�к���������FeCl3��Ϊ�õ�������CuCl2��2H2O���壬����_________������pH��4��ʹ��Һ�е�Fe3��ת��ΪFe(OH)3��������ʱ��Һ�е�c(Fe3��)��_________�����˺�������Һ����������Ũ���ᾧ���ɵ�CuCl2��2H2O���塣
��2���ڿ�����ֱ�Ӽ���CuCl2��2H2O����ò���������ˮCuCl2��ԭ����(����������)��____________________________________________����CuCl2��2H2O����õ�������ˮCuCl2�ĺ���������______________________________��
��3��ijѧϰС��������ӵ��������ⶨ����CuCl2��2H2O���������(��������I��������Ӧ������������)�Ĵ��ȣ��������£�ȡ0.36 g��������ˮ���������KI���壬��ַ�Ӧ�����ɰ�ɫ��������0.100 0 mol��L��1 Na2S2O3����Һ�ζ�������ζ��յ�ʱ������Na2S2O3����Һ20.00 mL��
�ٿ�ѡ��_______________���ζ�ָʾ�����ζ��յ��������________________________��
��CuCl2��Һ��KI��Ӧ�����ӷ���ʽΪ___________________________________________��
�۸�������CuCl2��2H2O�������ٷ���Ϊ__________________
���𰸡�Cu(OH)2��Cu2(OH)2CO3 ��CuO 2.6��10��9 mol��L��1 CuCl2�ڼ��ȹ�����ˮ�ⱻ�ٽ�,����Cu(OH)2,�����ɵ�HCl�ӷ�������ϵ�������ȫˮ�� �ڸ����HCl�����м��� ������Һ ��ɫ��ȥ��ά�ְ���Ӳ����� 2Cu2����4I��===2CuI����I2 95%
��������
��1��������������ڵ���pH����Ҫ��������ת��Ϊ���������������Ҳ������������ʣ��ȸ�����Һ��pH����������Ũ�ȣ��ٽ��ˮ�����ӻ�������������������Ũ�ȣ�������Fe(OH)3��Ksp����������Ũ�ȣ�
��2������ʱ�ٽ��Ȼ�ͭ��ˮ�������ɵ��Ȼ����ӷ����ˮ����ȫ��Ҫ��õ��ϴ�����ˮ�Ȼ�ͭӦ���Ȼ���������������ˮ�⣻
��3�����ݵ⻯�غ��Ȼ�ͭ����������ԭ��Ӧ�����ɵ⻯��ͭ�����͵ⵥ�ʣ��ⵥ�������۱��������ݵⵥ�ʱ�Na2S2O3����Һ��ȫ��ԭ�ﵽ�ζ����յ㣬���ݷ�����Ӧ���ӷ���ʽ���㡣
��1��Ϊ�õ�������CuCl22H2O����Ҫ��ȥ�Ȼ�������������������������ӣ�ʹ������Ũ�ȼ�С������������Ũ�����ٽ��Ȼ���ˮ���������������������Ҳ��������µ����ʣ����Լ������ʺ�Ӧ��ת��Ϊ�Ȼ�ͭ������Ӧ�ü���������ͭ���ʽ̼��ͭ������ͭ����Һ��pH=4��������Һ��������Ũ��Ϊ10-4mol/L��������������Ũ��Ϊ10-10mol/L��c��Fe3+��=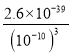 =2.6��10-9mol/L��
=2.6��10-9mol/L��
��2������CuCl2�ڼ��ȹ�����ˮ�ⱻ�ٽ��������ɵ�HCl���ӷ���������ϵ�����ˮ����ȫ�����ɼ�ʽ�Ȼ�ͭ��������ͭ��������CuCl2��2CuCl22H2O![]() Cu2(OH)2CuCl2��2HCl��2H2O����õ���ˮCuCl2�ĺ��������ǣ���CuCl22H2O�����ڸ����HCl�����м�����ˮ��
Cu2(OH)2CuCl2��2HCl��2H2O����õ���ˮCuCl2�ĺ��������ǣ���CuCl22H2O�����ڸ����HCl�����м�����ˮ��
��3������������Ƶζ��ⵥ�ʷ�Ӧ�ķ���ʽ��2Na2S2O3+I2�TNa2S4O6+2NaI�����õⵥ�������۱���ѡ��ָʾ��Ϊ���ۣ��յ�Ϊ��ɫ��ȥһ��ʱ�䲻�ָ���ɫ��
��CuCl2��Һ��KI��Ӧ����CuI��KCl��I2����Ӧ�����ӷ���ʽΪ2Cu2����4I��===2CuI����I2;
������2Na2S2O3+I2�TNa2S4O6+2NaI��2Cu2++4I-=2CuI��+I2��
�õ���ϵʽ 2Na2S2O3��2Cu2+
2 2
0.1000mol/L![]() 0.0200L 0.1000mol/L
0.0200L 0.1000mol/L![]() 0.0200L=0.002mol
0.0200L=0.002mol
������CuCl22H2O�������ٷ���Ϊ![]() =95%��
=95%��


 ������������Ծ�ϵ�д�
������������Ծ�ϵ�д� �������Ӳ�ϵ�д�
�������Ӳ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���л���Ľṹ������������ء�
�ٱ�����_____������ĸ��
a.������ b.ϩ�� c.Ȳ��
�ڼ��𱽺ͼױ����˵��Լ���_______������ĸ��
a.ˮ b.KMnO4������Һ c.NaOH��Һ
��2������쾰���еĻ��Գɷ�֮һ�������ᣨ�ṹʽ��ͼ����
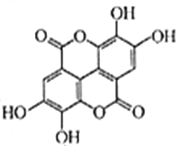
��������ķ���ʽΪ____________
������������к���������Ϊ_______��______�������ƣ�
��1moL������������__________moL Br2����ȡ����Ӧ��1moL�����������뺬______moL NaOH����Һ������Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ���仯�����ڹ�ҵ��������������;��ij�����Ի�ͭ��(��Ҫ�ɷ�Ϊ Cu2S�������� Fe2O3��SiO2 ������)Ϊԭ���Ʊ�������ˮ�ļ�ʽ̼��ͭ���������£�
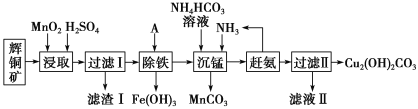
��֪��
�ٳ����¼������ʿ�ʼ�γɳ�������ȫ����ʱ��pH���±�
�������� | Fe2�� | Fe3�� | Cu2�� | Mn2�� |
��ʼ���� | 7.5 | 2.7 | 5.6 | 8.3 |
��ȫ���� | 9.0 | 3.7 | 6.7 | 9.8 |
��Ksp[Fe(OH)3]��4.0��10��38
��1���ӿ조��ȡ�����ʣ�������ͭ������⣬���ɲ�ȡ�Ĵ�ʩ��____����дһ�֣���
��2������I�е���Ҫ�ɷ���MnO2��S��SiO2����д������ȡ����Ӧ������S�Ļ�ѧ����ʽ��____��
��3�������¡�������ʱ������Լ�A����CuO�ȣ�����pH���ķ�ΧΪ____������ A ����Һ�� pH��Ϊ5������Һ�� Fe3����Ũ��Ϊ____mol/L��
��4��д�������̡�(�� Mn2��)�����з�Ӧ�����ӷ���ʽ��____��
��5�����ϰ���ʱ�������˵IJ���������____��
��6����Һ�������ᾧ�õ�������Ҫ��____(д��ѧʽ)��
��7�����ˢ�õ��ij�������ϴ�ӡ�������Եõ���ʽ̼��ͭ���жϳ����Ƿ�ϴ���IJ�����____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ƣ�Na2S2O5����������ԭ����ӡȾýȾ����ʳƷ�������ȡ�һ��ʪ���Ʊ��������ƵĹ���������ͼ��
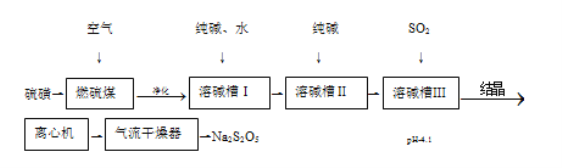
��֪��������NaHSO3��Һ���ᾧ�����ķ��롢�����Ƶ�Na2S2O5��
��1������ȼ��ȳ�Һ̬������ȼ��¯�У�������__��
��2������������Ҫ��ȥ������������__��
��3���ܼ�ۢ�����Ҫͨ������SO2����SO2���㣬������__��
��4���ܼ�ۢ��з�Ӧ�Ļ�ѧ����ʽΪ__��
��5�����Ļ�������ĸҺ��Ҫ���ص��ܼ��__ѭ��ʹ�ã�����������������������������
��6�������������з����Ļ�ѧ����ʽΪ__��
��7��Ϊ�˲ⶨ���ò�Ʒ��Na2S2O5�İٷֺ�����ȡm����Ʒ��ˮ�ܽ⣬��cmol��L-1�ĵ��Һ�ζ����յ����ĵ��ҺVmL���ò�Ʒ��Na2S2O5�İٷֺ���Ϊ__������ĸ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����-�����Ե��ʮ�����ã�������������������õ��IJ���Ե��ˮ�кܺõĴ����ã���˵�ع���ʱ�������������������������Ӧ�á���ѧ�ҽ���غ͵��ˮ��������Ƴ����͵ļ���ʽ��ص�������ɽ����������ת��Ϊ���ܴ��档��֪�������Ե���ܷ�Ӧ����ʽΪ��Fe+2NiOOH+2H2O![]() Fe��OH��2+2Ni��OH��2�������й�˵��������ǣ� ��
Fe��OH��2+2Ni��OH��2�������й�˵��������ǣ� ��
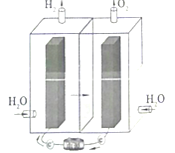
A.���ܡ��������ڶ�����Դ
B.�ô���װ���еĽ���ĤΪ�����ӽ���Ĥ
C.��װ�ô����ܷ����ķ�ӦΪ��2H2O![]() 2H2��+O2��
2H2��+O2��
D.��-�����Ե�طŵ�ʱ�����ķ�ӦΪ��Ni��OH��2+OH--e-�TNiOOH+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼���γɻ�������������Ԫ�أ��䵥�ʼ������������������������Ҫ��Դ���ʡ���ش��������⣺
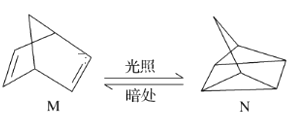
��1���л���M����̫������տ�ת����N��ת���������£���H����88.6 kJ��mol��1����M��N��ȣ����ȶ�����________��
��2����֪CH3OH(l)��ȼ������H����726.5 kJ��mol��1��CH3OH(l)��![]() O2(g)=CO2(g)��2H2(g)����H����a kJ��mol��1��a________726.5(����>����<����������)
O2(g)=CO2(g)��2H2(g)����H����a kJ��mol��1��a________726.5(����>����<����������)
��3����Cl2��H2O(g)ͨ�����ȵ�̿�㣬����HCl��CO2������1 mol Cl2���뷴Ӧʱ�ͷų�145.0 kJ������д���÷�Ӧ���Ȼ�ѧ����ʽ��________________________________________��
��4������͵�������ı������������ʡ���ʯī�����ۺͶ������Ѱ�һ����������ڸ��������գ��������ʿ������²���:4Al(s)��3TiO2(s)��3C(s)===2Al2O3(s)��3TiC(s)����H����1 176.0 kJ��mol��1����Ӧ�����У�ÿת��1 mol���ӷų�������Ϊ_______��
��5�� ��֪����C(s)��O2(g)===CO2(g)�� ��H1����393.5 kJ��mol��1
��2CO(g)��O2(g)===2CO2(g)�� ��H2����566 kJ��mol��1
��TiO2(s)��2Cl2(g)===TiCl4(s)��O2(g) ��H3��+141 kJ��mol��1
��TiO2(s)��2Cl2(g)��2C(s)===TiCl4(s)��2CO(g)�� ��H��__________________��
��6����֪��1 mol H��H����1 mol N��H����1mol N��N���ֱ���Ҫ��������436 kJ��391 kJ��946 kJ����N2(g)��H2(g)��Ӧ����NH3(g)���Ȼ�ѧ����ʽΪ:________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�������Һ�У�c(H+)��С���������˳����________
��0.1mol/L HCl��Һ ��0.1mol/L H2SO4��Һ ��0.1mol/L NaOH��Һ ��0.1mol/L CH3COOH��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б�����ȷ����
A.������������C6H6Cl6�ķ�Ӧ��ȡ����Ӧ
B.��������ˮ���𱽺����Ȼ�̼��Һ
C.�����ʵ����ļ�����������Ӧ���л�����ֻ��CH3Cl
D.1mol![]() ������4molH2�����ӳ�
������4molH2�����ӳ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��W��X��Y��Z��ԭ���������������������ͬ����������Ԫ�أ���ɫ����![]() ��������ɫ��Z������ĸ�Ԫ�ص��⻯���ˮ��Һ�������ԣ�����˵����ȷ���ǣ� ��
��������ɫ��Z������ĸ�Ԫ�ص��⻯���ˮ��Һ�������ԣ�����˵����ȷ���ǣ� ��
A.Z���ʵķе�ͣ���Z������Һ��
B.ԭ�Ӱ뾶��![]()
C.����������Ӧˮ��������ԣ�![]()
D.X��Y��Z��W�����γɼ��м��Լ����зǼ��Լ��Ļ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com