
| A. | ①③⑤ | B. | ②③④ | C. | ①③④⑤ | D. | ①②③④⑤ |
分析 可能反应X(g)+Y(g)?3Z(g)达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,据此进行判断.
解答 解:①单位时间内,A、B生成C的分子数与分解C的分子数相等,表明正逆反应速率相等,该反应达到平衡状态,故①正确;
②该反应为吸热反应,若体系的温度不再变化,表明正逆反应速率相等,该反应已经达到平衡状态,故②正确;
③外界条件不变时,A、B的浓度不随时间而变化,表明此时正逆反应速率相等,已经达到平衡状态,故③正确;
④该反应为气体体积增大的反应,当体系的压强不再变化时,表明各组分的浓度不再变化,该反应已经达到平衡状态,故④正确;
⑤该反应为气体分子数增大的反应,当体系的分子总数不再变化,表明正逆反应速率相等,已经达到平衡状态,故⑤正确;
故选D.
点评 本题考查了化学平衡状态的判断,题目难度不大,明确化学平衡状态的特征为解答关键,注意掌握化学平衡的概念及实质,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

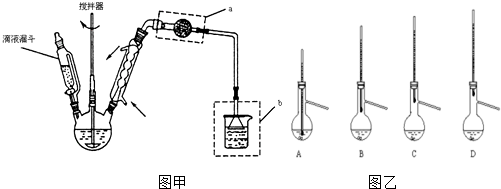
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol•L-1 | B. | 1.6mol•L-1 | C. | 0.8mol•L-1 | D. | 0.4mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com