
NH3经一系列反应可以得到HNO3和NH4NO3,如下图所示。

(1)Ⅰ中,NH3和O2在催化剂作用下反应,其化学方程式是_________________________。
(2)Ⅱ中,2NO(g)+O2(g)  2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。

①比较p1、p2的大小关系:________。
②随温度升高,该反应平衡常数变化的趋势是________。
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
①已知:2NO2(g)  N2O4(g) ΔH1 2NO2(g)
N2O4(g) ΔH1 2NO2(g) N2O4(l) ΔH2
N2O4(l) ΔH2
下列能量变化示意图中,正确的是(选填字母)________。

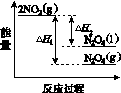

A B C
②N2O4与O2、H2O化合的化学方程式是________________________________________。
(4)Ⅳ中,电解NO制备NH4NO3,其工作原理如图所示。为使电解产物全部转化为NH4NO3,需补充A。A是________,说明理由:________________________________________。

(1)4NH3+5O2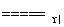 4NO+6H2O
4NO+6H2O
(2)①p1<p2 ②减小
(3)①A ②2N2O4+O2+2H2O===4HNO3
(4)NH3 根据反应:8NO+7H2O 3NH4NO3+2HNO3,电解产生的HNO3多
3NH4NO3+2HNO3,电解产生的HNO3多
[解析] (1)氨的催化氧化的反应方程式为
4NH3+5O2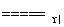 4NO+6H2O。
4NO+6H2O。
(2)①由2NO(g)+O2(g)  2NO2(g)可知该反应为气体体积减小的反应,温度相同,增大压强,平衡正向移动,NO的平衡转化率增大,根据图示和坐标含义,判断p1<p2;②再看同一压强线,温度升高,NO的平衡转化率降低,平衡向逆反应方向移动,则正反应为放热反应,温度升高,平衡常数减小。
2NO2(g)可知该反应为气体体积减小的反应,温度相同,增大压强,平衡正向移动,NO的平衡转化率增大,根据图示和坐标含义,判断p1<p2;②再看同一压强线,温度升高,NO的平衡转化率降低,平衡向逆反应方向移动,则正反应为放热反应,温度升高,平衡常数减小。
(3)①降低温度,NO2(g)转变为N2O4(l),则ΔH2<0,反应物能量高于生成物能量,C错误; N2O4(g)转变为N2O4(l)需要放出热量,所以NO2(g)转变为N2O4(g)比NO2(g)转变为N2O4(l)放出的热量少,B错误,所以正确的图示为A;②N2O4、O2和H2O反应生成硝酸的反应方程式为2N2O4+ O2+2H2O===4HNO3。
(4)根据工作原理装置图,可以确定阳极为NO失去电子转变为NO ,阴极NO转变为NH
,阴极NO转变为NH ,根据电极反应书写电极反应式为:
,根据电极反应书写电极反应式为:
阳极:NO-3e-+2H2O===NO +4H+
+4H+
阴极:NO+5e-+ 6H+===NH + H2O
+ H2O
然后根据得失电子守恒,硝酸根离子物质的量比铵根离子物质的量多,所以需要向溶液中加入的物质为NH3(即8NO+7H2O 3NH4NO3+2HNO3)。
3NH4NO3+2HNO3)。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.锥形瓶可用作加热的反应器
B.室温下,不能将浓硫酸盛放在铁桶中
C.配制溶液定容时,俯视容量瓶刻度会使溶液浓度偏高
D.用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制备下列气体时,所用方法正确的是( )
A.制氧气时,用Na2O2或H2O2作反应物可选择相同的气体发生装置
B.制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体
C.制乙烯时,用排水法或向上排空气法收集气体
D.制二氧化氮时,用水或NaOH溶液吸收尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质应用的说法错误的是( )
A.玻璃容器可长期盛放各种酸
B.纯碱可用于清洗油污
C.浓氨水可检验氯气管道漏气
D.Na2S可除去污水中的Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系: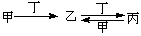 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是
A.若甲为焦炭,则丁可能是O2
B.若甲为SO2,则丁可能是氨水
C.若甲为Fe,则丁可能是盐酸
D.若甲为NaOH溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应广泛应用于金属的冶炼。下列说法不正确的是( )
A、电解熔融氯化钠制取金属钠的反应中,钠离子被还原,氯离子被氧化
B、湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应
C、用磁铁矿炼铁的反应中, 被
被 还原成
还原成 ,转移
,转移
D、铝热法还原铁的反应中,放出的热量能使铁熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如图所示。请回答下列问题。

(1)碘是________(填颜色)固体物质,实验室常用________方法来分离提纯含有少量杂质的固体碘。
(2)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:
3I2+6KOH 5KI+KIO3+3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
5KI+KIO3+3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为________;阴极上观察到的实验现象是________。
(3)电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验电解液中是否有I-的实验方案,并按要求填写下表。
要求:所需药品只能从下列试剂中选择,实验仪器及相关用品自选。
试剂:淀粉溶液、碘化钾淀粉试纸、过氧化氢溶液、稀硫酸。
| 实验方法 | 实验现象及结论 |
(4)电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
 →
→ →
→ →
→ →
→ →
→ →
→
步骤②的操作名称是________,步骤⑤的操作名称是________。步骤④洗涤晶体的目的是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com