
����Ŀ������[KAl��SO4��2]��һ���Σ�����ֽ�ȷ���Ӧ�ù㷺��ij��ȤС�����10.0g�������ޣ���90%��Al��������������Fe��Mg����־���Ʊ�������ʵ�鷽����ͼ1�� 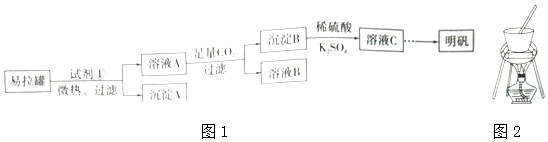
��1���Լ���Ӧѡ��������ţ��� a������b��H2SO4��Һc����ˮd��NaOH��Һ
��2���������ܽ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ ��
��3����ҺB�����ʵ���Ҫ�ɷ�Ϊ���ѧʽ����
��4������ҺC�еõ�������ʵ���������Ϊ����Ũ��������������ƣ������ˡ�ϴ�ӡ������ͼ2��ʾ�����������е�һ�������� ��
��5����С����ʵ�����֮�õ�118.5g�������������Ļ�����Ϊ �� ����֪��������Ħ������Ϊ474gmol��1��
���𰸡�
��1��d
��2��2Al+2NaOH+2H2O�T2NaAlO2+3H2��
��3��NaHCO3
��4����ȴ�ᾧ����������ʹ������
��5��75%
���������⣺��1�����������ܽ���ǿ���ǿ������Һ��������þֻ���ܽ���ǿ������Һ�е����ʲ��죬��ѡ��NaOH��Һ�ܽ������ޣ��ɳ�ȥ���е�����þ�����ʣ�
���Դ��ǣ�d����2����������������Һ��Ӧ����ƫ�����ƺ�������������Ӧ�Ļ�ѧ����ʽΪ2Al+2NaOH+2H2O�T2NaAlO2+3H2����
���Դ��ǣ�2Al+2NaOH+2H2O�T2NaAlO2+3H2������3�����ݷ�����֪��ƫ��������Һ��ͨ��CO2��Һ��������������������̼�����ƣ�ͨ�����˵õ�̼��������Һ����B������������������B������ҺBΪNaHCO3��Һ��
���Դ��ǣ�NaHCO3����4����������Һ������K2SO4��Һ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����õ�������������������ʹ��������
���Դ��ǣ���ȴ�ᾧ����������ʹ����������2��������Ԫ���غ㣬Al��KAl��SO4��212H2O�������Ͽɵõ�����������Ϊ�� ![]() =158g���������Ļ�����Ϊ
=158g���������Ļ�����Ϊ ![]() =75%��
=75%��
���Դ��ǣ�75%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����ϡ���Ϣ����Դ��ϵ���С�����˵������ȷ����
A. ˮ�ࡢ�������մɶ��Ǵ�ͳ�Ĺ����ι�ҵ��Ʒ
B. ��ǰ̫���ܵ�ص���Ҫ�����Ƕ�������
C. ��ǰ�����ʹ�õĹ�оƬ��Ҫ�����ǹ�
D. �������ά����Ҫ�����Ƕ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ƣ���һ�������������м��ȣ��ڶ������������������£��г�ַ�Ӧ��������˵����ȷ���ǣ� ��
A.��һ����ʧȥ���Ӷ�
B.������ʧȥ����һ����
C.�ڶ����Ƶķ�Ӧ�����������
D.�����Ƶķ�Ӧ��������һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ҫ��NaCl��BaCl2�Ļ��Һ�зֱ�õ�������NaCl��BaCl2���壬��һϵ�еIJ����У�Ӧѡ�õ��Լ���( )
A. ̼��ء����� B. ̼���ơ����� C. ̼���ơ����� D. �������ơ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��X����ѧ��ѧ�еij������ʣ�������ͼ��ʾת����ϵ������������ͷ�Ӧ������ȥ���� 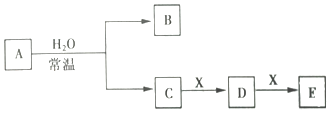
��1����AΪ����ɫ��ĩ����0.1molA��ˮ��Ӧʱת�Ƶĵ�����ĿΪ ��
��2����AΪ�����Ľ������ʣ���ɫ��Ӧ�ʻ�ɫ��X��һ���������ЧӦ�����壬������Ũ�ȵ�D��E������Һ���Լ�Ϊ ��
��3����B����Ư���ԣ���A��H2O��Ӧ�����ӷ���ʽ�� ��
��4����AΪ����ɫ���壬��E��Һ�еμ�������ˮ�����ɵİ�ɫ����Ѹ�ٱ����ɫ�����ձ�ɺ��ɫ�� ��X�Ļ�ѧʽΪ ��
��A��H2O��Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤������������˵����ȷ���ǣ�������
A.5.6 g�������ᷴӦʱʧȥ�ĵ�����ĿΪ0.3 NA
B.71 g��������ԭ����ĿΪNA
C.��״���£�������Ȼ�ϵĵ���������11.2 L�������ķ�����Ϊ0.5 NA
D.��25�棬1.01��105Paʱ��22.4 L����������ԭ����ĿΪ2 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȼ��������Ҫ�ɷ��Ǽ�����ˮ���ӵĽᾧˮ���CH4��nH2O�����侧�������ǣ� ��
A.���Ӿ���
B.���Ӿ���
C.ԭ�Ӿ���
D.��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͬ���������ȵ����壬���������ڵȵ�������ǣ� ��
A.12CO2��14CO
B.H2O2��D2O
C.N2��13CO
D.NO��CO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У���ʹ����ĺ�ɫʯ����ֽ����ɫ����
A. Һ��B. ����C. ��ˮD. �Ȼ����Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com