
【题目】A、B、C、D均为短周期元素,它们在元素周期表中的相对位置如图所示,其中B的单质在空气中含量约占80%。
A | B | C | |||
D |
(1)写出下列元素的名称:C____,D___。
(2)画出B的原子结构示意图____。C在元素周期表中的位置是____。
(3)B、C两种元素最简单氢化物的稳定性由强到弱的顺序是_____。写出A的最简单氢化物的电子式:______。
【答案】氟 镁 ![]() 第二周期ⅦA族 HF>NH3
第二周期ⅦA族 HF>NH3 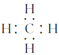
【解析】
由B的单质在空气中含量约占80%可知B为N元素;由周期表的相对位置可知,A为C元素、C为F元素、D为Mg元素。
(1)由以上分析可知,C为F元素,名称为氟,D为Mg元素,名称为镁,故答案为:氟;镁;
(2)B为N元素,原子核外有7个电子,2个电子层,原子结构示意图为![]() ;C为F元素,位于周期表第二周期ⅦA族,故答案为:
;C为F元素,位于周期表第二周期ⅦA族,故答案为:![]() ;第二周期ⅦA族;
;第二周期ⅦA族;
(3)元素非金属性越强,氢化物的稳定性越强,氟元素的非金属性比氧元素强,则最简单氢化物的稳定性由强到弱的顺序是HF>NH3;A为C元素,最简单氢化物的分子式为CH4,电子式为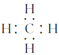 ,故答案为:HF>NH3;
,故答案为:HF>NH3;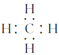 。
。


科目:高中化学 来源: 题型:
【题目】银的冶炼有很多方法,在《天工开物》均有记载,而现代流行的“氰化法”,即 用NaCN溶液浸出矿石中的银的方法是常用的方法。该方法具备诸多优点:银的回收率高、对游离态和化合态的银均能浸出、对能源消耗相对较少,生产工艺简便等,但银化物通常有毒。其炼制工艺简介如下:

(1)矿石需要先进行破碎、研磨,其目的是_________。
(2)写出该工艺的一个明显的缺点____________。
(3)用NaCN浸泡矿石(该矿石是辉银矿,其主要成分是Ag2S)时,反应容器处于开口状态,产生的银以[Ag(CN)2]-形式存在,硫元素被氧化至最高价,试写出主要反应的离子方程式________。
(4)银往往和锌、铜、金等矿伴生,故氰化法得到的银中往往因含有上述金属而不纯净,需要进一步纯化,从而获得纯净的银。其中方法之一就是进行电解精炼,在精炼过程中,含有杂质的银作_______极(填“阴”或“阳”),该电极上发生的主要反应式为_____。
(5)有人提出了另外的提纯银的方案,先将锌粉还原后的混合金属用略过量的硝酸溶解,通 过精确调整溶液的pH来进行金属元素逐一分离,已知:
①溶解后的离子浓度如表:
Zn2+ | Cu2+ | Ag+ | |
物质的量浓度(mol/L) | 0.001 | 0.002 | 0.5 |
②某些金属离子的氢氧化物Ksp如表:
Zn2+ | Cu2+ | Ag+ | …… | |
Ksp | 1.0×10-17 | 2.0×10-20 | 2.0×10-8 |
(已知lg2=0.3),该设计方案 ______(填“可行”或“不可行”),其原因是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四种粒子的结构示意图中,说法正确的是
①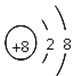 ②
②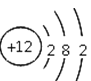 ③
③ ④
④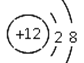
A. 它们表示四种不同的元素B. ①④表示的是阳离子
C. ①③④表示的元素都是非金属元素D. ②表示的元素在化合物中通常显+2价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)烧杯间填满碎泡沫塑料的作用是___________________________
(2)环形玻璃搅拌棒能否用环形铁质搅拌棒代替?_______(填“能”或“不能”), 其原因是____________________________。
(3)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是___________________________。
实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应, 与上述实验相比,所放出的热量________________(填“相等”“不相等”),若实验操作均正确,则所求中和热_________(填“相等”“不相等”)。
(4)已知在稀溶液中,强酸和强碱发生中和反应生成1 mol H2O时,放出57.3 kJ的热量,则上述反应的热化学方程式为:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国C.Marchetin博士对世界一次能源替代趋势作了如图所示预测。回答下列问题:
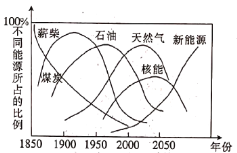
(1)图中属于化石能源的有煤、石油和_____。
(2)目前采用铀核裂变方式获取核能,![]() 中含有的中子数为____;
中含有的中子数为____;![]() 与
与![]() 的关系是_____。
的关系是_____。
(3)太阳能是一种新能源,制造太阳能电池的材料有Si、Ga、As等。它们能用于制造太阳能电池是利用其____性质;Ga与As均是第四周期的主族元素,Ga与Al同主族,As与N同主族,则元素As、Ga的最高价氧化物对应水化物酸性较强的是____(填化学式)。
(4)近年来我国在南海成功试开采可燃冰,可燃冰释放的气体主要有CH4、少量乙烷、丙烷及丁烷等。丙烷完全燃烧的化学方程式为____;异丁烷的一氯取代物有___种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 乙烷和乙烯都能用来制取氯乙烷,且反应类型相同
B. 无水乙醇比医用酒精的消毒效果更好
C. 除去甲烷的乙烯可通过酸性高锰酸钾溶液洗气
D. 甲苯和乙苯都是苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是批量生产的笔记本电脑所用的甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应。电池总反应式为2CH3OH+3O2===2CO2+4H2O。下列说法中不正确的是
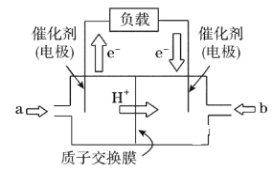
A. 左边的电极为电池的负极,a处通入的是甲醇
B. 每消耗3.2 g氧气转移的电子为0.4 mol
C. 电池负极的反应式为CH3OH+H2O6e===CO2+6H+
D. 电池的正极反应式为O2+2H2O+4e===4OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以石油和淀粉或纤维素为原料均可制得乙酸乙酯,转化关系如下图:

其中气体B在标况下的密度为:1.25 g/L。请回答:
(1)B中官能团的名称是________。
(2)A的分子式是________。
(3)反应④的化学方程式为________。
(4)下列说法正确的是________。
A.反应②⑤⑥属于取代反应
B.物质F的结构简式为CH3CH2OOCCH3
C.B和E可在一定条件下直接合成F,该方法符合绿色化学理念
D.可用新制氢氧化铜鉴别C、D、E三种物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请填写下表:
物质 | 摩尔质量 | 物质的量 | 质量 | 分子或离子数目 |
SO2 | ________ | 2 mol | ________ | ________ |
SO42- | ________ | ________ | ________ | 6.02×1022 |
O2 | ________ | ________ | 8.0 g | ________ |
(2)O2和O3是氧元素的两种单质。根据分子式回答。等质量的O2和O3所含分子数之比为____,原子个数比为____。
(3)摩尔质量是指单位物质的量的物质所含有的质量。
①已知NH3的相对分子质量为17,则NH3的摩尔质量为____。
②1.28 g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com