

| A£® | µća“¦µÄÕż·“Ó¦ĖŁĀŹ±Čµćb“¦µÄ“ó | |
| B£® | µćc“¦µÄÕż·“Ó¦ĖŁĀŹÓėÄę·“Ó¦ĖŁĀŹĻąµČ | |
| C£® | µćd£Øt1Ź±æĢ£©µÄn£ØN2£©±Čµće£Øt2Ź±æĢ£©“¦µÄn£ØN2£©“ó | |
| D£® | ĘäĖūĢõ¼ž²»±ä£¬773KĻĀ·“Ó¦ÖĮt1Ź±æĢ£¬“ĖŹ±»³öµÄĮ½øłĘ½ŠŠĻß¼äµÄ¾ąĄė½«ŅŖ±äŠ” |
·ÖĪö A£®ĪļÖŹµÄÅضČŌ½“óĘä·“Ó¦ĖŁĀŹŌ½“ó£»
B£®cµćŗó°±ĘųĪļÖŹµÄĮæŌö“óµ½²»±ä£¬ĒāĘųĪļÖŹµÄĮæ¼õŠ”µ½²»±ä£¬¹Źcµć·“Ó¦ĻņÕż·“Ó¦½ųŠŠ£»
C£®d”¢e“¦ÓŚĶ¬Ņ»Ę½ŗāדĢ¬£»
D£®øĆ·“Ó¦µÄÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶Č£¬Ę½ŗāÄęĻņŅĘ¶Æ£¬·“Ó¦Īļ×Ŗ»ÆĀŹ½µµĶ£¬Ę½ŗāŹ±°±ĘųĪļÖŹµÄĮæ¼õŠ””¢·“Ó¦ĪļĪļÖŹµÄĮæŌö“ó£®
½ā“š ½ā£ŗA£®aµćĒāĘųĪļÖŹµÄĮæ“óÓŚbµć£¬ĖłŅŌµćaĒāĘųÅضČøü“ó£¬ŌņaµćÕż·“Ó¦ĖŁĀŹ±ČµćbµÄ“󣬹ŹAÕżČ·£»
B£®cµćŗó°±ĘųĪļÖŹµÄĮæŌö“óµ½²»±ä£¬ĒāĘųĪļÖŹµÄĮæ¼õŠ”µ½²»±ä£¬¹Źcµć·“Ó¦ĻņÕż·“Ó¦½ųŠŠ£¬Õż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ£¬¹ŹB“ķĪó£»
C£®d”¢e“¦ÓŚĶ¬Ņ»Ę½ŗāדĢ¬£¬Ōņµćd £Øt1Ź±æĢ£©ŗĶµće £Øt2Ź±æĢ£©“¦n £ØN2£©Ņ»Ńł£¬¹ŹC“ķĪó£»
D£®øĆ·“Ó¦µÄÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶Č£¬Ę½ŗāÄęĻņŅĘ¶Æ£¬·“Ó¦Īļ×Ŗ»ÆĀŹ½µµĶ£¬Ę½ŗāŹ±°±ĘųĪļÖŹµÄĮæ¼õŠ””¢·“Ó¦ĪļĪļÖŹµÄĮæŌö“󣬓ĖŹ±»³öµÄĮ½øłĘ½ŠŠĻß¼äµÄ¾ąĄė½«ŅŖ±äŠ”£¬¹ŹDÕżČ·£¬
¹ŹŃ”£ŗBC£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāĶ¼ĻóĪŹĢā£¬ĢāÄæÄѶČÖŠµČ£¬×¢Ņā·ÖĪöĶ¼ĻóÖŠø÷ĪļĄķĮæµÄ±ä»ÆĒśĻߣ¬°ŃĪÕĘ½ŗāדĢ¬µÄĢŲÕ÷ĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£®


 ³õ֊ѧŅµæ¼ŹŌµ¼ÓėĮ·ĻµĮŠ“š°ø
³õ֊ѧŅµæ¼ŹŌµ¼ÓėĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÕżĻņŅĘ¶Æ | B£® | ÄęĻņŅĘ¶Æ | C£® | “ļµ½Ę½ŗā | D£® | ²»Ņ»¶Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā


²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

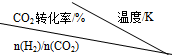 | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | c2=2c1 | B£® | c2£¼2c1 | C£® | c2£¾2c1 | D£® | c1=2c2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚH2O2·Ö½ā¹ż³ĢÖŠ£¬Fe2+ŹĒ·“Ó¦µÄ“߻ƼĮ | |
| B£® | ŌŚH2O2Éś²ś¹ż³ĢÖŠ£¬ŅŖŃĻøń±ÜĆā»ģČė Fe2+ | |
| C£® | H2O2µÄŃõ»ÆŠŌ±ČFe3+Ē棬»¹ŌŠŌ±ČFe2+Ēæ | |
| D£® | ŌŚH2O2·Ö½ā¹ż³ĢÖŠ£¬ČÜŅŗµÄpHÖš½„ĻĀ½µ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś | B£® | ¢Ś¢Ü | C£® | ¢Ł¢Ū | D£® | ¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com