
ΓΨΧβΡΩΓΩΡ≥–ΓΉι”Ο Β―ι1―ι÷ΛFeCl3”κCuΒΡΖ¥”ΠΘ§Ιέ≤λΒΫ”–ΑΉ…Ϊ≥ΝΒμ≤ζ…ζΘ§ΨωΕ®Ε‘ΤδΫχ––…ν»κΧΫΨΩΓΘ
Β―ι1ΘΚ
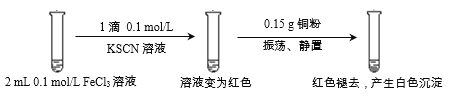
Ή ΝœΘΚ
i. CuSCNΓΔCuClΨυΈΣΡ―»ή”ΎΥ°ΒΡΑΉ…ΪΙΧΧεΘΜΨυΡή”κœθΥαΖ¥”ΠΘ§Ζ÷±π…ζ≥…Cu2+”κSO42-ΓΔCu2+”κCl-ΓΘ
ii. SCN-±Μ≥ΤΈΣΡ⬱պάκΉ”Θ§–‘÷ ”ꬱպάκΉ”œύΥΤΘΜ(SCN)2–‘÷ ”ꬱպΒΞ÷ œύΥΤΘ§ΤδΥ°»ή“Κ≥ ΜΤ…ΪΓΘ
Θ®1Θ©FeCl3»ή“Κ”κKSCN»ή“ΚΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ__________________ΓΘ
Θ®2Θ©œ¬Ν–”… Β―ι1ΒΟΒΫΒΡΆΤ¬έ÷–Θ§ΚœάμΒΡ «_______________Θ®ΧνΉ÷ΡΗ–ρΚ≈Θ©ΓΘ
a. CuΡήΜΙ‘≠Fe3+
b. Fe3+”κSCN-ΒΡΖ¥”Π «Ω…ΡφΖ¥”Π
c. ΑΉ…Ϊ≥ΝΒμ÷–ΒΡCu(I)Θ®I±μ Ψ+1ΦέΆ≠‘ΣΥΊΘ©Ω…Ρή «”…Fe3+―θΜ·CuΒΟΒΫΒΡ
Θ®3Θ©ΈΣΧΫΨΩ Β―ι1÷–ΑΉ…Ϊ≥ΝΒμΒΡ≥…Ζ÷Θ§–ΓΉιΆ§―ß Β ©ΝΥ Β―ι2ΘΚ
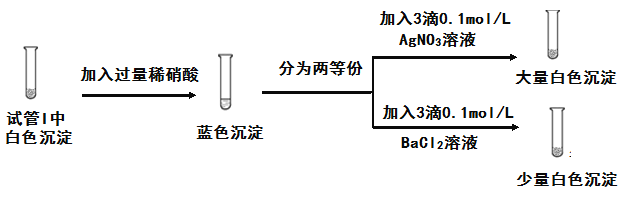
”… Β―ι2Ω…÷ΣΘ§ Β―ι1÷–ΑΉ…Ϊ≥ΝΒμΒΡ≥…Ζ÷ «____ΓΘ
Θ®4Θ©ΗΟ–ΓΉι”ϊΫχ“Μ≤ΫΧΫΨΩ Β―ι1÷–ΑΉ…Ϊ≥ΝΒμ≤ζ…ζΒΡ‘≠“ρΘ§ Β ©ΝΥ Β―ι3ΘΚ
≤Ϋ÷η | Β―ι≤ΌΉς | Β―ιœ÷œσ |
I | »ή“Κ±δΈΣάΕ…ΪΘ§≥Έ«εΆΗΟςΘ§ΒΉ≤Ω÷Μ”–…ΌΝΩΚλ…ΪΙΧΧε Θ”ύ | |
II | »ΓI÷–…œ≤ψ«ε“Κ”Ύ ‘Ιή÷–Θ§ΒΈΦ”1ΒΈ 0.1mol/L KSCN»ή“Κ | ΝΔΩΧ≥ωœ÷Κλ…ΪΘ§Ά§ ±”–ΑΉ…Ϊ≥ΝΒμ…ζ≥… |
III | ’ώΒ¥II÷– ‘ΙήΘ§Ψ≤÷Ο | ΑΉ…Ϊ≥ΝΒμ±δΕύΘ§Κλ…Ϊ÷πΫΞΆ »Ξ |
ΔΌ≤Ϋ÷ηIΒΡ Β―ι≤ΌΉς «_____________________ΓΘ
ΔΎΗυΨί Β―ι3ΒΡœ÷œσΘ§–ΓΉιΆ§―ß»œΈΣFe3+”κCuΖ¥”ΠΒΡ―θΜ·≤ζΈο≤ΜΚ§Cu(I)Θ§ΥϊΟ«ΒΡ≈–Εœ“άΨί «______ΓΘ
Δέ≤Ϋ÷ηII÷–Φ”»κKSCN»ή“ΚΚσ≥ωœ÷Κλ…ΪΒΡΩ…Ρή‘≠“ρ «________________ΓΘ
ΔήΫβ Ά≤Ϋ÷ηIII÷– Β―ιœ÷œσ≤ζ…ζΒΡΩ…Ρή‘≠“ρΘΚ_______________________ΓΘ
ΓΨ¥πΑΗΓΩFe3+ + 3SCN-![]() Fe(SCN)3 abc CuClΚΆCuSCN œρ2 mL 0.1 mol/L FeCl3»ή“Κ÷–Φ”»κ0.15 gΆ≠ΖέΘ§’ώΒ¥ΓΔΨ≤÷Ο »τ”–Cu(I)…ζ≥…Θ§≤Ϋ÷ηI÷–”Π≤ζ…ζCuClΑΉ…Ϊ≥ΝΒμΘ§ΒΪ≤Ϋ÷ηI÷–ΈόΑΉ…Ϊ≥ΝΒμ≤ζ…ζ Cu2+”κSCN-Ζ¥”Π…ζ≥…(SCN)2Θ§Fe2+±Μ(SCN)2―θΜ·ΈΣFe3+ Cu2+”κSCN-ΖΔ…ζΖ¥”ΠΘΚ2Cu2+ + 4SCN-= 2CuSCNΓΐ+ (SCN)2Θ§CuSCN”κCl-ΖΔ…ζ≥ΝΒμΉΣΜ·Ζ¥”ΠΘΚCuSCN + Cl-=CuCl + SCN-Θ§SCN-ΦΧ–χ”κCu2+Ζ¥”ΠΘ§ΒΦ÷¬ΑΉ…Ϊ≥ΝΒμ±δΕύΘΜΥφΉ≈Ζ¥”ΠΒΡΫχ––SCN-÷πΫΞ±ΜœϊΚΡΘ§ΤΫΚβFe3+ + 3SCN-
Fe(SCN)3 abc CuClΚΆCuSCN œρ2 mL 0.1 mol/L FeCl3»ή“Κ÷–Φ”»κ0.15 gΆ≠ΖέΘ§’ώΒ¥ΓΔΨ≤÷Ο »τ”–Cu(I)…ζ≥…Θ§≤Ϋ÷ηI÷–”Π≤ζ…ζCuClΑΉ…Ϊ≥ΝΒμΘ§ΒΪ≤Ϋ÷ηI÷–ΈόΑΉ…Ϊ≥ΝΒμ≤ζ…ζ Cu2+”κSCN-Ζ¥”Π…ζ≥…(SCN)2Θ§Fe2+±Μ(SCN)2―θΜ·ΈΣFe3+ Cu2+”κSCN-ΖΔ…ζΖ¥”ΠΘΚ2Cu2+ + 4SCN-= 2CuSCNΓΐ+ (SCN)2Θ§CuSCN”κCl-ΖΔ…ζ≥ΝΒμΉΣΜ·Ζ¥”ΠΘΚCuSCN + Cl-=CuCl + SCN-Θ§SCN-ΦΧ–χ”κCu2+Ζ¥”ΠΘ§ΒΦ÷¬ΑΉ…Ϊ≥ΝΒμ±δΕύΘΜΥφΉ≈Ζ¥”ΠΒΡΫχ––SCN-÷πΫΞ±ΜœϊΚΡΘ§ΤΫΚβFe3+ + 3SCN- ![]() Fe(SCN)3Ρφœρ“ΤΕ·Θ§ΒΦ÷¬Κλ…Ϊ÷πΫΞΆ »Ξ
Fe(SCN)3Ρφœρ“ΤΕ·Θ§ΒΦ÷¬Κλ…Ϊ÷πΫΞΆ »Ξ
ΓΨΫβΈωΓΩ
Θ®1Θ©FeCl3»ή“Κ”κKSCN»ή“ΚΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣFe3+ + 3SCN- ![]() Fe(SCN)3Θ§
Fe(SCN)3Θ§
¥πΑΗΈΣΘΚFe3+ + 3SCN- ![]() Fe(SCN)3ΘΜ
Fe(SCN)3ΘΜ
Θ®2Θ©a. Φ”»κCuΘ§»ή“ΚΚλ…ΪΆΥ»ΞΘ§≤ζ…ζΑΉ…ΪΙΧΧεΘ§ΫαΚœ“―÷Σ–≈œΔΘ§CuSCNΓΔCuClΨυΈΣΡ―»ή”ΎΥ°ΒΡΑΉ…ΪΙΧΧεΘ§ΥΒΟς»ή“Κ÷–»ΐΦέΧζάκΉ”œϊ ßΘ§Ά≠ΒΞ÷ ΉΣ±δΈΣ―«Ά≠άκΉ”Θ§Ω…÷ΛΟςΆ≠ΚΆ»ή“Κ÷–ΒΡFe3+ΖΔ…ζ―θΜ·ΜΙ‘≠Ζ¥”ΠΘ§»ΐΦέΧζάκΉ”Μ·ΚœΦέΫΒΒΆΘ§±ΜΜΙ‘≠Θ§Ι a’ΐ»ΖΘΜ
b. Ά≠ΚΆ»ή“Κ÷–ΒΡFe3+ΖΔ…ζΖ¥”Π ±Θ§»ή“Κ÷–Fe3+≈®Ε»Φθ–ΓΘ§ ΙΖ¥”ΠFe3+ + 3SCN- ![]() Fe(SCN)3 Ρφœρ“ΤΕ·Θ§Fe(SCN)3 ÷πΫΞΦθ…ΌΘ§»ή“ΚΆ …ΪΘ§‘ρΩ…“‘ΥΒΟςFe3+”κSCN-ΒΡΖ¥”Π «Ω…ΡφΖ¥”ΠΘ§Ι b’ΐ»ΖΘΜ
Fe(SCN)3 Ρφœρ“ΤΕ·Θ§Fe(SCN)3 ÷πΫΞΦθ…ΌΘ§»ή“ΚΆ …ΪΘ§‘ρΩ…“‘ΥΒΟςFe3+”κSCN-ΒΡΖ¥”Π «Ω…ΡφΖ¥”ΠΘ§Ι b’ΐ»ΖΘΜ
c. Ά≠‘ΣΥΊ”…0Φέ±δΈΣ+1ΦέΘ§Μ·ΚœΦέ…ΐΗΏ±Μ―θΜ·Θ§»ή“Κ÷–Κ§”–Cl-ΓΔSCN-ΓΔFe3+ΚΆK+Θ§Cl-ΈΣ-1Φέ «¬»‘ΣΥΊΒΡΉνΒΆΦέΘ§÷ΜΨΏ”–ΜΙ‘≠–‘Θ§SCN-±Μ≥ΤΈΣΡ⬱պάκΉ”Θ§–‘÷ ”ꬱպάκΉ”œύΥΤΘ§‘ρSCN-ΨΏ”–ΜΙ‘≠–‘Θ§≤ΜΡή ΙΆ≠ΒΞ÷ ±Μ―θΜ·ΘΜΒΞ÷ ΒΡΜΙ‘≠–‘‘Ϋ«ΩΘ§ΤδάκΉ”ΒΡ―θΜ·–‘‘Ϋ»θΘ§KΒΡΜΙ‘≠–‘«Ω”ΎFeΘ§‘ρFe3+ΒΡ―θΜ·–‘«Ω”ΎK+Θ§‘ρΆ≠ΒΞ÷ ”κFe3+ΖΔ…ζ―θΜ·ΜΙ‘≠Ζ¥”ΠΘ§Ι c’ΐ»ΖΘΜ
Θ®3Θ©ΗυΨί“―÷Σ–≈œΔΘ§CuSCNΓΔCuClΨυΈΣΡ―»ή”ΎΥ°ΒΡΑΉ…ΪΙΧΧεΘΜΨυΡή”κœθΥαΖ¥”ΠΘ§œθΥαΨΏ”–―θΜ·–‘Θ§ΫΪ―«Ά≠άκΉ”ΚΆSCN-―θΜ·Θ§Ζ÷±π…ζ≥…Cu2+”κSO42-ΓΔCu2+”κCl-Θ§ΗυΨίΆΦ÷–Ζ¥”ΠΘ§œρΦ”»κœθΥαΚσΒΡ»ή“Κ÷–Φ”»κœθΥα“χΘ§≤ζ…ζΑΉ…Ϊ≥ΝΒμΘ§ΥΒΟς»ή“Κ÷–Κ§”–Cl-ΘΜœρΦ”»κœθΥαΚσΒΡ»ή“Κ÷–Φ”»κ¬»Μ·±ΒΘ§≤ζ…ζΑΉ…Ϊ≥ΝΒμΘ§ΥΒΟς»ή“Κ÷–Κ§”–SO42-Θ§Ι ΗυΨί“‘…œΖ÷ΈωΩ…÷ΣΘ§ Β―ι1÷–ΑΉ…Ϊ≥ΝΒμΒΡ≥…Ζ÷ «CuSCNΓΔCuClΘ§
¥πΑΗΈΣΘΚCuSCNΓΔCuClΘΜ
Θ®4Θ©ΔΌΫαΚœ Β―ι1ΦΑ≤Ϋ÷ηI÷–ΒΡ Β―ιœ÷œσΘ§“ΣΫχ“Μ≤ΫΧΫΨΩ Β―ι1÷–ΑΉ…Ϊ≥ΝΒμ≤ζ…ζΒΡ‘≠“ρΘ§–η“ΣΆ≠ΚΆ¬»Μ·Χζ»ή“ΚΖ¥”ΠΘ§≤Ϋ÷ηIΒΡ Β―ι≤ΌΉς «œρ2 mL 0.1 mol/L FeCl3»ή“Κ÷–Φ”»κ0.15 gΆ≠ΖέΘ§’ώΒ¥ΓΔΨ≤÷ΟΘ§
¥πΑΗΈΣΘΚœρ2 mL 0.1 mol/L FeCl3»ή“Κ÷–Φ”»κ0.15 gΆ≠ΖέΘ§’ώΒ¥ΓΔΨ≤÷ΟΘΜ
ΔΎFe3+”κCuΖ¥”Π»τ”–Cu(I)…ζ≥…Θ§≤Ϋ÷ηI÷–”Π≤ζ…ζCuClΑΉ…Ϊ≥ΝΒμΘ§ΒΪ≤Ϋ÷ηI÷–œ÷œσΈΣ»ή“Κ±δΈΣάΕ…ΪΘ§≥Έ«εΆΗΟςΘ§ΒΉ≤Ω÷Μ”–…ΌΝΩΚλ…ΪΙΧΧε Θ”ύΘΜΈόΑΉ…Ϊ≥ΝΒμ≤ζ…ζΘ§‘ρ»œΈΣFe3+”κCuΖ¥”ΠΒΡ―θΜ·≤ζΈο≤ΜΚ§Cu(I)Θ§
¥πΑΗΈΣΘΚ»τ”–Cu(I)…ζ≥…Θ§≤Ϋ÷ηI÷–”Π≤ζ…ζCuClΑΉ…Ϊ≥ΝΒμΘ§ΒΪ≤Ϋ÷ηI÷–ΈόΑΉ…Ϊ≥ΝΒμ≤ζ…ζΘΜ
Δέ≤Ϋ÷ηII÷–Φ”»κKSCN»ή“ΚΚσ≥ωœ÷Κλ…ΪΘ§Ά§ ±”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…Θ§ΥΒΟςCu2+”κSCN-Ζ¥”Π…ζ≥…(SCN)2ΚΆ―«Ά≠άκΉ”Θ§―«Ά≠άκΉ””ꬻάκΉ”ΫαΚœ…ζ≥…CuClΑΉ…Ϊ≥ΝΒμΘ§(SCN)2”ꬱպΒΞ÷ ΒΡ–‘÷ œύΥΤΘ§Fe2+±Μ(SCN)2―θΜ·ΈΣFe3+Θ§Fe3+”ωSCN-≤ζ…ζΚλ…Ϊ»ή“ΚΘ§
¥πΑΗΈΣΘΚCu2+”κSCN-Ζ¥”Π…ζ≥…(SCN)2Θ§Fe2+±Μ(SCN)2―θΜ·ΈΣFe3+ΘΜ
ΔήCu2+”κSCN-ΖΔ…ζΖ¥”ΠΘΚ2Cu2+ + 4SCN-= 2CuSCNΓΐ+ (SCN)2Θ§CuSCN”κCl-ΖΔ…ζ≥ΝΒμΉΣΜ·Ζ¥”ΠΘΚCuSCN + Cl-=CuCl + SCN-Θ§SCN-ΦΧ–χ”κCu2+Ζ¥”ΠΘ§ΒΦ÷¬ΑΉ…Ϊ≥ΝΒμ±δΕύΘΜΥφΉ≈Ζ¥”ΠΒΡΫχ––SCN-÷πΫΞ±ΜœϊΚΡΘ§ΤΫΚβFe![]() Fe(SCN)3Ρφœρ“ΤΕ·Θ§ΒΦ÷¬Κλ…Ϊ÷πΫΞΆ »ΞΘ§
Fe(SCN)3Ρφœρ“ΤΕ·Θ§ΒΦ÷¬Κλ…Ϊ÷πΫΞΆ »ΞΘ§
¥πΑΗΈΣΘΚCu2+”κSCN-ΖΔ…ζΖ¥”ΠΘΚ2Cu2+ + 4SCN-= 2CuSCNΓΐ+ (SCN)2Θ§CuSCN”κCl-ΖΔ…ζ≥ΝΒμΉΣΜ·Ζ¥”ΠΘΚCuSCN + Cl-=CuCl + SCN-Θ§SCN-ΦΧ–χ”κCu2+Ζ¥”ΠΘ§ΒΦ÷¬ΑΉ…Ϊ≥ΝΒμ±δΕύΘΜΥφΉ≈Ζ¥”ΠΒΡΫχ––SCN-÷πΫΞ±ΜœϊΚΡΘ§ΤΫΚβFe3+ + 3SCN- ![]() Fe(SCN)3Ρφœρ“ΤΕ·Θ§ΒΦ÷¬Κλ…Ϊ÷πΫΞΆ »ΞΓΘ
Fe(SCN)3Ρφœρ“ΤΕ·Θ§ΒΦ÷¬Κλ…Ϊ÷πΫΞΆ »ΞΓΘ


 ΨΪ”ΔΩΎΥψΩ®œΒΝ–¥πΑΗ
ΨΪ”ΔΩΎΥψΩ®œΒΝ–¥πΑΗ ”Π”ΟΧβΒψ≤ΠœΒΝ–¥πΑΗ
”Π”ΟΧβΒψ≤ΠœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΆ§Έ¬Ά§―Ιœ¬Θ§‘Ύ3÷ßœύΆ§ΧεΜΐΒΡ ‘Ιή÷–Ζ÷±π≥δ”–Β»ΧεΜΐΜλΚœΒΡ2÷÷ΤχΧεΘ§ΥϋΟ« «ΔΌ NOΚΆNO2Θ§ΔΎ NO2ΚΆO2Θ§Δέ NH3ΚΆN2ΓΘœ÷ΫΪ3÷ß ‘ΙήΨυΒΙ÷Ο”ΎΥ°≤έ÷–Θ§≥δΖ÷Ζ¥”ΠΚσΘ§ ‘Ιή÷– Θ”ύΤχΧεΒΡΧεΜΐΖ÷±πΈΣV1ΓΔV2ΓΔV3Θ§‘ρœ¬Ν–ΙΊœΒ’ΐ»ΖΒΡ «
A.V1ΘΨV2ΘΨV3B.V1ΘΨV3ΘΨV2C.V2ΘΨV3ΘΨV1D.V3ΘΨV1ΘΨV2
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥–ΓΉι…ηΦΤ Β―ιΕ‘Νρ»Φ…’ΒΡ≤ζΈοΦΑΤδ–‘÷ Ϋχ––―ι÷ΛΘ§ Β―ιΉΑ÷Ο»γœ¬ΆΦΥυ ΨΓΘ
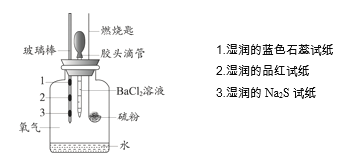
œ¬Ν– Β―ι ¬ Β”κΥυΒΟΫα¬έœύΖϊΒΡ «
Β―ι ¬ Β | ΥυΒΟΫα¬έ | |
A | Σ»σΒΡΤΖΚλ ‘÷ΫΆ …Ϊ | ÷ΛΟςΝρ»Φ…’ΒΡ≤ζΈο÷–”–SO2 |
B | Σ»σΒΡNa2S ‘÷Ϋ…œ≥ωœ÷Β≠ΜΤ…ΪΙΧΧε | ÷ΛΟςΝρΒΡ»Φ…’≤ζΈοΡή±ΜΜΙ‘≠≥…Νρ |
C | Σ»σΒΡάΕ…Ϊ ·»ο ‘÷Ϋ±δΚλ | ÷ΛΟςΝρΒΡ»Φ…’≤ζΈο÷–”–ΥαάύΈο÷ |
D | Φ”»κBaCl2»ή“Κ≤ζ…ζΑΉ…Ϊ≥ΝΒμ | ÷ΛΟςΝρ»Φ…’ΒΡ≤ζΈο÷–”–SO3 |
A.AB.BC.CD.D
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ”–œ¬Ν–άκΉ”ΨßΧεΩ’ΦδΫαΙΙ Ψ“βΆΦΘΚΓώΈΣ―τάκΉ”Θ§ΓπΈΣ“θάκΉ”Θ°“‘M¥ζ±μ―τάκΉ”Θ§N¥ζ±μ“θάκΉ”Θ§Μ·―ß ΫΈΣMN2ΒΡΨßΧεΫαΙΙΈΣ

≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩLED≤ζΤΖΒΡ Ι”ΟΈΣ≥« –‘ωΧμ…Ϊ≤ ΓΘœ¬ΆΦ ««β―θ»ΦΝœΒγ≥Ί«ΐΕ·LEDΖΔΙβΒΡ“Μ÷÷ΉΑ÷Ο Ψ“βΆΦΓΘœ¬Ν–”–ΙΊ–π ω’ΐ»ΖΒΡ «

A. a¥ΠΆ®»κ―θΤχΘ§ b¥ΠΆ®«βΤχ
B. Ά®»κH2ΒΡΒγΦΪΖΔ…ζΖ¥”ΠΘΚH2Θ≠2e- ΘΫ 2H+
C. Ά®»κO2ΒΡΒγΦΪΖΔ…ζΖ¥”ΠΘΚO2 + 4e- + 2H2O ΘΫ 4OHΘ≠
D. ΗΟΉΑ÷ΟΫΪΜ·―ßΡήΉν÷’ΉΣΜ·ΈΣΒγΡή
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ…ηNAΈΣΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΘ°œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
A. ΗΏΈ¬œ¬Θ§0.2 mol Fe”κΉψΝΩΥ°’τΤχΖ¥”ΠΘ§…ζ≥…ΒΡH2Ζ÷Ή” ΐΡΩΈΣ0.3NA
B. “Έ¬œ¬Θ§1 L pH=13ΒΡNaOH»ή“Κ÷–Θ§”…Υ°ΒγάκΒΡOH©¹άκΉ” ΐΡΩΈΣ0.1NA
C. «β―θ»ΦΝœΒγ≥Ί’ΐΦΪœϊΚΡ22.4 LΘ®±ξΉΦΉ¥ΩωΘ©ΤχΧε ±Θ§Βγ¬Ζ÷–Ά®ΙΐΒΡΒγΉ” ΐΡΩΈΣ2NA
D. 5NH4NO3![]() 2HNO3+4N2Γϋ+9H2OΖ¥”Π÷–Θ§…ζ≥…28 g N2 ±Θ§ΉΣ“ΤΒΡΒγΉ” ΐΡΩΈΣ3.75NA
2HNO3+4N2Γϋ+9H2OΖ¥”Π÷–Θ§…ζ≥…28 g N2 ±Θ§ΉΣ“ΤΒΡΒγΉ” ΐΡΩΈΣ3.75NA
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Ϋβ Ά ¬ ΒΒΡΜ·―ßΖΫ≥Χ ΫΜράκΉ”ΖΫ≥Χ Ϋ≤Μ’ΐ»ΖΒΡ «Θ® Θ©
A. œρAgCl–ϋΉ«“Κ÷–Φ”»κKI»ή“ΚΘΚAgCl(s)ΘΪIΘ≠(aq)ΘΫAgI(s)ΘΪClΘ≠(aq)
B. ΟςΖ·ΨΜΥ°ΘΚAl3ΘΪΘΪ3H2O![]() Al(OH)3ΘΪ3HΘΪ
Al(OH)3ΘΪ3HΘΪ
C. 90Γφ ±Θ§≤βΒΟ¥ΩΥ°÷–KwΘΫ3.8ΓΝ10Θ≠13ΘΚH2O(l)![]() HΘΪ(aq)ΘΪOHΘ≠(aq) ΓςHΘΦ0
HΘΪ(aq)ΘΪOHΘ≠(aq) ΓςHΘΦ0
D. ”Ο»»ΒΡ¥ΩΦν»ή“ΚΩ…“‘«εœ¥”ΆΈέΘΚCO32Θ≠ΘΪH2O![]() HCO3Θ≠ΘΪOHΘ≠
HCO3Θ≠ΘΪOHΘ≠
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΧΰAΒΡ÷ ΤΉΆΦ÷–Θ§÷ Κ…±»Ήν¥σΒΡ ΐ÷ΒΈΣ42ΓΘΧΦ«βΝΫ‘ΣΥΊΒΡ÷ ΝΩ±»ΈΣ6:1Θ§ΤδΚΥ¥≈Ι≤’ώ«βΤΉ”–»ΐΗωΖεΘ§ΖεΒΡΟφΜΐ±»ΈΣ1:2:3ΓΘA”κΤδΥϊ”–ΜζΈο÷°ΦδΒΡΙΊœΒ»γœ¬ΆΦΥυ ΨΘΚ

“―÷ΣΘΚCH2ΘΫCH2 ![]() HOCH2CH2OHΘ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
HOCH2CH2OHΘ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)FΒΡΫαΙΙΦρ ΫΈΣ__________________ΓΘ
(2)”–ΜζΈοC÷–ΒΡΙΌΡήΆ≈Οϊ≥Τ_______________________ΓΘ
(3)÷Η≥ωœ¬Ν–ΉΣΜ·ΒΡΜ·―ßΖ¥”Πάύ–ΆΘΚAΓζB__________ EΓζG____________ΓΘ
(4)–¥≥ωC”κ–¬÷ΤΒΡ«β―θΜ·Ά≠Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ___________________________ΓΘ
(5)E‘Ύ“ΜΕ®ΧθΦΰœ¬Ω…“‘œύΜΞΖ¥”Π…ζ≥…“Μ÷÷Νυ‘ΣΜΖ”–ΜζΈοΘ§‘ρ¥ΥΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ__________ ΓΘ
(6)”κEΜΞΈΣΆ§Ζ÷“λΙΙΧεΘ§«“ τ”ΎθΞάύΒΡ”–ΜζΈοΘ§≥ΐCH3OCOOCH3ΓΔCH3CH2OCOOHΆβΜΙ”– __________÷÷(Ζ÷Ή”÷–ΈόOΓΣOΦϋ)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΘ®1Θ©”–œ¬Ν–ΦΗΉιΈο÷ Θ§«κΫΪ–ρΚ≈Χν»κœ¬Ν–Ω’ΗώΡΎΘΚ
AΘ°CH2=CH-COOHΚΆ”ΆΥαΘ®C17H33COOHΘ© BΘ°12C60ΚΆ ·ΡΪ
CΘ°![]() ΚΆ
ΚΆ ![]() DΘ°35ClΚΆ37Cl EΘ°““¥ΦΚΆ““Εΰ¥Φ
DΘ°35ClΚΆ37Cl EΘ°““¥ΦΚΆ““Εΰ¥Φ
ΔΌΜΞΈΣΆ§ΈΜΥΊΒΡ «_____________ΘΜΔΎΜΞΈΣΆ§œΒΈοΒΡ «________________ΘΜ
ΔέΜΞΈΣΆ§ΥΊ“λ–ΈΧεΒΡ «__________ΘΜΔήΜΞΈΣΆ§Ζ÷“λΙΙΧεΒΡ «_____________ΘΜ
ΔίΦ»≤Μ «Ά§œΒΈοΘ§”÷≤Μ «Ά§Ζ÷“λΧεΘ§“≤≤Μ «Ά§ΥΊ“λ–ΈΧεΘ§ΒΪΩ…Ω¥≥… «Ά§“ΜάύΈο÷ ΒΡ «____ΓΘ
Θ®2Θ©–¥≥ωœ¬Ν–”–ΜζΈοΒΡœΒΆ≥ΟϋΟϊΜρΫαΙΙΦρ ΫΘΚ
AΘ°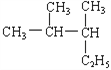 ΘΚ________________________ΘΜ
ΘΚ________________________ΘΜ
BΘ°CH3CH(CH3)C(CH3)2(CH2)2CH3ΘΚ_______________________ΘΜ
CΘ°3Θ§4-ΕΰΦΉΜυ-4-““ΜυΗΐΆιΘΚ______________________________ΘΜ
DΘ°2Θ≠ΦΉΜυΘ≠2Θ≠ΕΓœ©ΘΚ_________________ΘΜ
EΘ°2Θ§4Θ§6-»ΐœθΜυ±ΫΖ”ΘΚ___________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com