
利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是
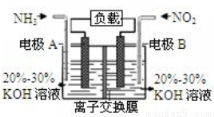
A.电流从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电极A极反应式为2NH3-6e-=N2+6H+
D.当有4.48LNO2(标准状况)被处理时,转移电子为0.8mol
科目:高中化学 来源:2016-2017学年河南省高二上9月月考化学卷(解析版) 题型:选择题
已知反应:①101kPa时,2C(s)+O2(g)═2CO(g);△H=﹣221kJ/mol
②稀溶液中,H+(aq)+OHˉ(aq)═H2O(l);△H=﹣57.3kJ/mol.下列结论正确的是( )
A.碳的燃烧热小于110.5 kJ/mol
B.①的反应热为221 kJ/mol
C. 浓硫酸与稀NaOH溶液反应的中和热为﹣57.3 kJ/mol
浓硫酸与稀NaOH溶液反应的中和热为﹣57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出的热量小于57.3 kJ
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
生活因化学而精彩,化学因实验而生动,实验因“洗涤”而更加精碗,关于沉淀或晶体洗涤的说法错误的是( )
A. 洗涤的目的一般是除去沉淀或晶体表面可溶性的杂质,提高纯度
B. 洗涤的试剂一般可选用蒸馏水、冰水、乙醇、该物质的饱和溶液
C. 洗涤的操作是向过滤器里的固体加洗涤剂,使洗涤剂浸没固体,待洗涤剂自然流下
D. 洗净的检验是检验最后一次洗涤液中是否含有形成沉淀的该溶液中的离子
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期9月月考化学试卷(解析版) 题型:选择题
向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2,在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是
A.Cu与Cu2O 的物质的量之比为2:1
B.硝酸的物质的量浓度为2.6mol/L
C.产生的NO在标准状况下的体积为4.48L
D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上第一次月考化学试卷(解析版) 题型:填空题
自来水厂生产自来水时,需要用到净水剂,对水进行消毒杀菌处理。
(1)漂白粉是常用的一种消毒剂,制备过程的化学方程式为 。漂白粉不能与家庭中常用的洁厕剂(一种酸性液体,主要含HCl)混合使用,否则容易造成人体中毒,其原因是(用有关的离子方程式表示) 。
(2)高铁酸钾(K2FeO4)是一种新型多功能水处理剂。工业上有多种方法制备高铁酸钾,其中一种方法是在氢氧化钾溶液中用次氯酸钠氧化氢氧化铁。该反应可用离子方程式表示为 。
(3)用高铁酸钾和锌制成的高铁碱性电池,能储存比普通碱性电池多50%电能,已知该电池的总反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,则负极的电极反应式是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上第一次月考化学试卷(解析版) 题型:选择题
在一定温度下,下列叙述不是可逆反应A(g)+2B(g) 2C(g)达到平衡状态标志的是
2C(g)达到平衡状态标志的是
①C的生成速率与C的分解速率相等;
②单位时间生成amol A,同时生成3amolB;
③A、B、C的浓度不再变化;
④混合气体平均摩尔质量不再变化
⑤混合气体的总压强不再变化;
⑥混合气体的物质的量不再变化;
⑦单位时间内消耗amol A,同时生成3amol B ⑧A、B、C的分子数比为1:3:2
A.②⑧ B.①⑥ C.②④ D.③⑧
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上第一次月考化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是
A.次氯酸钙溶液中通入过量的二氧化碳Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
B.硫酸亚铁溶液中加入过氧化氢溶液Fe2++2H2O2+4H+=Fe3++4H2O
C.用氨水吸收少量二氧化硫OH-+SO2=HSO3-
D.硝酸铁溶液加入过量氨水3NH3·H2O+Fe3+=Fe(OH)3↓+3NH4+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高一上第二次月考化学卷(解析版) 题型:选择题
一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应:N2(g)+3H2(g) 2NH3(g) ΔH = -92.2kJ•mol—1,测得0到10秒内,c(H2)减小了0.75mol•L—1,下列说法正确的是( )
2NH3(g) ΔH = -92.2kJ•mol—1,测得0到10秒内,c(H2)减小了0.75mol•L—1,下列说法正确的是( )
A.10到15秒内c(NH3) 增加量等于0.25mol •L—1
B.10秒内氨气的平均反应速率为0.025mol•L—1·s—1
C.达平衡后,分离出少量NH3,v正 增大
D.该反应的逆反应的活化能不小于92.2kJ•mol—1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江牡丹江高级中学高一9月月考化学卷(解析版) 题型:实验题
我国拥有丰富的海洋资源,海水制盐历史悠久,早在5000年前的仰韶文化时期,先人就利用海水煮盐。为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

(1)第①步操作的名称是 ,第②步判断BaCl2已过量的方法是 。
(2)第④步加入试剂的化学式为 。
(3)第⑤步操作所需玻璃仪器的名称是 。
(4)若 第⑤步、第⑥步顺序颠倒,将对实验结果产生影响,其原因是 。
第⑤步、第⑥步顺序颠倒,将对实验结果产生影响,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com