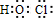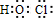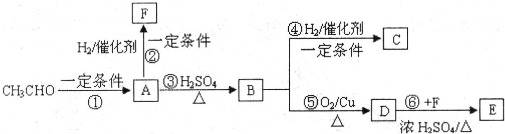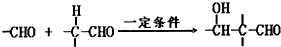
(2012?河东区一模)一定温度下在体积为5L的密闭容器中发生可逆反应.
(Ⅰ)若某可逆反应的化学平衡常数表达式为:K=
(1)写出该反应的化学方程式:
C(s)+H
2O(g)
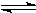
CO(g)+H
2(g)
C(s)+H
2O(g)
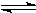
CO(g)+H
2(g)
;
(2)能判断该反应一定达到化学平衡状态的依据是
A、B、C
A、B、C
(填选项编号).
A.容器中气体的平均相对分子质量不随时间而变化
B.υ
正(H
2O)=υ
逆(H
2)
C.容器中气体的密度不随时间而变化
D.容器中总的物质的量不随时间而变化
E.消耗n mol H
2的同时消耗n mol CO
(Ⅱ)若该密闭容器中加入的是2molFe(s)与1mol H
2O(g),t
1秒时,H
2的物质的量为0.20mol,到第t
2秒时恰好达到平衡,此时H
2的物质的量为0.35mol.
(1)t
1~t
2这段时间内的化学反应速率v(H
2)=
0.03/(t2-t1)mol?L-1?s-1
0.03/(t2-t1)mol?L-1?s-1
.
(2)若继续加入2mol Fe(s),则平衡
不
不
移动(填“向正反应方向”、“向逆反应方向”或“不”),继续通入1mol H
2O(g) 再次达到平衡后,H
2的物质的量为
0.7
0.7
mol.
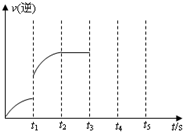
(3)该反应的逆反应速率随时间变化的关系如右图.t
1时改变了某种条件,改变的条件可能是
使用了催化剂
使用了催化剂
、
升高了温度
升高了温度
.(填写2项)

 (2012?河东区一模)一定温度下在体积为5L的密闭容器中发生可逆反应.
(2012?河东区一模)一定温度下在体积为5L的密闭容器中发生可逆反应.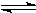 CO(g)+H2(g)
CO(g)+H2(g)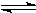 CO(g)+H2(g)
CO(g)+H2(g)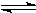 CO(g)+H2 (g)
CO(g)+H2 (g) 

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案