
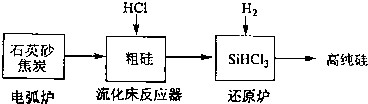
| 发生的主要反应 | |||||
| 电弧炉 | SiO2+2C
| ||||
| 流化床反器 | Si+3HCl
| ||||
| 还原炉 | SiHCl3+H2
|
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
| ||
| ||
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:
| A、金属钠和氧气反应,条件不同,产物不同 |
| B、钠钾合金通常状况下呈液态,可作原子反应堆的导热剂 |
| C、钠的化学活泼性很强,少量的钠可保存在有机溶剂CCl4中 |
| D、由于钠比较活泼,所以它能从盐的熔融物中置换出金属活动顺序表中钠后面的金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无法确定 |
| B、0.08 mol?L-1?min-1 |
| C、0.32 mol?L-1?min-1 |
| D、0.06 mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 2006年诺贝尔化学奖、医学和生理学奖分别授予在研究DNA、RNA方面有突出成就的美国科学家.核酸有两种:含核糖的是核糖核酸(RNA),含脱氧核糖的是脱氧核糖核酸(DNA),人们的基因组通过从细胞核里的DNA向蛋白质的合成机制发出生产蛋白质的指令运作,这些指令通过mRNA传送.核糖是合成核酸的重要原料,常见的两种核糖结构简式为:戊醛糖CH2OH-CHOH-CHOH-CHOH-CHO,下列关于核糖的叙述不正确的是( )
2006年诺贝尔化学奖、医学和生理学奖分别授予在研究DNA、RNA方面有突出成就的美国科学家.核酸有两种:含核糖的是核糖核酸(RNA),含脱氧核糖的是脱氧核糖核酸(DNA),人们的基因组通过从细胞核里的DNA向蛋白质的合成机制发出生产蛋白质的指令运作,这些指令通过mRNA传送.核糖是合成核酸的重要原料,常见的两种核糖结构简式为:戊醛糖CH2OH-CHOH-CHOH-CHOH-CHO,下列关于核糖的叙述不正确的是( )| A、戊醛糖和D-核糖互为同分异构体 |
| B、它们都能发生酯化反应 |
| C、戊醛糖属于单糖 |
| D、由戊醛糖→脱氧核糖(CH2OH-CHOH-CHOH-CH2-CHO)可看成是一个氧化过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
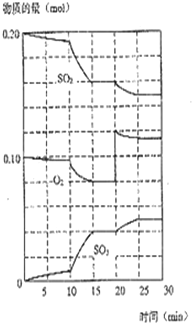 在一定条件下,二氧化硫和氧气发生如下反应:
在一定条件下,二氧化硫和氧气发生如下反应:| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验操作及现象 | 实验结论 | |
| A | 向2mL 0.1mol?L-1 CH3COOH溶液中滴加等浓度的NaHCO3溶液,有气泡产生 | 酸性: CH3COOH>H2CO3 |
| B | 向2mL 0.1mol?L-1 NaOH溶液中滴加3滴0.1mol?L-1 MgCl2溶液,出现白色沉淀后,再滴加3滴0.1mol?L-1 FeCl3溶液,出现红褐色沉淀 | 溶度积: Mg(OH)2>Fe(OH)3 |
| C | 在少量无水乙醇中加入金属Na,生成可以在空气中燃烧的气体 | CH3CH2OH是弱电解质 |
| D | 用3mL稀H2SO4溶液与足量Zn反应,当气泡稀少时,加入1mL浓H2SO4,又迅速产生较多气泡 | H2SO4浓度增大,反应速率加快 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com