
【题目】已知A,B,C,D分别是Cu、Ag、Fe、Al四种金属中的一种.已知①A,C均能与稀硫酸反应放出气体;②B与D的硝酸盐反应,置换出单质D;③C与强碱反应放出气体,由此可以推断A,B,C,D依次是( )
A.Fe、Cu、Al、Ag
B.Al、Cu、Fe、Ag
C.Cu、Ag、Al、Fe
D.Ag、Al、Cu、Fe
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某芳香烃A有如图转化关系: 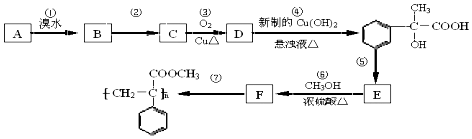
(1)写出反应②和⑤的反应条件:②;⑤ .
(2)写出A和D结构简式:A;D
(3)写出反应⑥的化学方程式: .
(4)反应③的反应类型 .
(5)根据已学知识和获取的信息,写出以CH3COOH, ![]() 为原料合成重要的化工产品
为原料合成重要的化工产品 ![]() 的路线流程图(无机试剂任选) 合成路线流程图示例如下:CH3CH2OH
的路线流程图(无机试剂任选) 合成路线流程图示例如下:CH3CH2OH ![]() H2C=CH2
H2C=CH2 ![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】匹多莫德是一种免疫调节剂,其合成路线如下:

已知:i ![]()
ii ![]()
(1)A中官能团名称________。
(2)B的结构简式________。
(3)②的反应类型________。
(4)写出谷氨酸生成F的化学方程式________。
该过程,还可能生成高聚物,写出任意一种的结构简式________。
(5)③的化学方程式________。
(6)写出半胱氨酸与HCHO反应生成G的化学方程式________。
(7)结合信息,写出以乙醇和必要无机试剂合成![]() 的路线________。
的路线________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下有:①5.4mL H2O ②5.6L CH4 ③3.01×1023个H2S分子 ④19.6g H2SO4 , 这些物质中,含分子个数由多到少的顺序是( )
A.③①②④
B.③①④②
C.①②③④
D.④②③①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气作为空气污染的主要来源之一,其中含有大量的有害物质,包括CO、NOx、碳氢化合物和固体悬浮颗粒等.为汽车尾气的治理,环境工作者面临着巨大的挑战.试回答以下问题: 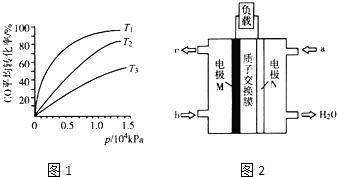
(1)用CH4催化还原NO,可以消除氮氧化物的污染.已知: ①CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=﹣1160kJmol﹣1
②CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=﹣574kJmol﹣1
由CH4将NO2完全还原成N2 , 生成CO2和水蒸气的热化学方程式是 .
(2)NOx也可以被NaOH溶液吸收而生成NaNO3、NaNO2 , 已知某温度下,HNO2的电离常数K=﹣9.7×10﹣4 , NO2﹣的水解常数K=﹣8.0×10﹣10 , 则该温度下水的离子积常数=(用含Ka、Kb的代数式表示),此时溶液的温度25℃(填“>”“<”或“=”).
(3)化工上利用CO合成甲醇,反应的热化学方程式为CO(g)+2H2(g)CH3OH(g)△H=﹣90.8kJmol﹣1 . 不同温度下,CO的平衡转化率与压强的关系如图1所示,图中T1、T2、T3的高低顺序是 , 理由是 .
(4)化工上还可以利用CH3OH生产CH3OCH3 . 在体积均为1.0L的恒容密闭容器中发生反应2CH3OH(g)CH3OCH3(g)+H2O(g).
容器换号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH2(g) | H2O(g) | ||
Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 207 | 0.20 | 0.090 | 0.090 |
该反应的正反应为反应(填“放热”或“吸热”).若起始时向容器I中充入CH3OH 0.15mol、CH3OCH30.15mol和H2O 0.10mol,则反应将向方向进行(填“正”或“逆”).
(5)CH3OH燃料电池在便携式通讯设备、汽车等领域有着广泛的应用.已知电池工作时的总反应方程式为2CH3OH+3O2═2CO2+4H2O,电池工作时的示意图如图2所示.质子穿过交换膜移向电极区(填“M”或“N”),负极的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.将纯水加热的过程中,Kw变大,pH变小
B.保存FeSO4溶液时,加入稀HNO3抑制Fe2+水解
C.FeCl3溶液蒸干、灼烧至恒重,最终得到FeCl3固体
D.向0.1 molL﹣1氨水中加入少量水,pH减小, ![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1molH2O的质量是18g
B.氮原子的质量就是氮的相对原子质量
C.1molH2SO4中含1molH2
D.氢氧化钠的摩尔质量是40g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛被称为“二十一世纪金属”,工业上用钛铁矿制备金属钛的工艺流程如下:

已知:钛铁矿主要成分与浓硫酸反应的主要产物是TiOSO4和FeSO4,TiOSO4遇水会水解。请回答下列问题:
(1)操作1用到的玻璃仪器除烧杯外还有_________;
(2)请结合化学用语解释将TiO2+转化为H2TiO3的原理_______________。
(3)已知钛的还原性介于铝与锌之间。如果可从Na、Zn、Fe三种金属中选一种金属代替流程中的镁,那么该金属跟四氯化钛反应的化学方程式是____________。
(4)电解TiO2来获得Ti是以TiO2作阴极,石墨为阳极,熔融CaO为电解质,用碳块作电解槽,其阴极反应的电极反应式是___________________________________。
(5)为测定溶液中TiOSO4的含量,先取待测钛液10 mL用水稀释至100 mL,加过量铝粉,充分振荡,使其完全反应:3TiO2+ +Al+6H+=3Ti3++Al3++3H2O。过滤后,取无色滤液20.00 mL,向其中滴加2~3滴KSCN溶液作指示剂,用______________________(填一种玻璃仪器的名称)滴加0.1000mol·L-1 FeCl3溶液,发生Ti3++Fe3+=Ti4++Fe2+。滴定终点时的现象是___________________________________,若用去了30.00mL FeC13溶液,待测钛液中TiOSO4的物质的量浓度是______________mol/L。
【答案】 漏斗、玻璃棒 溶液中存在平衡:TiO2++2H2O![]() H2TiO3+2H+,当加入水稀释、升温后,平衡正向移动 TiCl4+4Na
H2TiO3+2H+,当加入水稀释、升温后,平衡正向移动 TiCl4+4Na![]() Ti+4NaCl TiO2 + 4e- = Ti + 2O2- 酸式滴定管 溶液由无色变成红色且半分钟不褪色 1.50 mol/L
Ti+4NaCl TiO2 + 4e- = Ti + 2O2- 酸式滴定管 溶液由无色变成红色且半分钟不褪色 1.50 mol/L
【解析】钛铁矿用浓硫酸溶解,浓硫酸具有酸性,强氧化性,反应的主要产物是TiOSO4和FeSO4,还可能有少量Fe2(SO4)3;向所得溶液中加入大量水稀释后,加入过量铁粉还原Fe3+,过滤得到滤液中只含有TiOSO4和FeSO4;TiOSO4水解过滤后得到H2TiO3,H2TiO3加热灼烧得到TiO2,加入Cl2、过量碳高温反应生成TiCl4,TiCl4和Mg高温反应得到MgCl2和Ti。
(1)操作1为过滤,所需玻璃仪器有烧杯、漏斗、玻璃棒,故还缺少的仪器为:漏斗和玻璃棒;故答案为:漏斗、玻璃棒;
(2)TiOSO4遇水会水解,水解方程式为TiO2++2H2OH2TiO3+2H+,水解是吸热过程,加热能促进水解;加水稀释,促进水解。
故答案为:溶液中存在平衡:TiO2++2H2OH2TiO3+2H+,当加入水稀释、升温后,平衡正向移动;
(3)在流程中,金属镁置换出钛单质,反应方程式为:TiCl4+2Mg![]() Ti+2MgCl2。钛的还原性介于铝与锌之间,即还原性:Al>Ti>Zn,又因为还原性Na>Al>Zn>Fe,则Na>Al>Ti>Zn>Fe,故Na、Zn、Fe三种金属中只能选择金属Na代替镁。反应方程式为:TiCl4+4Na
Ti+2MgCl2。钛的还原性介于铝与锌之间,即还原性:Al>Ti>Zn,又因为还原性Na>Al>Zn>Fe,则Na>Al>Ti>Zn>Fe,故Na、Zn、Fe三种金属中只能选择金属Na代替镁。反应方程式为:TiCl4+4Na
![]() Ti+4NaCl。
Ti+4NaCl。
故答案为:TiCl4+4Na![]() Ti+4NaCl;
Ti+4NaCl;
(4)根据题意可知,TiO2作阴极,得电子,被还原得到单质Ti,则阴极电极反应式为:TiO2+4e-=Ti+2O2-。故答案为:TiO2+4e-=Ti+2O2-;
(5)FeC13有强的氧化性,腐蚀橡胶,且其溶液呈酸性,所以选择酸式滴定管。用KSCN溶液作指示剂,TiO2+反应完之前溶液为无色。当反应完,再滴入1滴FeC13溶液,溶液立即变红色,且半分钟后溶液颜色不褪色,到达滴定终点,停止滴定。
滴定过程中消耗n(FeC13)=0.1mol/L×0.03L=0.003mol。根据反应方程式可得出TiOSO4与Fe3+的关系式:TiOSO4~Ti3+~Fe3+,即滴定过程中n(FeC13)= n(TiOSO4)= 0.003mol。原待测液为10mL,稀释至100mL后,取2omL溶液进行滴定实验。所以原10mL待测液中含n(TiOSO4)= 0.003mol×![]() =0.015mol,c(TiOSO4)=
=0.015mol,c(TiOSO4)= ![]() =1.5 molL-1。
=1.5 molL-1。
故答案为:酸式滴定管;溶液由无色变成红色且半分钟不褪色 ;1.5 molL-1.
【题型】综合题
【结束】
11
【题目】Fe3+与CN-、F-、有机分子等形成的化合物具有广泛的应用。
(1)Fe3+基态核外电子排布式为________。
(2)乙酰基二茂铁是常用汽油抗震剂,其结构如图甲所示。此物质中碳原子的杂化方式是__________。
(3)C、N、O原子的第一电离能由大到小的顺序是___________________________。
(4)配合物K3Fe(CN)6可用于电子传感器的制作。与配体互为等电子体的一种分子的化学式为________________。已知(CN)2是直线形分子,并具有对称性,则(CN)2中π键和σ键的个数比为__________________。
(5)F-不仅可与Fe3+形成3-,还可以与Mg2+、K+形成一种立方晶系的离子晶体,此晶体应用于激光领域,其结构如图乙所示,则该晶体的化学式为__________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com