
【题目】在某有机物A的分子中,具有酚羟基、醇羟基、羧基等官能团,其结构简式如图.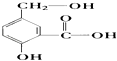
请同学们根据官能团
①A跟NaOH溶液反应的化学方程式是:
②A跟NaHCO3溶液反应的化学方程式是:
③A在一定条件下跟Na反应的化学方程式是: .
 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
【题目】随着各地治霾力度的加大,大力发展高性能燃料电池汽车成为研究课题。如图是某课题组设计的液体燃料电池示意图。下列有关叙述不正确的是

A. 该电池的优点是不产生污染气体,且液体燃料便于携带
B. 电池内部使用的是阴离子交换膜,OH-经交换膜移向负极
C. 该燃料电池的电极材料采用多孔纳米碳材料(如图),目的是增大接触面积,增加吸附量
D. 该电池中通入N2H4的电极为正极,发生的电极反应式为N2H4+4OH--4e-=N2↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是

A. Y、R两种元素的气态氢化物稳定性:Y>R
B. 简单离子的半径:X<Z<M
C. 最高价氧化物对应水化物的酸性:R<N
D. 由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
[探究一]
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是__________________。
(2)另称取铁钉6.0 g放入15.0 mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中的Fe2+,应选用_________。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.酸性KMnO4溶液
②乙同学取448 mL(标准状况)气体Y通入足量溴水中,发生下列反应:SO2+Br2+2H2O===2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33 g。由此推知气体Y中SO2的体积分数为________。
[探究二] 分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
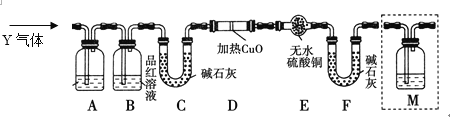
(3)装置B的作用是__________________________________________________。
(4)认为气体Y中还含有Q的理由是____________________ (用化学方程式表示)。
(5)为确认Q的存在,需要用到装置M,则M中装的试剂是______________,并将M添加于________(选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H2,预计实验现象应是_____________________________。
(7)若某气体可能由CO2、SO2、H2中的一种或多种组成,经测定其中氧的质量分数为50%,则该气体的组成可能为___________(填序号)。
a.SO2 b.H2、SO2 c.H2、CO2 d.CO2、SO2 e.SO2、CO2、H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于同温同压下等体积的CO2和CO的叙述:①质量相等②密度相等③所含分子数相等④所含碳原子数相等,其中正确的是
A. ①②③④ B. ②③④ C. ③④ D. ③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2FeO4是一种高效多功能水处理剂。制备Na2FeO4的方法如下:2FeSO4+6Na2O2 =2Na2FeO4 +2Na2O+2Na2SO4 +O2↑,对此反应下列说法中正确的是( )
A. 还原剂与氧化剂物质的量之比为1:3
B. 每生成44.8L氧气就有4 mol Fe2+ 被氧化
C. 还原产物是Na2FeO4和Na2O
D. 1mol FeSO4发生反应时,反应中共有4 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有三份白色固体分别为碳酸钠、碳酸氢钠及二者的混合物。某化学课外活动小组对其进行相关实验和探究。
I.甲组同学采用加热的方法确定其成分。
(1)除托盘天平、药匙、三脚架、泥三角、玻璃棒和干燥器外,完成本实验还需要的实验仪器有_________。
(2)该小组同学准确称取一定量的样品m1g,多次加热、冷却、称量直至恒重,质量为m2g。依据得出结论,请完成下表。
m2与m1的关系 | 结论 | |
① | 样品为Na2CO3 | |
② | 样品为NaHCO3 | |
③ | 样品为Na2CO3和 NaHCO3的混合物 |
II.乙组同学利用已鉴别出的NaHCO3和Na2CO3,继续进行实验,对于“能否用CaCl2鉴别的NaHCO3和Na2CO3”的问题进行探究。
(3)小组同学先将NaHCO3、Na2CO3、CaCl2固体分别配制成0.5mol/L的溶液。设汁如下实验方案:
表1
实验方案 | 预测现象 | |
实验1 | 向2mL Na2CO3溶液中滴加1mL CaCl2溶液 | 有白色沉淀生成 |
实验2 | 向2mL NaHCO3溶液中滴加1mL CaCl2溶液 | 无白色沉淀生成 |
若已知:①室温下,0.5mol/L NaHCO3溶液pH=8.5,溶液中c(HCO3-)=0.49 mol/L 。
②室温下, H2CO3的二级电离常数K2=5.6×10-11。
③Ksp(CaCO3)=2.8×10-9。
试估算使0.5mol/L NaHCO3溶液中的CO32-沉淀所需的c(Ca2+)应不低于_____mol/L,并由此得出结论:实验2的预测现象_____(填“正确”或“不正确”)。
⑷实际实验过程发现实验2的现象为白色沉淀并有无色气体生成。此现象对应的离子方程式为_____________。
(5)该小组同学继续设计实验对NaHCO3溶液与CaCl2溶液的反应进行探究,利用气体压力传感器得到的部分实验数据如下:(注:CaCl2溶液浓度相同)
表2 容器内气体浓度达到10000ppm所需时间
C(NaHCO3)/(mol/L) | 所需时间/s | |||
v(CaCl2):v(NaHCO3) | ||||
1:5 | 2:5 | 4:5 | 1:1 | |
1.0 | 142 | 124 | 114 | 156 |
0.5 | 368 | 264 | 244 | 284 |
0.25 | 882 | 450 | 354 | 632 |
0.1 | 1126 | 1316 | 816 | 1816 |
由实验数据可得出的结论是:
①当v(CaCl2):v(NaHCO3)一定时,随着_____,气体逸出速率减小;
②NaHCO3浓度在0.1~1.0mol/L,v(CaCl2)与v(NaHCO3)的比值为____时,气体逸出速率最快,可获得理想的实验观察效果。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】贝若霉是由阿司匹林,扑热息痛经化学法并合制备的解热镇痛抗炎药,其合成反应式(反应条件略去)如下: 
下列叙述错误的是( )
A.FeCl3溶液可区别阿司匹林和扑热息痛
B.1mol阿司匹林最多可消耗2mol NaOH
C.常温下贝若脂在水中的溶解度小于扑热息痛
D.C6H7NO是扑热息痛发生类似酯水解反应的产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH2=CHCl(氯乙烯,沸点-13.9C)是聚氯己烯的单体。某学习小组依据文献报道用乙烷氧氯化法设计制取氯乙烯。回答下列问题:
(1)甲组同学设计下列装置制备氯化氢和氧气。

①装置A和B用于制备和干燥HCl;浓硫酸显示的性质是_____;导管I的作用是_______;B的后续装置发生堵塞时,玻璃管II出现的现象是____________________。
②装置C制O2时发生反应的离子方程式为____________________。
(2)乙组同学利用甲组制得的氯化氢和氧气并利用下列装置制取氯乙烯。

①装置D除干燥三种气体外,另外两个作用是__________和____________。
②E中发生反应的化学方程式为______________________。
③装置G的作用是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com