
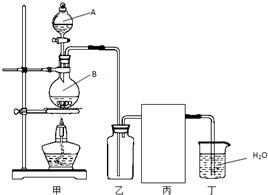
 (1)实验室制备HCl气体的反应为:
(1)实验室制备HCl气体的反应为:| 实验 次数 | 草酸溶液的体积 (mL) | ||
| 1 | 20.00 | ||
分析 (1)①熟悉仪器的形状及用途,说出其名称;
②氯化氢易溶于水,所以应加入防止倒吸装置;
③检验装置的气密性,应先在装置中形成封闭体系;
④浓盐酸易挥发,浓硫酸具有吸水性,溶于水放出大量的热有利于氯化氢的挥发;
(2)①高锰酸钾溶液颜色为紫红色,滴定终点时,溶液由无色变为红色,不用指示剂,当最后一滴溶液滴入,溶液的紫色退去,且30s内不复现,可达到滴定终点;
②氧化还原滴定法测定物质浓度,应测量的数据为反应消耗的高锰酸钾的体积,应读取的数据有滴定前读数,滴定后读数,据此算成消耗高锰酸钾的体积,为求实验的准确性,应测3次然后取平均值计算;
③设草酸溶液的浓度为c,根据关系式2KMnO4~5H2C2O4计算.
解答 解:(1)①图中A为分液漏斗,用来盛放液态反应物;
故答案为:分液漏斗;
②氯化氢易溶于水,为防止倒吸发生,丙应是防倒吸用的安全瓶,装置图为: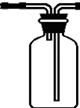 或者
或者 ;
;
故答案为: 或者
或者 ;
;
③检验装置的气密性,应先在装置中形成封闭体系,所以正确操作为:关闭分液漏斗活塞,把导管插入水中;
故答案为:关闭分液漏斗活塞,把导管插入水中;
④浓盐酸易挥发,浓硫酸具有吸水性,溶于水放出大量的热有利于氯化氢的挥发,向浓硫酸中滴加浓盐酸,不需要加热就能产生氯化氢,
故答案为:浓盐酸和浓硫酸;
(2)①高锰酸钾溶液颜色为紫红色,滴定终点时,溶液由无色变为红色,所以溶液恰好由无色变成浅紫红色,且半分钟不变化,达到滴定终点;
故答案为:溶液恰好由无色变成浅紫红色,且半分钟不变化;
②实验过程中应该测量的数据为滴定前滴定管的读数,滴定后滴定管的读数,测量3次,
数据表格如下:
| 实验 次数 | 草酸溶液的体积 (mL) | KMnO4溶液的体积 | ||
| 滴定前读数(mL) | 滴定后读数(mL) | KMnO4溶液体积(mL) | ||
| 1 | 20.00 | a | b | b-a |
| 2 | 20.00 | c | d | d-c |
| 3 | 20.00 | e | f | f-e |
| 实验 次数 | 草酸溶液的体积 (mL) | KMnO4溶液的体积 | ||
| 滴定前读数(mL) | 滴定后读数(mL) | KMnO4溶液体积(mL) | ||
| 1 | 20.00 | a | b | b-a |
| 2 | 20.00 | c | d | d-c |
| 3 | 20.00 | e | f | f-e |
点评 本题为实验题,考查了实验室制备氯化氢、氧化还原滴定法测定物质的浓度,明确物质的性质和滴定法测定物质浓度的步骤及注意事项是解题关键,注意有效数字的保留.


科目:高中化学 来源: 题型:选择题
| 相关实验 | 预期目的 | |
| A | 将SO2通入溴水,溴水褪色 | 验证SO2的还原性 |
| B | 将氯水加入淀粉KI溶液中 | 验证Cl非金属性比I强 |
| C | 在相同温度下,将表面积相同的铝条和镁条投入等体积同浓度的盐酸中,观察产生气泡的速率. | 比较同周期金属元素的金属性强弱. |
| D | 利用电解质溶液的导电性装置,检测AlCl3溶液的导电性 | 证明AlCl3是离子化合物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在溶剂中提高苯的比例,能提高溶液的导电性 | |
| B. | 电解时阳极的电极反应式为2Br--2e-=Br2 | |
| C. | 电解时可用铁作阳极材料 | |
| D. | 汽油样品应加在阴极区 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
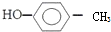
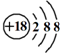
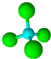
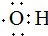
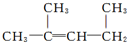 的名称:1,3-二甲基-2丁烯( )
的名称:1,3-二甲基-2丁烯( )| A. | ⑤ | B. | ④⑤ | C. | ③⑦ | D. | ②⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com