

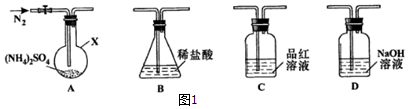
���� ��1������a�������Ƿ�ֹ���屻����ʱ����������
��2��ֹͣ���Ⱥ������ͨ��һ��ʱ���O2��ʹ���ɵĶ�������ȫ���ϳ������գ�
��3��������Һ���ƹ���Ϊ���㡢�������ܽ⡢ϴ��ת�ơ����ݡ�ҡ�ȵȲ���ѡ��������
��4���������������ữ��BaCl2��Һ�������ó������ˡ�ϴ�ӡ������������Ϊ4.66g��Ԫ���غ������Ԫ�غ���Ԫ�����ʵ���������õ���ѧʽ��
��5����װ��D��Ϊװ��������ʯ�ҵĸ���ܿ��ܿ����ж�����̼��ˮ��������Ӱ��ⶨ�����
��6���ζ����ⶨ��Һ��Na2SO3�ĺ�����Ҫ���������������Һ�����������Һ�����������������ܣ����������Һ���������������������ƣ�
��� �⣺��1����������������ˮ��������������Һ������������������©���������Ƿ�ֹҺ�嵹�����ʴ�Ϊ����ֹ������
��2��������У�ֹͣ���Ⱥ������ͨ��һ��ʱ���O2����Ŀ��Ϊʹ���ɵ�SO2ȫ����NaOH��Һ���գ�
�ʴ�Ϊ��ʹ���ɵ�SO2ȫ����NaOH��Һ���գ�
��3������IV�н�D��������Һ��ˮ���Ƴ�250mL��Һ��������Һʱ����IJ������������������ձ��⣬����Ҫ250 mL����ƿ�������õ��Ľ�ͷ�ιܣ�
�ʴ�Ϊ��250 mL����ƿ����ͷ�ιܣ�
��4��12.0gFexSy�����պ����ɵĶ����������գ���D��������Һ��ˮ���Ƴ�250mL��Һ��ȡ25.00mL����IV��������Һ������������˫��ˮ���ټ������������ữ��BaCl2��Һ�������ó������ˡ�ϴ�ӡ������������Ϊ4.66g����Ԫ���غ�n��S��=n��BaSO4��=$\frac{4.66g}{233g/mol}$=0.02mol��250ml��Һ�к���Ԫ�����ʵ���0.02mol��$\frac{250ml}{25ml}$=0.2mol����Ԫ�����ʵ���=$\frac{12.0g-0.2mol��32g/mol}{56g/mol}$=0.1mol����ѧʽ��n��Fe����n��S��=0.1��0.2=1��2��x=1��y=2����ѧʽΪFeS2��
�ʴ�Ϊ��FeS2��
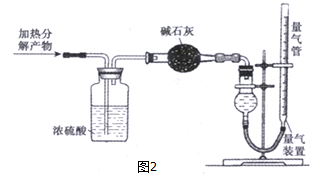
��5����װ��D��Ϊװ��������ʯ�ҵĸ���ܣ�ͨ���ⶨ��Ӧǰ�����ܵ�������������Ԫ�صĺ���ʱ����SO2���������ҿ����е�CO2��ˮ��������ʹ��������أ�������������
�ʴ�Ϊ������SO2���������ҿ����е�CO2��ˮ��������ʹ��������أ�
��6����Һ�г�����Na2SO4�⣬�����ܺ���Na2SO3��0.10mol•L-1KMnO4������Һ �ζ��յ���ҺԪ�ر�Ϊ�Ϻ�ɫ˵����Ӧ�ﵽ�յ㣬���������������������Ƶ�����������0.10mol•L-1KI������Һ������������������Һ����ѡ�Լ�Ϊ��0.10mol•L-1KMnO4������Һ�����������Һ����ǿ������ʢ����ʽ�ζ����У�
�������õķ�Ӧԭ��Ϊ2MnO4-+5SO32-+6H+=5SO42-+2 Mn2++3H2O��
�ʴ�Ϊ���٣���ʽ��2MnO4-+5SO32-+6H+=5SO42-+2 Mn2++3H2O��
���� ���⿼����������ɵ�ʵ��ⶨ���ζ�ʵ����жϺͶ������㣬ע���������ʵ��������գ���Ŀ�Ѷ��еȣ�


 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧʽ | ����ƽ�ⳣ�� |
| HCN | K=4.9��10-10 |
| CH3COOH | K=1.8��10-5 |
| H2CO3 | K1=4.4��10-7��K2=4.7��10-11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ͱ��� | B�� | H2O��H2O2 | ||
| C�� | 3H��2H | D�� | CH3CH2OH��CH3OCH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6�� | B�� | 7�� | C�� | 8�� | D�� | 9�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 5�� | B�� | 6�� | C�� | 3�� | D�� | 4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ������ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ں�c(NH4Cl)��3c(AlCl3)����Һ�еμ�ϡNaOH��Һ���������ӷ���ʽ������ʵ���������( )
A��Al3����3NH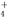 ��6OH��===Al(OH)3����3NH3��H2O
��6OH��===Al(OH)3����3NH3��H2O
B��2Al3����NH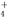 ��7OH��===2Al(OH)3����NH3��H2O
��7OH��===2Al(OH)3����NH3��H2O
C��Al3����3NH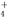 ��7OH��===AlO
��7OH��===AlO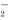 ��3NH3��H2O��2H2O
��3NH3��H2O��2H2O
D��Al3����5NH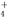 ��9OH��===5NH3��H2O��AlO
��9OH��===5NH3��H2O��AlO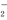 ��7H2O
��7H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ӱ�ʡ������ѧ�ڵ����ε��л�ѧ�Ծ��������棩 ���ͣ�ʵ����
KMnO4��MnO2������Ҫ��ѧ���ʣ���ʵ���ҿ������������ʹ�����ijѧϰС����������ʵ��Ʊ�������̽�����£�
I.MnO2���Ʊ���
��ѧϰС������˽���MnO2�����н϶��MnO��MnCO3��Fe2O3����Ʒת��Ϊ��MnO2ʵ�飬�乤���������£�
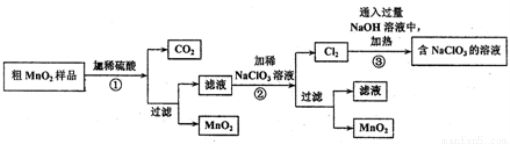
��ش��������⣺
��1���ڢٲ������У�����CO2�Ļ�ѧ����ʽΪ____________��
��2���ڢڲ������У�NaClO3����MnSO4�����ӷ���ʽΪ_____________��
��3���ڢ۲������У����յõ��Ĺ����NaClO3�⣬��һ���������������е�_________������ţ���
a. NaCl b. NaClO c. NaClO4 d. NaOH
��4��Ϊ�õ�������MnO2���뽫���˺��MnO2�ϲ������ϴ�ӡ�ϴ�ӳ������õIJ��������У�_____________���ж��Ƿ�ϴ�Ӹɾ���ѡ�õ��Լ���____________���ѧʽ����
��5��NaClO3��MnO2��һ�������¶���������Ũ������ȡ��������ȡ��������������NaClO3��MnO2�����ʵ���֮��Ϊ__________��
��6����ҵ�Ͽ�����ʯīΪ�缫����ữ����������ȡ�������̣��ù��̵�������ӦʽΪ___________��
II.KMnO4���Ʊ������ʣ�
��7��ʵ�����ɶ��������Ʊ�������ؿɷֶ������У�
��һ����MnO2��KOH���۲�ͨ��������2MnO2+4KOH+O2=2K2MnO4+2H2O
�ڶ�����ͨ��CO2����ʹK2MnO4�����绯��Ӧ����KMnO4��MnO2��
�ڶ�����ɷ�Ӧʱ��ת��ΪKMnO4��K2MnO4ռ��ȫ���İٷ���ԼΪ______�ߣ���ȷ��0.1%��
��8����С��ͬѧΪ��̽��KMnO4��Һ��Na2C2O4��Һ�ķ�Ӧ���̣�������KMnO4��Һ��ε���һ�������Na2C2O4��Һ�У��¶���ͬ��������������¼���������£�

�뽫MnO4-����C2O42- �����ӷ���ʽ����������
______MnO4-+C2O42-+_______=______Mn2++_____CO2��+_______
�����KMnO4��Һ��ɫʱ��仯�Ŀ���ԭ��_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���й����л���˵����ȷ����
������������ʱ�����Ҵ����������μ���Ũ������
�������յķ�����������˿����
����֬ˮ��ɵõ����������
����ά�غ͵��۶��Ƕ��ǣ�����Ϊͬ���칹��
�������顢��֬�͵�������һ����������ˮ��
���Ҵ����Ƿ�ˮ�����ý�����������
����ϩ�����鶼�ܷ����Ӿ۷�Ӧ
�൰����ˮ������ղ����Ƕ���
A���ڢ�B���٢ڢۢ�C���ܢݢޢ�D���٢�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com