
| A. | 凡是两种或两种以上的物质发生的反应都属于化合反应 | |
| B. | 在反应中,不一定所有元素的化合价都发生变化 | |
| C. | 一种元素被氧化,一定有另一种元素被还原 | |
| D. | 物质只有和氧气发生反应才是氧化还原反应 |
分析 A.两种或两种以上的物质发生的反应,其生成物不一定只有一种;
B.氧化还原反应中可能所有元素的化合价均变化,可能只有一种元素的化合价变化;
C.可能只有一种元素的化合价变化;
D.氧化还原反应中不一定有氧气参加.
解答 解:A.两种或两种以上的物质发生的反应,其生成物不一定只有一种,如盐酸与NaOH反应生成NaCl和水,为复分解反应,故A错误;
B.氧化还原反应中可能所有元素的化合价均变化,如氯气与少量溴化亚铁反应,可能只有一种元素的化合价变化,如氯气与水反应中只有Cl元素的化合价变化,故B正确;
C.可能只有一种元素的化合价变化,如氯气与NaOH的反应中,只有Cl元素的化合价变化,故C错误;
D.氧化还原反应中不一定有氧气参加,如氢气与氯气反应生成HCl,为氧化还原反应,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意结合实例分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
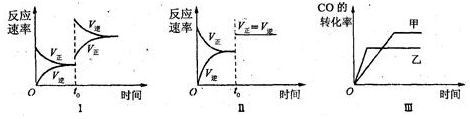
| A. | 图Ⅱ研究的只是t0时使用催化剂对反应速率的影响 | |
| B. | 图Ⅰ研究的是t0时缩小容器体积对反应速率的影响 | |
| C. | 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 | |
| D. | 图Ⅲ研究的是催化剂对化学平衡的影响,且甲使用了催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由H2(g)、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 | |
| B. | 高压比常压有利于由SO2和氧气合成SO3的反应 | |
| C. | 红棕色的NO2,加压后颜色先变深后变浅 | |
| D. | 黄绿色的氯水光照后颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3熔点高,可用于制作耐高温仪器 | |
| B. | 高纯度的硅单质用于制作光导纤维,光导纤维有导电性 | |
| C. | H7N9型禽流感病毒在高温条件下被杀死的过程是蛋白质变性 | |
| D. | 明矾净水与胶体的性质有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化羰在氧气中完全燃烧后的生成物是CO2和SO2 | |
| B. | C3O2与CO一样可以在氧气中燃烧生成CO2 | |
| C. | COS分子中所有原子都满足8电子稳定结构 | |
| D. | CO、C3O2、CO2都是碳的氧化物,它们互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2反应速率3 mol•l-1•min-1 | B. | N2反应速率0.3 mol•l-1•s-1 | ||
| C. | H2反应速率0.3mol•l-1•s-1 | D. | NH3反应速率0.4mol•l-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 干法 | Fe2O3、KNO3、KOH 混合加热共熔生成紫红色 K2FeO4 和 KNO2 等产物 |
| 湿法 | 强碱性介质中,Fe(NO3)3和 KClO 反应生成紫红色 K2FeO4溶液 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
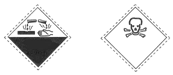
| A. | 腐蚀性、有毒 | B. | 自燃物品、易燃 | C. | 爆炸性、腐蚀性 | D. | 氧化剂、有毒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com