
现有部分短周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
T |
M层上电子数是K层上电子数的3倍 |
|
X |
最外层电子数是次外层电子数的2倍 |
|
Y |
常温下单质为双原子分子,其氢化物水溶液呈碱性 |
|
Z |
元素最高正价是+7价 |
(1)元素X位于元素周期表的第______________周期第________族,它的一种核素可测定文物年代,这种核素的符号是________。
(2)元素Y的原子结构示意图为______________,与氢元素形成一种离子YH,写出某溶液中含有该微粒的检验方法___________________________________________________。
(3)元素Z与元素T相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________。
a.常温下Z的单质和T的单质状态不同 b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(1)二 ⅣA C (2)  取适量溶液放入试管,然后加入浓NaOH溶液,加热,若产生能使湿润的红色石蕊试纸变蓝的气体,可以证明该溶液中含有NH (3)Cl b
取适量溶液放入试管,然后加入浓NaOH溶液,加热,若产生能使湿润的红色石蕊试纸变蓝的气体,可以证明该溶液中含有NH (3)Cl b
【解析】
试题分析:M层上电子数是K层上电子数的3倍,则T元素是S元素。最外层电子数是次外层电子数的2倍,所以X应该是碳元素。常温下单质为双原子分子,其氢化物水溶液呈碱性,则Y是氮元素。元素最高正价是+7价,因此Z是氯元素。
(1)元素X位于元素周期表的第第二周期第ⅣA族,它的一种核素可测定文物年代,这种核素的符号是C。
(2)元素Y的原子结构示意图为 。由于NH4+能和强碱反应发出氨气,氨气是碱性气体,据此可以鉴别,即取适量溶液放入试管,然后加入浓NaOH溶液,加热,若产生能使湿润的红色石蕊试纸变蓝的气体,可以证明该溶液中含有NH。
。由于NH4+能和强碱反应发出氨气,氨气是碱性气体,据此可以鉴别,即取适量溶液放入试管,然后加入浓NaOH溶液,加热,若产生能使湿润的红色石蕊试纸变蓝的气体,可以证明该溶液中含有NH。
(3)同周期自左向右,非金属性逐渐增强,氢化物的稳定性逐渐增强,所以非金属性较强的是氯元素,可以根据氢化物的稳定性检验,答案选b。
考点:考查元素周期表的结构、元素周期律的应用和判断以及NH4+的检验
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。


科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | K层和M层上电子数之和等于L层上电数子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| A | 该元素的一种原子,原子核中没有中子 |
| B | 有三个电子层,且K、M层电子数之和等于L层电子数 |
| C | 单质为双原子分子,其氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
| E | 1mol E的单质与足量的稀盐酸反应,可得到氢气33.6L (标准状况) |
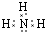
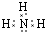
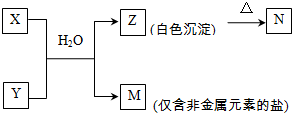
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的3倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 第三周期元素的简单离子中半径最小 |
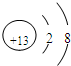
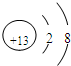
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
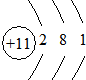
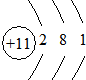
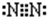
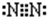
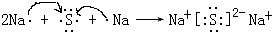
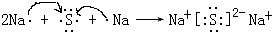
| O2 |
| O2 |
| H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
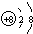
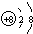
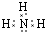
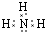
 Al(OH)3
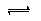
Al(OH)3 Al3++3OH-
Al3++3OH- Al(OH)3
Al(OH)3 Al3++3OH-
Al3++3OH-查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com