
【加试题】白藜芦醇是肿瘤、心血管病的预防药,主要来源于花生、葡萄、桑葚等植物。合成路线如下:
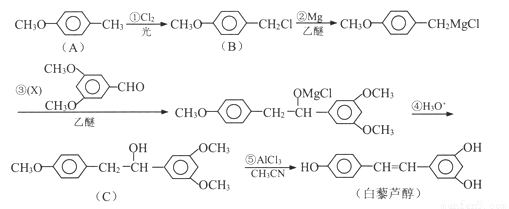
(1)下列说法不正确的是__________
A.第①步由A生成B的过程中,副产物主要为: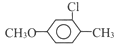
B.X能发生银镜反应,一定条件下1molX能与4molH2发生加成反应
C.第⑤步既发生取代反应,又发生了消去反应
D.化合物C的分子式为C17H22O4
(2)写出白藜芦醇与足量浓溴水反应后生成的有机物的结构简式__________。
(3)B与氢氧化钠水溶液反应生成Y,Y经过两步氧化生成Z(C8H8O3),写出Y、Z在浓硫酸作用下加热反应的化学方程式_____________。
(4)写出同时符合下列条件的X的同分异构体的结构简式_________。
①能与FeCl3溶液发生显色反应
②1H核磁共振谱显示有4个吸收峰,峰面积之比为1:1:2:6
(5)模仿上述合成路线,以乙烯为原料合成CH3CH(OH)CH2CH3,设计合成路线_________。(无机试剂任选)
科目:高中化学 来源:2017届福建省晋江市等四校高三第二次联合考试理综化学试卷(解析版) 题型:选择题
a、b、c、d为原子序数依次增大的短周期元素,c?的电子层结构与氖相同,化合物ac易溶于常见液体a2b,d的化合物灼烧时火焰呈黄色,下列有关叙述错误的是( )
A. 元素的非金属性次序为c>b>a B. d和其他3种元素均能形成离子化合物
C. 化合物acb中c元素的化合价为+1价 D. 元素a、b、d组成的固体化合物中存在离子键和共价键
查看答案和解析>>
科目:高中化学 来源:2017届江西省、临川一中高三1月联考理综化学试卷(解析版) 题型:填空题
铬是人体必需的微量元素,铬元素形成的化合物很多,常见的有Cr2O3、(NH4)2Cr2O7、[Cr(CH3COO)2]2•2H2O等,请回答下列问题:
(1)铬熔点较高,一般应用铝热反应制备铬单质。写出利用Cr2O3制备单质铬的化学方程式 ____________________ 。
(2)实验室常用Fe2+处理含(NH4)2Cr2O7的废水,其流程如下:
Cr2O72﹣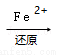 Cr3+
Cr3+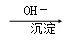 Cr(OH)3↓
Cr(OH)3↓
①(NH4)2Cr2O7中铬的化合价为 ________ 。
②第一步的离子方程式为_____ 。
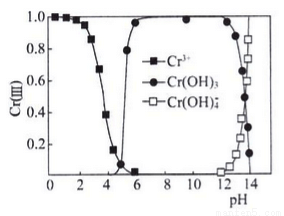
③已知三价铬[Cr(III)]在水溶液中的存在形态随pH的变化如下图,为尽可能除去铬元素实现废水达标排放,pH要控制在_______;若pH过高,溶液中残留铬量增大,其原因是 __________
(3)醋酸亚铬水合物{[Cr(CH3COO)2]2•2H2O,相对分子质量为376} 是常用的氧气吸收剂。实验室中以锌粒、三氯化铬溶液、醋酸钠溶液和盐酸为制备醋酸亚铬水合物,其装置如图所示,且仪器1中预先加入锌粒。
已知二价铬不稳定,极易被氧气氧化,不与锌反应。制备过程中发生的相关反应如下:
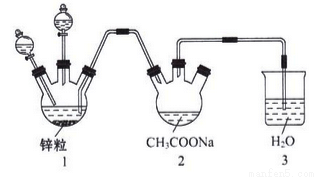
a.Zn+2HCl═ZnCl2+H2↑
b.Zn+2CrCl3═2CrCl2+ZnCl2
c.2Cr2++4CH3COO?+2H2O═[Cr(CH3COO)2]2•2H2O↓
①以上发生的反应中,属于氧化还原反应的是_______(填序号)。
②往仪器1中加入盐酸和三氯化铬溶液的顺序是先加入盐酸一段时间后再加入三氯化铬溶液,然后再加入盐酸。这样做的主要目的是____________________。
③已知其他反应物足量,实验时取用的CrCl3溶液中含溶质9.51g,取用的醋酸钠溶液为1.5L0.1mol•L-1实验后得干燥纯净的[Cr(CH3COO)2]2•2H2O 9.48 g,则该实验所得产品的产率为 __________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省、溧水高级中学)等六校高三2月联考化学试卷(解析版) 题型:选择题
下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作及现象 | 结论 |
A | 测定等物质的量浓度的Na2CO3和Na2SO3溶液的pH,前者pH比后者的大 | 非金属性:S>C |
B | 向苯酚浊液中滴加Na2CO3溶液,浊液变澄清 | CO32-结合质子能力比C6H5O-强 |
C | 向10 mL 0.2 mol·L-1NaOH溶液中滴入2滴0.1 mol·L-1MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol·L-1FeCl3溶液,白色沉淀转化为红褐色沉淀 | 相同温度下的Ksp:Mg(OH)2>Fe(OH)3 |
D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置,下层溶液显紫红色 | Fe3+的氧化性大于I2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届江苏省、溧水高级中学)等六校高三2月联考化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写不正确的是
A. 用氨水吸收过量的二氧化硫:NH3·H2O+SO2=HSO3-+NH4+
B. 用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+ = I2+2H2O
C. 向NH4Al(SO4)2溶液中滴入Ba(OH) 2溶液恰好使SO42-完全沉淀:2Ba2+ + Al3+ + 2SO42- + 4OH- = AlO2- + 2BaSO4↓+ 2H2O
D. 向含0.1mol·L-1 Na2CO3和0.2mol·L-1 NaOH的混合溶液中加入等体积的0.15mol·L-1的硫酸:CO32-+3H++2OH- = 2H2O+HCO3-
查看答案和解析>>
科目:高中化学 来源:2017届浙江省台州市高三上学期期末质量评估考试化学试卷(解析版) 题型:选择题
为探究固体A的组成和性质,设计实验并完成如下转化。
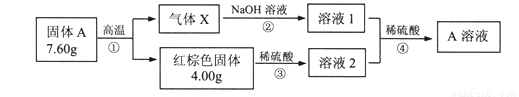
已知:X由两种化合物组成,若将X通入品红溶液,溶液褪色。若将X通入足量双氧水中,X可全部被吸收且只得到一种强酸,再稀释到1000mL,测得溶液的PH=1。在溶液2中滴加KSCN溶液,溶液呈血红色。请回答:
(1)固体A的化学式______________。
(2)写出反应①的化学方程式____________。
(3)写出反应④中生成A的离子方程式______________。
查看答案和解析>>
科目:高中化学 来源:2017届浙江省台州市高三上学期期末质量评估考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A. HCl、HBr、HI的分子间作用力依次增大,热稳定性也依次增强
B. N2和Cl2两种分子中,每个原子的最外层都具有8电子稳定结构
C. 在O2、CO2和SiO2中,都存在共价键,它们均由分子构成
D. KOH和MgCl2都是离子晶体,均在共价键和离子键
查看答案和解析>>
科目:高中化学 来源:2017届福建省漳州市八校高三2月联考化学试卷(解析版) 题型:选择题
下列表示物质结构的化学用语或模型正确的是( )
A. HF的电子式: H+[: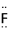 :]- B. HClO的结构式:H—O—Cl
:]- B. HClO的结构式:H—O—Cl
C. S2﹣的结构示意图: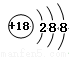 D. CH4分子的球棍模型:
D. CH4分子的球棍模型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com