
 乳酸亚铁{[CH3CH(OH)COO]2Fe}广泛应用于乳制品、营养液等,能溶于水,可由乳酸与FeCO3反应制得.
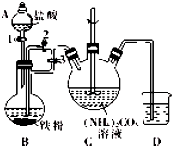
乳酸亚铁{[CH3CH(OH)COO]2Fe}广泛应用于乳制品、营养液等,能溶于水,可由乳酸与FeCO3反应制得.分析 Ⅰ.(1)装置B中铁粉与稀盐酸反应生成氢气和氯化亚铁,据此判断反应现象;
(2)关闭活塞3、打开活塞2,产生的氢气使圆底烧瓶中压强增大,从而可将氯化亚铁溶液压人装置C;
Ⅱ.(1)制得的FeCO3在空气中容易被氧化成铁离子,所以要加少量的铁粉,防止亚铁离子被氧化,据此答题;
(2)从溶液中获得晶体,应经过冷却结晶、过滤、洗涤、干燥等操作;
(3)先加入硫氰化钾溶液,溶液不变色,然后加入新制氯水,若溶液变为血红色则证明溶液中含有亚铁离子.
解答 解:Ⅰ.(1)装置B中铁粉与稀盐酸反应生成氯化亚铁和氢气,反应的离子方程式为:Fe+2H+=Fe2++H2↑,则观察到的现象为:铁粉逐渐溶解,液体中有气泡冒出、溶液变成浅绿色,
故答案为:液体中有气泡冒出、溶液变成浅绿色;
(2)先关闭活塞3、打开活塞2,铁与稀盐酸反应生成的氢气使圆底烧瓶中压强增大,从而将B中生成的FeCl2溶液压入装置C,
故答案为:关闭活塞3,打开活塞2;
Ⅱ.(1)制得的FeCO3在空气中容易被氧化成铁离子,所以要加少量的铁粉,防止亚铁离子被氧化,
故答案为:防止亚铁离子被氧化;
(2)在75℃下搅拌使之充分反应制得乳酸亚铁,从热溶液中获得乳酸亚铁晶体,应经过冷却结晶、过滤、洗涤、干燥等操作,
故答案为:冷却结晶(或低温蒸发、冷却结晶);过滤;
(3)证明乳酸亚铁中含Fe2+的方法是:取少量乳酸亚铁溶液于试管中,先加入硫氰化钾溶液,溶液不变色,然后加入新制氯水,若溶液变为血红色则证明溶液中含有亚铁离子,
故答案为:取少量乳酸亚铁溶液于试管中,先加入硫氰化钾溶液,溶液不变色,然后加入新制氯水,若溶液变为血红色则证明溶液中含有亚铁离子.
点评 本题考查了制备方案的设计与评价,题目难度中等,明确实验目的及化学实验基本操作方法为解答关键,注意掌握物质制备方案的设计与评价原则,试题知识点较多、综合性较强,充分考查学生的分析、理解能力及化学实验能力.


科目:高中化学 来源: 题型:多选题
| A. | 品红溶液褪色---漂白性 | B. | 高锰酸钾溶液褪色---漂白性 | ||
| C. | 导致酸雨---酸性氧化物 | D. | 通入H2S溶液中变浑浊---氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | 1 | 2 | 3 | 4 |
| V(Na2S2O3)(mL) | 28.32 | 25.31 | 25.30 | 25.32 |
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用焰色反应可以检验某些金属元素 | |
| B. | C元素和S元素在自然界中既有游离态,又有化合态 | |
| C. | SO2和Na2O2都能使紫色石蕊试液褪色,但漂白原理不同 | |
| D. | 新型陶瓷,玻璃,水泥不都是硅酸盐材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 福尔马林(蚁酸):加入足量饱和碳酸钠溶液充分振荡,蒸馏,收集馏出物 | |
| B. | 甘油(水):用分液漏斗分离 | |
| C. | 苯(苯酚):加NaOH溶液,充分振荡,分液 | |
| D. | 乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO32-、H+、NO3-、Na+ | B. | OH-、K+、NO3-、Cl- | ||
| C. | Mg2+、H+、OH-、SO42- | D. | Na+、Cu2+、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①⑤ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸化学式 | HClO | H2CO3 |
| 电离平衡常数 | K=3.0×10-8 | K1=4.4×10-7,K2=4.7×10-11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com