
| A. | SO3的水溶液能导电,所以SO3是电解质 | |
| B. | 自由移动离子数目多的电解质溶液导电能力一定强 | |
| C. | NaHSO4在水溶液里及熔融状态下均可电离出Na+、H+、SO${\;}_{4}^{2-}$ | |
| D. | NH3属于非电解质,但其水溶液能够导电 |
分析 A.导电了不是硫酸电离的,硫酸为电解质,三氧化硫为非电解质;
B.溶液导电性与溶液中离子浓度大小有关,与离子数目多的,离子浓度不一定大;
C.硫酸氢钠为强电解质,在溶液中完全电离出钠离子、氢离子和硫酸根离子,但是在熔融状态下锂电离出钠离子和硫酸氢根离子;
D.氨气溶于水生成一水合氨,一水合氨能够电离,所以氨水导电,而氨气不电离,属于非电解质.
解答 解:A.SO3的水溶液能导电,导电离子是硫酸电离的,硫酸为电解质,而SO3不电离,属于非电解质,故A错误;
B.自由移动离子浓度越大的电解质溶液导电能力一定强,但是离子数目多的溶液中离子浓度不一定大,导电能力不一定强,故B错误;
C.NaHSO4在水溶液里电离出Na+、H+、SO42-,而在熔融状态下电离出Na+、HSO4-,故C错误;
D.氨气在溶液中不发生电离,为非电解质,氨气溶于水形成能够导电的氨水,故D正确;
故选D.
点评 本题考查了电解质与非电解质、溶液导电性强弱判断,题目难度不大,明确电解质与非电解质的概念为解答关键,注意影响溶液导电性强弱的因素,为易错点,试题侧重基础知识的考查,培养了学生的灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
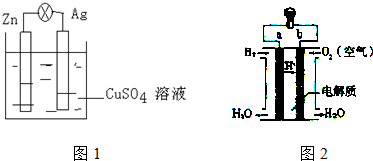
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
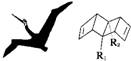 始祖鸟烯(Pterodactyladiene),形状宛如一只展翅飞翔的鸟,其键线式如图,其中R1、R2为烷烃基.则下列有关始祖鸟烯的说法中正确的是( )
始祖鸟烯(Pterodactyladiene),形状宛如一只展翅飞翔的鸟,其键线式如图,其中R1、R2为烷烃基.则下列有关始祖鸟烯的说法中正确的是( )| A. | 始祖鸟烯与CH2═CH-CH═CH2互为同系物 | |
| B. | 若R1、R2为-CH3,则其化学式为C12H16 | |
| C. | 若R1═R2,一定条件下烯烃双键碳原子上的氢也能取代,则始祖鸟烯环上的二氯代物有10种 | |
| D. | 始祖鸟烯既能使酸性高锰酸钾褪色也能使溴水褪色,其褪色原理是一样的 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1,3二氯丙烷 | B. | 1,1二氯丙烷 | C. | 1,2二氯丙烷 | D. | 2,2二氯丙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 碳 | 氮 | Y | |
| X | 硫 | Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取25.0gCuSO4•5H2O溶于1L水中 | |
| B. | 取16.0gCuSO4•5H2O溶于水,再稀释至1L | |
| C. | 将胆矾加热失去结晶水,再取无水硫酸铜16.0g溶于1L水 | |
| D. | 取25.0gCuSO4•5H2O溶于水,再稀释配成1L溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
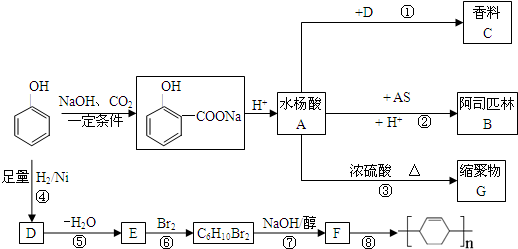
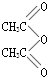 ,
, .
.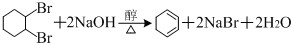 .
.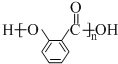 .
.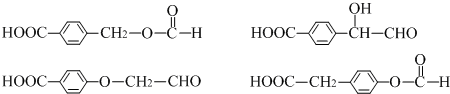 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com