
下列有关物质的分类或归类不正确的是
①混合物:漂白粉、福尔马林、水玻璃 ②化合物:CaCl2、烧碱、HD
③电解质:明矾、盐酸、硫酸钡 ④纯净物:干冰、冰水混合物、红宝石
⑤同位素:12 6C、13 6C、14 6C ⑥同系物:C2H4、C3H6、C4H8
A.只有② B.①②③④
C.只有③④ D.②③④⑥
 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
下列离子在溶液中能大量共存的是( )。
A. Na+、CO32—、SO42—、H+ B. K+、OH—、H+、Cl—
C. Mg2+、H+、NO3—、SO42— D. Fe3+、K+、OH—、NO3—
查看答案和解析>>
科目:高中化学 来源: 题型:
阿托酸乙酯可用于辅助胃肠道痉挛及溃疡。阿托酸乙酯的一种合成路线如下图所示:
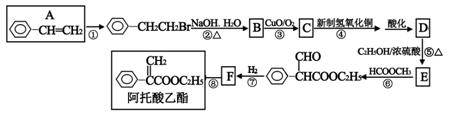
请回答下列问题:
(1)E的分子式为 ,F的结构简式 ,阿托酸乙酯所含官能团的名称 ;
(2)在反应①②③④⑤⑥⑦⑧中,属于取代反应的有 ;
(3)反应③的方程式 。
(4)有关阿托酸乙酯的说法正确的是 ( )
A.能使高锰酸钾褪色,不能使溴水褪色
B.1mol阿托酸乙酯最多能与4molH2加成
C.能发生加成、加聚、氧化、水解等反应
D.分子式为C11H13O2
(5)D的同分异构体有多种,符合含有苯环且能与碳酸氢钠反应放出气体的同分异构体有 种(不包含D)。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示的装置,在铁圈和银圈的焊接处,用一根棉线将其悬吊在盛水的烧杯中,使之平衡。小心地向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是
A.铁圈和银圈左右摇摆不定 B.保持平衡状况
C.铁圈向下倾斜 D.银圈向下倾斜
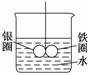
查看答案和解析>>
科目:高中化学 来源: 题型:
工业制备氯化铜时,将浓盐酸用蒸气加热到80℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO),充分搅拌使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液[参考数据:pH≥9.6时,Fe2+完全水解成Fe(OH)2;pH≥6.4时,Cu2+完全水解成Cu(OH)2;pH≥3.7时,Fe3+完全水解成Fe(OH)3]。请回答以下问题:
(1)第一步除Fe2+,能否直接调整pH=9.6将Fe2+沉淀除去?______,理由是______
_____________________________________________________________________。
有人用强氧化剂NaClO将Fe2+氧化为Fe3+:
①加入NaClO后,溶液的pH变化是___________(填序号);
A.一定增大 B.一定减小
C.可能增大 D.可能减小
②你认为用NaClO作氧化剂是否妥当?__________,理由是_________________
___________________________________________________________。
③现有下列几种常用的氧化剂,可用于除去该混合溶液中Fe2+的有_________(填序号)。
A.浓HNO3 B.KMnO4 C.Cl2 D.O2
(2)除去溶液中的Fe3+的方法是调整溶液的pH=3.7,现有下列试剂均可以使强酸性溶液的pH调整到3.7,可选用的有__________(填序号)。
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的操作与现象描述及相关结论正确的是
A.取少量溶液,加几滴KSCN溶液,若有血红色沉淀产生则溶液中含有Fe3+
B.Na2SO4·10H2O失水时吸热,结晶时放热,因而该晶体可作为储热材料实现化学能与热能的相互转换
C.取5mL0.1mol·L-1KI溶液,滴加0.1mol·L-1FeCl3溶液5-6滴,继续加入2mLCCl4,充分振荡后静置,取上层溶液加KSCN溶液,无明显现象
D.取一小块金属钠,用滤纸吸干表面的煤油,放入烧杯中,再加一定量的水,观察现象
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下,浓度均为0.1 mol·L-1的4种钠盐溶液pH如下表:
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
下列说法中正确的是
A.足量SO2通入NaClO溶液中发生反应的离子方程式为:H2O+SO2+ClO-=HClO+HSO3-
B.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO溶液,pH最大的是H2SO3
D.NaHSO3溶液中离子浓度大小顺序为:c(Na+)> c(H+)>c(HSO3-) >c(SO32-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将某一元酸HA和NaOH溶液等体积混合,实验信息如下:
| 实验编号 | c(HA)/ mol·L-1 | c(NaOH)/ mol·L-1 | 反应后溶液pH |
| 甲 | 0.1 | 0.1 | pH=9 |
| 乙 | c1 | 0.2 | pH=7 |
下列判断不正确的是 ( )
A.c1一定大于0.2 mol·L-1
B.HA的电离方程式是HA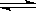 H++A-
H++A-
C.甲反应后溶液中:c(Na+) > c(OH-) > c(A-) > c(H+)
D.乙反应后溶液中:c(Na+) < c(HA)+c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
用Cl2生产某些含氯有机物时会产生副产物HC1。利用反应A,可实现氯的循环利用。
反应A: 4HCl+O2 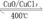 2Cl2+2H2O
2Cl2+2H2O
(1)已知:i 反应A中, 4 mol HCI被氧化,放出115.6kJ的热量。[
mol HCI被氧化,放出115.6kJ的热量。[
ii 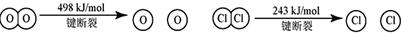 m
m
①H2O的电子式是_______________.
②反应A的 热化学方程式是____________________________________________________。
热化学方程式是____________________________________________________。
③断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差约为__________kJ,H2O中H—O 键比HCl中H—Cl键(填“强”或“弱”)_______________。
键所需能量相差约为__________kJ,H2O中H—O 键比HCl中H—Cl键(填“强”或“弱”)_______________。
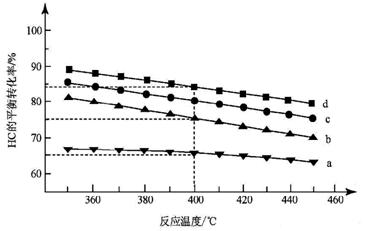 (2)对于反应A,下图是4种投料比[n(HCl):n(O2),
(2)对于反应A,下图是4种投料比[n(HCl):n(O2),
分别为1:1、2:1、4:1、6:1]下,反应温度对HCl平衡转化率影响的曲线。
①曲线b对应的投料比是__________。
②当曲线b、c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度高低与投料比多少的关系是 ______________________________。
______________________________。
③投料比为2:1、温度为400℃时,平衡混合气中Cl2 的物质的量分数__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com