
| A. | 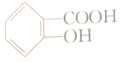 | B. | 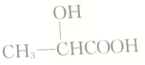 | C. | 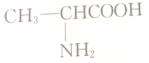 | D. | 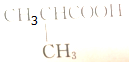 |
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
| A. | CO2是还原剂,在该反应中被氧化 | |
| B. | Na2O2是氧化剂,在该反应中发生氧化反应 | |
| C. | 氧化剂和还原剂的物质的量之比为1:2 | |
| D. | 若有2 mol Na2O2参加反应,则有2 mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ①②③④ | C. | ①③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应Ⅰ中HCl是氧化剂 | B. | 反应Ⅱ中Cl2被氧化,发生氧化反应 | ||
| C. | 还原性:CoCl2>HCl>I2 | D. | 氧化性:Co2O3>Cl2>HIO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 化学反应 | 离子方程式 | 评价 |
| A | 碳酸钙与盐酸 | CO32-+2H+=H2O+CO2↑ | 错误,碳酸钙是弱电解质,不应写成离子形式 |
| B | 向次氯酸钙溶液通入过量CO2 | Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | 正确 |
| C | 石灰水中滴加少量NaHCO3溶液 | Ca2++HCO3-+OH-=CaCO3↓+H2O | 错误,不满足Ca(OH)2的配比 |
| D | 过量铁屑溶于稀硝酸 | 3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O | 正确 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石 | B. | 氧化铝 | C. | 聚乙烯 | D. | 不锈钢 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若m=1,则M(NO3)m溶液和氨水互滴时的现象可能不同 | |
| B. | 若m=2,则在空气中蒸干、灼烧MSO4溶液一定能得到MSO4 | |
| C. | 若m=3,则MCl3与足量氢氧化钠溶液反应一定生成M(OH)m | |
| D. | Mm+离子一定不能与酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
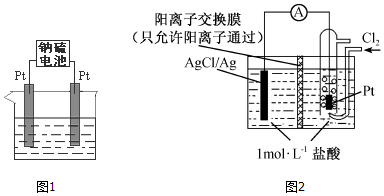
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com