
| A、③⑤①② | B、③② |
| C、②③④⑤ | D、③④①② |


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
| A、澄清透明的溶液中:K+、Al3+、SO42-、MnO4- |
| B、0.1mol?L-1CH3COONa溶液中:H+、Ca2+、Cl-、NO3- |
| C、滴入KSCN显血红色的溶液中:NH4+、Mg2+、S2-、Cl- |
| D、c(H+)=1×10-13 mol?L-1的溶液中:Na+、NH4+、SO42-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 转化为 |
| A、O2和Cr(OH)3是反应物 |
| B、产物中一定有H2O |
| C、H2O2是氧化剂 |
| D、2 mol H2O2反应需要3 mol H2CrO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
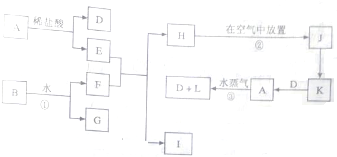
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 在一烧杯中盛有稀H2S04溶液.同时有一表面光滑的塑料小球悬浮于溶液中央,如图所示.向该烧杯里缓缓注入与稀H2SO4等密度的Ba(OH)2溶液至恰好完全反应.在此实验过程中
在一烧杯中盛有稀H2S04溶液.同时有一表面光滑的塑料小球悬浮于溶液中央,如图所示.向该烧杯里缓缓注入与稀H2SO4等密度的Ba(OH)2溶液至恰好完全反应.在此实验过程中查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl) |
| B、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C、1.0 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| D、某二元弱酸酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+2c(A2-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com