
除去下列物质中所含杂质(括号中的物质)所选用的试剂和装置均正确的是( )
Ⅰ.试剂:①KMnO4/H+ ②NaOH溶液 ③饱和Na2CO3溶液 ④H2O ⑤Na ⑥Br2/H2O ⑦Br2/CCl4
Ⅱ装置:
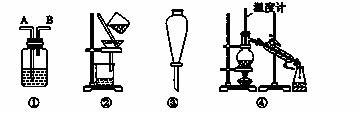
| 选项 | 物质 | 试剂 | 装置 |
| A | C2H6(C2H4) | ⑥ | ① |
| B | 苯(苯酚) | ① | ③ |
| C | CH3COOC2H5(CH3COOH) | ③ | ② |
| D | 甲苯(二甲苯) | ⑦ | ④ |
 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2===Na2S2O5。
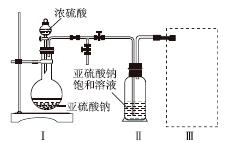
(1)装置Ⅰ中产生气体的化学方程式为______________________________________。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是______。
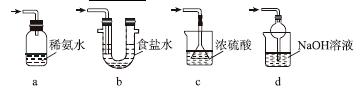
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填序号)。
实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO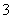 的电离程度大于水解程度,可采用的实验方法是________(填序号)。
的电离程度大于水解程度,可采用的实验方法是________(填序号)。
a.测定溶液的pH b.加入Ba(OH)2溶液
c.加入盐酸 d.加入品红溶液
e.用蓝色石蕊试纸检测
(5)检测Na2S2O5晶体在空气中已被氧化的实验方案是
________________________________________________________________________
________________________________________________________________________。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O===H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测定结果________(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化属于物理变化的是 ( )
A.氧气在放电条件下变成臭氧,
B.胆矾在加热条件下变成白色无水硫酸铜
C.漂白的草帽久置空气中变黄
D.氢氧化铁胶体加入硫酸镁产生沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
我国制碱工业的先驱——侯德榜先生,1939年发明了著名的侯氏制碱法,其核心反应原理可用如下化学方程式表示:NH3+C02+NaCl+H20=NH4CI+NaHCO3(晶体),依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和。
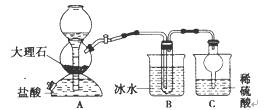
(1)A装置中所发生反应的离子方程式为 .
C装置中稀硫酸的作用为
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100 g水);
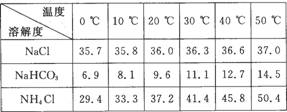
参照表中数据,请分析B装置中使用冰水的目的是
(3)该校学生在检查完此套装置的气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出
应在 装置之间(填写字母)连接一个盛有 的洗气装置,其作用 。
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85 g,实验后得到干燥的NaHCO3晶体的质量为5.04 g,则NaHCO3的产率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
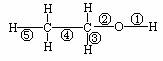
乙醇分子中不同的化学键如右图。下列关于乙醇在不同的反应中断裂化学键的说法
错误的是
A.与金属钠反应时,键①断裂
B.在Cu催化下与O2反应时,键①、③断裂
C.与乙酸在浓硫酸作用下反应时,键②断裂
D.与浓硫酸共热至140℃时,键①或键②断裂;共热至170℃时,键②、⑤断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
某芳香烃A,分子式为C8H10 ;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色;J分子内有两个互为对位的取代基。在一定条件下有如下的转化关系 (无机物略去):
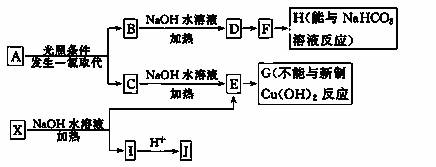
(1)J中所含的含氧官能团的名称为________________________________________。
(2)E与H反应的化学方程式是___________________________________________;
反应类型是______________。
(3)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物M,以M为单体合成的高分子化合物的名称是____________。
(4)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式。①与FeCl3溶液作用显紫色;②与新制Cu(OH)2悬浊液作用产生红色沉淀;③苯环上的一卤代物有2种;
④核磁共振氢谱显示有四种波峰,且波峰的面积之比为1∶2∶2∶1。________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某仅含C、H、O三种元素的有机物A 7.4 g与足量O2点燃后,所得产物依次通过盛有浓H2SO4和碱石灰的仪器,两仪器分别增重9 g、和17.6 g;同温同压下,A蒸汽的密度是H2的37倍,则能够与钠反应放出H2的A的同分异构体的数目为(不考虑立体异构) ( )
A.8 B.6 C.4 D.2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com