
【题目】氨与硝酸都是氮的重要化合物,在工农业生产中有广泛应用。回答下列问题。
(1)氨气的制备
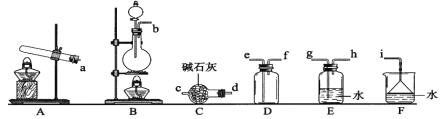

①氨气制取的发生装置可以选择上图中的_________(填字母),反应的化学方程式为__________。
②选择上图装置组装一套实验装置来收集一瓶干燥的氨气,所选装置的连接顺序为:发生装置→______→______,______→_____→i(按气流方向,用小写英文字母表示)。
③可用如右装置进行氨的喷泉实验,引发喷泉的操作是__________。
(2)如图所示,NH3经一系列反应可以得到HNO3。

①反应①的化学方程式为__________________________。
②产物NO是大气污染物之一。在400℃左右且有催化剂存在的情况下,可用氨将一氧化氮还原为无色无毒气体。该反应的化学方程式_______________________。
【答案】A Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O d c f e 先挤压胶头滴管的水进入圆底烧瓶,再打开止水夹 4NH3+5O2
CaCl2+2NH3↑+2H2O d c f e 先挤压胶头滴管的水进入圆底烧瓶,再打开止水夹 4NH3+5O2![]() 4NO+6H2O 4NH3+6NO
4NO+6H2O 4NH3+6NO![]() 5N2+6H2O
5N2+6H2O
【解析】
(1) ①在实验室中是用铵盐与碱共热制取氨气的,反应的化学方程式为Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O;反应物都是固体,反应需要在加热条件下进行,为防止产生的水回流,使试管炸裂,所以要选择A装置制取氨气;
CaCl2+2NH3↑+2H2O;反应物都是固体,反应需要在加热条件下进行,为防止产生的水回流,使试管炸裂,所以要选择A装置制取氨气;
②选用A装置制取氨气;然后用C装置干燥氨气;然后选用D装置用向下排空气的方法收集氨气,为防止氨气污染空气,同时要注意防止倒吸现象的发生,最后用F进行尾气处理,按气流方向,用小写英文字母表示连接顺序为a→d→c→f→e→i;
③可用如右装置进行氨的喷泉实验,引发喷泉的操作是先挤压胶头滴管,使其中的水进入圆底烧瓶,然后打开止水夹,烧瓶内氨气溶解在水中,气体压强减小,烧杯内的水在大气压强作用下不断进入烧瓶内,从而形成喷泉;
(2) ①NH3与氧气在催化剂存在时,在加热条件,被氧化产生NO,同时有水生成,反应的化学方程式为4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
②在400℃左右且有催化剂存在的情况下,可用氨将一氧化氮还原为无色无毒气体是N2和CO2,根据电子守恒、原子守恒。可得该反应的化学方程式:4NH3+6NO![]() 5N2+6H2O。
5N2+6H2O。


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源: 题型:
【题目】下面叙述正确的是
A. 氯水应保存在无色的细口试剂瓶中
B. 液溴应保存在磨口玻璃塞的试剂瓶中,并加少量水进行水封
C. 能使湿润的淀粉碘化钾试纸变蓝的气体一定是氯气
D. 碘易溶于酒精,所以可以用酒精从碘水中萃取碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下图所示装置制备氯气并进行一系列相关实验(夹持设备及必要的加热装置已省略)。

(1)整套装置装配完毕后,首先进行的操作是______________________,再添加试剂。
(2)实验室常用MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O制取氯气:
MnCl2+Cl2↑+2H2O制取氯气:
①实验时,通常采用密度为1.19g/cm3、浓度为36.5%的浓盐酸。该浓盐酸的物质的量浓度为___________________________。
②标准状况下,上述反应每生成4.48L氯气,转移电子的物质的量为_________ mol。
(3)洗气装置B的作用是除去Cl2中的HCl气体,同时用作安全瓶(监测实验时装置C中是否发生堵塞)。若装置C发生堵塞,装置B中将观察到的现象是_____________。
(4)装置C的作用是验证氯气是否具有漂白性。为此,实验时装置C中I、II、III处依次放入的物质是___________(填字母)。
A | B | C | D | |
I | 干燥的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 湿润的有色布条 |
II | 碱石灰 | 无水氯化钙 | 无水氯化钙 | 浓硫酸 |
III | 湿润的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 干燥的有色布条 |
(5)设计装置D、E的目的是比较氯、溴、碘的氧化性。当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为橙色,说明氯气的氧化性比溴单质的______(填“强”“或“弱”)。打开活塞,将装置D中少量溶液加入装置E中,振荡后静置,观察到的现象是___________。
(6)F为尾气吸收装置。实验时,该装置中反应的离子方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于NaHCO3的性质,下列说法正确的是
A. 热稳定性比Na2CO3大
B. 相同温度下溶解度比Na2CO3要大
C. NaHCO3只能和酸作用不能和碱作用
D. 和酸反应放出等量的CO2所消耗的酸比Na2CO3少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。下图所示是硫及其部分化合物的“价类二维图”, 根据图示回答下列问题:

(1)图中A、B、C、D四种物质中,属于非电解质的是__________(用化学式表示)。
(2)足量B通入紫色石蕊溶液的现象是__________________________;
用一个化学方程式说明B具有还原性_____________________________。
(3)C在反应中既可作氧化剂,又可作还原剂。当它作氧化剂时,理论上其可被还原为__________(填标号)。
A.Na2S B.S C.H2SO3 D.Na2SO4 E.H2SO4
(4)将A与SO2混合,可生成淡黄色固体。该反应的氧化剂与还原剂的物质的量之比为_____。
(5)D的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为_________________,反应中D显示酸性和______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化锂是一种优良的贮氢材料,它是一种紫色或红色的晶状固体,在空气中长期暴露,最终会变成碳酸锂。氮化锂易水解生成氢氧化锂和氨气,在空气中加热能剧烈燃烧,特别是细粉末状的氮化锂;锂与氨反应生成LiNH2和H2。实验室用干燥、纯净的N2与金属锂(密度为0.534g·cm3)反应制取氮化锂。某课题组拟选择下列装置完成实验(装置可重复使用):

回答下列问题:
(1)若实验室用生石灰与浓氨水混合制备少量氨气,气流从左至右,选择上述装置制备少量氮化锂。装置连接顺序为__________________________________________。
(2)E装置的作用是_____________________________;写出D中化学方程式为______________________________。
(3)实验步骤如下:①装药品②引发反应产生氨气③检查装置气密性④点燃C处酒精灯⑤点燃D处酒精灯。正确的先后顺序为________________________________。(填序号)
(4)实验室保存锂的方法是______________;写出C中的化学方程式________________________________。氮化锂的电子式为_______________________________________
(5)设计简单实验证明C中产物为氮化锂:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是( )
A. CS2为V形的极性分子
B. ClO3-的空间构型为平面三角形
C. SF6中有6对完全相同的成键电子对
D. SiF4和SO32-的中心原子前者为sp3杂化,后者为sp2杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p轨道的电子数等于次外层的电子总数,B元素可分别与A、C、D、E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7∶8,E与B的质量比为1∶1。根据以上条件,回答下列问题:
(1)画出C的原子结构示意图:________。
(2)写出D原子的外围电子排布式:________。
(3)写出A元素单质在B中完全燃烧的化学方程式:______________。
(4)指出E元素在元素周期表中的位置:____________。
(5)比较A、B、C三种元素的第一电离能的大小顺序:________________(按由大到小的顺序排列,用元素符号表示)。
(6)比较元素D和E的电负性的相对大小:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述错误的是

A. 雾和霾的分散剂相同
B. 雾霾中含有硝酸铵和硫酸铵
C. NH3是形成无机颗粒物的催化剂
D. 雾霾的形成与过度施用氮肥有关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com