
| A.浓硫酸和浓硝酸都不能用来直接跟锌粒反应制氢气 |
| B.浓硫酸和浓硝酸都能与金属铜反应 |
| C.浓硫酸和浓硝酸加水稀释后都能与金属铜反应 |
| D.浓硫酸和浓硝酸在常温下都能用金属铝或铁制容器盛放 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.打雷时也能产生臭氧,臭氧分子是直线型分子 |
| B.臭氧转化为氧气和氧气转化为臭氧均须吸收能量 |
| C.臭氧和氧气的相互转化能保持大气中臭氧的含量基本稳定 |
| D.向大气中排放氮的氧化物和氟氯代烃均能加快臭氧的分解 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Fe2O3 + SO2↑+ SO3↑,若将此反应生成的气体通入BaCl2溶液中,则( )
Fe2O3 + SO2↑+ SO3↑,若将此反应生成的气体通入BaCl2溶液中,则( )| A.析出BaSO3沉淀 | B.析出BaSO4沉淀 | C.逸出SO3气体 | D.逸出SO2气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
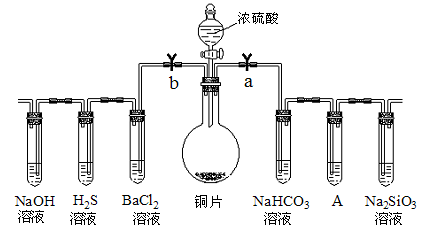

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
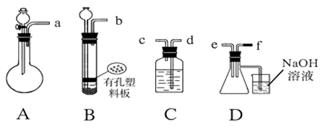
 f各导管口连接起来,正确的顺序有
f各导管口连接起来,正确的顺序有 | A.befcda | B.adcefb | C.acdfeb | D.acdefb |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在蔗糖中加入浓H2SO4后出现发黑现象,说明浓H2SO4具有脱水性 |
| B.浓H2SO4和Cu加热反应,表现浓H2SO4的强氧化性和酸性 |
| C.常温下,浓硫酸可以用铝罐贮存,说明铝与浓H2SO4不反应 |
| D.蓝色硫酸铜晶体加入浓H2SO4后变白,说明浓H2SO4具有吸水性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
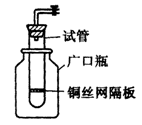

| A.用带火星的细木条靠近干燥管口a,观察细木条是否着火燃烧. |
| B.将C装置中反应后的固体物质溶于适量水配成溶液. |
| C.在配成的溶液中加入用硝酸酸化的硝酸钡溶液,观察是否有沉淀生成. |
| D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2SO3溶液 | B.硫化钠 | C.浓H2SO4 | D.固体氢氧化钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com