
| A�� | ��֪ag��ϩ������ȼ��ʱ����1molCO2��Һ̬ˮ���ų�bkJ�����������ʾ��ϩȼ���ȵ��Ȼ�ѧ����ʽΪ2C2H4��g��+6O2��g���T4CO2��g��+4H2O��l����H=-4b kJ•mol-1 | |
| B�� | ��֪��H2��g��+F2��g���T2HF��g����H=-270kJ•mol-1����1mol������1mol������Ӧ����2molҺ̬������ų���������ֵС��270kJ | |
| C�� | ���³�ѹ�£���0.5molN2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3��g��������19.3kJ�����Ȼ�ѧ����ʽΪN2��g��+3H2��g��?2NH3��g����H=-38.6kJ•mol-1 | |
| D�� | ��֪����C��s��ʯī��+O2��g���TCO2��g����H=-393.5kJ•mol-1����C��s�����ʯ��+O2��g���TCO2��g����H=-395.0kJ•mol-1 ��C��s�����ʯ���TC��s��ʯī����H=-1.5kJ•mol-1 |
���� A����֪��ϩ������ȼ��ʱ����1molCO2��Һ̬ˮ���ų�b k J������������ʽ�ж�����̼Ϊ2mol����ų�������Ϊ2bkJ��������ϩȼ���ȵ��Ȼ�ѧ����ʽΪC2H4��g��+3O2��g��=2CO2��g��+2H2O��l������H=-2b kJ/mol��
B��Һ̬���������������̬������������ͣ����ݷ�Ӧ����������ϵ�жϣ�
C��0.5molN2��1.5molH2�����ܱ������г�ַ�Ӧ����NH3��g��������19.3kJ�����ɵİ��������ʵ���С��1mol����ͬ�����µ�ͬһ���淴Ӧ�����淴Ӧ��Ӧ����ֵ��ȣ������෴��
D�������Ȼ�ѧ����ʽ��˹���ɼ�������жϣ�
��� �⣺A����֪��ϩ������ȼ��ʱ����1molCO2��Һ̬ˮ���ų�b k J������������ʽ�ж�����̼Ϊ2mol����ų�������Ϊ2bkJ��������ϩȼ���ȵ��Ȼ�ѧ����ʽΪC2H4��g��+3O2��g��=2CO2��g��+2H2O��l������H=-2b kJ/mol����A����
B��Һ̬���������������̬������������ͣ����������غ㣬1mol������1mol������Ӧ����2molҺ̬������ų�����������270kJ����B����
C����ͬ�����µ�ͬһ���淴Ӧ�����淴Ӧ��Ӧ����ֵ��ȣ������෴��0.5molN2��1.5molH2�����ܱ������г�ַ�Ӧ����NH3��g��������19.3kJ�����ɵİ��������ʵ���С��1mol������2mol�����ֽ⣬���յ���������38.6kJ����C����
D����C��s��ʯī��+O2��g���TCO2��g����H=-393.5 kJ/mol��
��C��s�����ʯ��+O2��g���TCO2��g����H=-395.0 kJ/mol��
�����ݸ�˹���ɢ�-�ٵõ�C��s�����ʯ���TC��s��ʯī����H=-1.5kJ•mol-1����D��ȷ��
��ѡD��
���� ���⿼�鷴Ӧ�ȣ���Ӧ�ʱ京�����⣬��˹���ɵļ���Ӧ��\���淴Ӧ��ע��Cѡ�������Ӧ���̣�Ϊ�״��㡢�ѵ㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl2ͨ��ˮ�� | B�� | Cl2ͨ��FeCl2��Һ�� | ||
| C�� | NH3ͨ��ˮ�� | D�� | NO2ͨ��ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.0 L 1.0 mo1•L-1��NaAlO2 ˮ��Һ�к��е���ԭ����Ϊ2 NA | |
| B�� | ����NA��ԭ�ӵ������ڱ�״���µ����ԼΪ22.4 L | |
| C�� | ��״���£�2.24 LCl2������ˮ��Ӧת�Ƶĵ�����Ϊ0.2NA | |
| D�� | V L a mol•L-1���Ȼ�����Һ�У���Fe3+����ĿΪNA����Cl-����Ŀ����3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����--Al2��SO4��3•12H2O | B�� | Ư��--NaClO | ||
| C�� | �մ��--NaHCO3 | D�� | ˮú��--CO��H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ħ���ǹ��ʿ�ѧ�罨����õ�һ�������� | |
| B�� | Ħ�������ʵ����ĵ�λ�����Ħ������Ϊmol | |
| C�� | 1mol����Լ��6.02��1023��O2 | |
| D�� | 0.5molH2O���е�ԭ����ĿΪ1.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3 mL | B�� | 7.5 mL | C�� | 15 mL | D�� | 22.5 mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.1 | 11.6 | 10.3 | 11.1 | 11.3 |
| A�� | CO2+H2O+2NaClO�TNa2CO3+2HClO | B�� | CO2+H2O+NaClO�TNaHCO3+HClO | ||
| C�� | CO2+H2O+C6H5ONa-��NaHCO3+C6H5OH | D�� | CH3COOH+NaCN�TCH3COONa+HCN |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
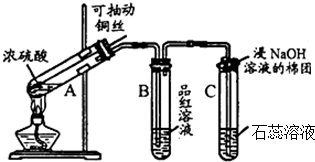
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com