
【题目】工业回收铅蓄电池中的铅,常用Na2CO3或NaHCO3溶液处理铅膏(主要成分PbSO4)获得PbCO3:PbSO4(s) + CO32-(aq) ![]() PbCO3(s) + SO42-(aq) K = 2.2×105。 经处理得到的PbCO3灼烧后获得PbO,PbO再经一步转变为Pb。下列说法正确的是( )
PbCO3(s) + SO42-(aq) K = 2.2×105。 经处理得到的PbCO3灼烧后获得PbO,PbO再经一步转变为Pb。下列说法正确的是( )
A.PbSO4的溶解度小于PbCO3
B.处理PbSO4后,Na2CO3或NaHCO3溶液的pH升高
C.若用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4 , Na2CO3溶液中的PbSO4转化率较大
D.整个过程涉及一个复分解反应和两个氧化还原反应
【答案】C
【解析】A.根据方程式,PbCO3的溶解度小于PbSO4,故A不符合题意;
B. 处理PbSO4后,Na2CO3或NaHCO3溶液转变为硫酸钠溶液,pH降低,故B不符合题意;
C. 若用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4,碳酸氢钠的电离程度较小,碳酸根离子浓度较小,而碳酸钠中碳酸根离子浓度较大,Na2CO3溶液中的PbSO4转化率较大,故C符合题意;
D. 整个过程涉及两个复分解反应:PbSO4(s) + CO32-(aq) ![]() PbCO3(s) + SO42—(aq)和PbCO3灼烧后获得PbO,一个氧化还原反应:PbO转变为Pb,故D不符合题意。
PbCO3(s) + SO42—(aq)和PbCO3灼烧后获得PbO,一个氧化还原反应:PbO转变为Pb,故D不符合题意。
所以答案是:C


科目:高中化学 来源: 题型:
【题目】As2O3在医药、电子等领域有重要应用.某含砷元素(As)的工业废水经如图1流程转化为粗As2O3 . 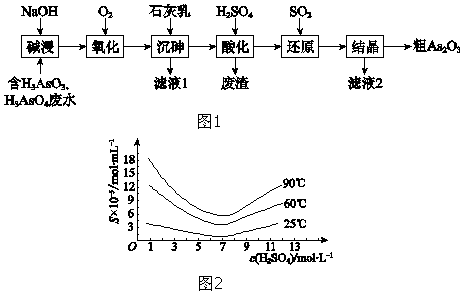
(1)“碱浸”的目的是将废水中的H3AsO3和H3AsO4转化为盐.H3AsO4转化为Na3AsO4反应的化学方程式是 .
(2)“氧化”时,1mol AsO33﹣转化为AsO43﹣至少需要O2mol.
(3)“沉砷”是将砷元素转化为Ca5(AsO4)3OH沉淀,发生的主要反应有: a.Ca(OH)2(s)Ca2+(aq)+2OH﹣(aq)△H<0
b.5Ca2++OH﹣+3AsO43﹣Ca5(AsO4)3OH△H>0
研究表明:“沉砷”的最佳温度是85℃.
用化学平衡原理解释温度高于85℃后,随温度升高沉淀率下降的原因是 .
(4)“还原”过程中H3AsO4转化为H3AsO3 , 反应的化学方程式是 .
(5)“还原”后加热溶液,H3AsO3分解为As2O3 , 同时结晶得到粗As2O3 . As2O3在不同温度和不同浓度硫酸中的溶解度(S)曲线如图2所示.为了提高粗As2O3的沉淀率,“结晶”过程进行的操作是 .
(6)下列说法中,正确的是(填字母). a.粗As2O3中含有CaSO4
b.工业生产中,滤液2可循环使用,提高砷的回收率
c.通过先“沉砷”后“酸化”的顺序,可以达到富集砷元素的目的.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究并回答问题
(1)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
| A | B | C | D | E | F |
4molL﹣1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1= , V6= , V9=;
②反应一段时间后,实验A中的金属呈色,实验E中的金属呈色;
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因 .
(2)在100℃和200kPa的条件下,反应aA(g)bB(g)+cC(g)建立平衡后,在不加入任何物质的条件下逐步增大体系的压强(维持温度不变),下表列出的不同压强下反应建立平衡时物质B的浓度.
压强(kPa) | 200 | 500 | 1 000 |
B的浓度(molL﹣1) | 0.04 | 0.1 | 0.27 |
根据表中的数据,回答下列问题:
①压强从200kPa增加到500kPa时,平衡移动(填“正向”“逆向”或“不”),理由是 .
②压强从500kPa增加到1 000kPa时,平衡转移(填“正向”“逆向”或“不”),其原因可能是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Fe2+、Al3+和Na+。某同学为了确认其成分,取部分试液,设计并完成了如下实验:
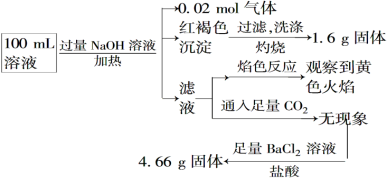
下列说法正确的是
A.原溶液中c(Fe3+)=0.2 mol·L-1
B.要确定原溶液中是否含有Fe2+,其操作为取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有Fe2+
C.SO42-、NH4+、Na+一定存在,CO32-,Al3+一定不存在
D.溶液中至少有4种离子存在,其中Cl-一定存在,且c(Cl-)≥0.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中,由H2和CO直接制备二甲醚(CH3OCH3),其过程包含以下反应:
i.CO(g)+2H2(g) ![]() CH3OH(g) H1=90.1kJ·mol1
CH3OH(g) H1=90.1kJ·mol1
ii.2CH3OH(g) ![]() CH3OCH3(g)+H2O(g) H2=24.5kJ·mol1
CH3OCH3(g)+H2O(g) H2=24.5kJ·mol1
当其他条件相同时,由H2和CO直接制备二甲醚的反应中,CO平衡转化率随条件X 的变化曲线如右图所示。下列说法正确的是( )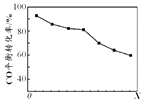
A.由H2和CO直接制备二甲醚的反应为放热反应
B.条件X为压强
C.X增大,二甲醚的产率一定增大
D.X增大,该反应的平衡常数一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年我国科研人员研制出一种室温“可呼吸”NaCO2电池。放电时该电池“吸入”CO2 , 充电时“呼出”CO2。吸入CO2时,其工作原理如右图所示。吸收的全部CO2中,有2/3转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法正确的是:( )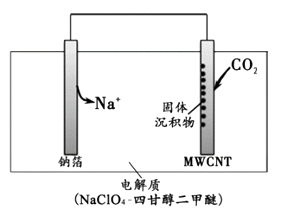
A.“吸入”CO2时,钠箔为正极
B.“呼出”CO2时,Na+向多壁碳纳米管电极移动
C.“吸入”CO2时的正极反应:4Na+ + 3CO2 + 4e-= 2Na2CO3 + C
D.标准状况下,每“呼出”22.4LCO2 , 转移电子数为0.75mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。

请回答下列问题。
(1)B、C、D、E 4种物质的化学式为:
B____________、C____________、D____________、E____________。
(2)沉淀F与NaOH溶液反应的离子方程式为________________________________。
沉淀E与稀硫酸反应的离子方程为____________________________________。
溶液G与过量稀氨水反应的化学方程为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁、铝合金投入100mL一定物质的量浓度盐酸中,合金全部溶解,向所得溶液中滴加4mol /LNaOH溶液至过量,生成沉淀的质量与加入NaOH溶液的体积关系如图(横坐标体积单位是mL,纵坐标质量单位是g),求:
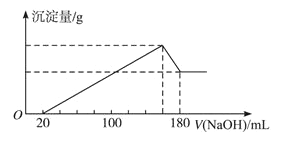
(1)原合金中Mg、Al质量各多少克?_________
(2)盐酸的物质的量浓度c(HCl)=____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能说明SO2具有漂白作用的是
A.SO2气体能使溴水褪色
B.SO2能使酸性高锰酸钾溶液褪色
C.SO2气体能使含NaOH的酚酞溶液褪色
D.SO2气体能使黄色的草帽辫变白色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com