
【题目】某有机物,在标准状况下,其蒸气密度为2.054g/L,则其摩尔质量为_____________,又知4.6克该有机物完全燃烧生成二氧化碳2.24L(标准状况)和1.8克水,则该有机物的分子式为________,该有机物能与乙醇发生酯化反应,则该有机物的结构简式为______________。
【答案】46g/mol CH2O2 HCOOH
【解析】
有机物蒸气的密度为2.054g/L,则相对分子质量为2.054×22.4=46,摩尔质量为46g/mol,计算水、二氧化碳的物质的量可确定有机物分子式,该有机物能与乙醇发生酯化反应,说明含有羧基,以此解答该题。
有机物蒸气的密度为2.054g/L,则相对分子质量为2.054×22.4=46,摩尔质量为46g/mol;
n (CO2) =![]() =0.1mol,n (H2O)=
=0.1mol,n (H2O)=![]() =0.1mol,则有机物含有1个C原子、2个H原子,O原子个数为=
=0.1mol,则有机物含有1个C原子、2个H原子,O原子个数为=![]() =2,则分子式为CH2O2;
=2,则分子式为CH2O2;
该有机物能与乙醇发生酯化反应,应含有羧基,则有机物为HCOOH。


科目:高中化学 来源: 题型:
【题目】常温下,用0.010mol/L的NaOH溶液滴定10.00mL 0.010mol/L的酸H2A,滴定过程中加入NaOH溶液的体积(V)与溶液中lg![]() 的关系如图所示(10mL之后的曲线未画出)。下列叙述正确的是( )
的关系如图所示(10mL之后的曲线未画出)。下列叙述正确的是( )
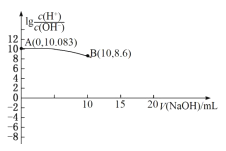
A.H2A![]() H++HA-
H++HA-
B.Ka(HA-)的数量级为10-5
C.滴定过程中,水的电离程度最大的为B点溶液
D.V(NaOH)=15mL时的溶液中:c(Na+)>c(A2-)>c(HA-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照《能源发展“十三五”规划》的要求,到2020年,中国煤炭消费总量控制在41亿吨以内,所占比重应减少到58%。推进煤炭清洁高效利用是我国能源发展重要举措之一。![]() 在催化活性碳(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种的吸附状态。下列有关叙述不正确的是( )
在催化活性碳(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种的吸附状态。下列有关叙述不正确的是( )
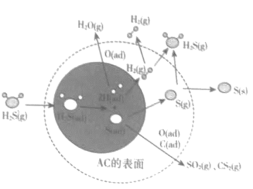
A.图中阴影部分为![]() 的解离过程
的解离过程
B.图中既有O-H键的形成也有O-H键的断裂
C.![]() 在AC表面的去除率与温度有关
在AC表面的去除率与温度有关
D.![]() 在AC表面作用生成的产物有
在AC表面作用生成的产物有![]() 等
等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 是原子序数依次增大的四种短周期主族元素,常见单质分子
是原子序数依次增大的四种短周期主族元素,常见单质分子![]() 中含有3对共用电子对,由
中含有3对共用电子对,由![]() 、
、![]() 形成的一种气态化合物不能稳定地存在于空气中,
形成的一种气态化合物不能稳定地存在于空气中,![]() 、
、![]() 同周期且
同周期且![]() 的最高正价是
的最高正价是![]() 的7倍。下列说法正确的是( )。
的7倍。下列说法正确的是( )。
A.含氧酸的酸性:![]()
B.简单离子半径:![]()
C.最简单氢化物的沸点:![]()
D.![]() 与
与![]() 形成的化合物中只含有离子键
形成的化合物中只含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用乙醇制取乙烯,并验证乙烯的性质。完成下列填空:
(1)实验室制取乙烯的化学方程式为:________________________________________
(2)可用于制取乙烯的发生装置是____________。(选填编号)
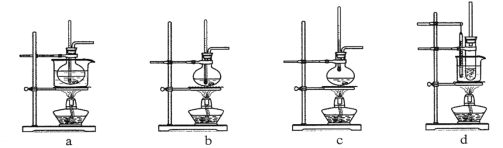
(3)反应液加入碎瓷片的目的是:_______________________。
(4)制得的乙烯中常含有SO2和CO2 ,设计实验证明乙烯能使溴水褪色。(画出装置图)____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取软锰矿石(主要成分为MnO2)116 g跟足量浓盐酸发生如下反应(杂质不参与反应)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,制得22.4 L Cl2(标准状况),下列有关说法中不正确的是
MnCl2+Cl2↑+2H2O,制得22.4 L Cl2(标准状况),下列有关说法中不正确的是
A.这种软锰矿石中MnO2的质量分数为75%
B.被氧化的HCl的物质的量为4 mol
C.参加反应的HCl的质量为146 g
D.被还原的MnO2的物质的量为1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,22.4 L氢气中含有2NA个中子
B. 0.1NA个氯化氢分子占有体积为2.24 L
C. 2克金属钙变成钙离子时失去的电子数为0.1NA
D. 50 mL 0.1 mol·L-1H2SO4溶液中含有H+数为0.005NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车用汽油的抗爆剂约含17%的1,2—二溴乙烷(无色液体,沸点:131℃,熔点:9.3℃)。同学们在实验室拟制备少量1,2—二溴乙烷,流程如图:
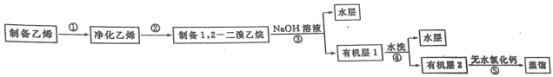
任务I:1,2—二溴乙烷的制备(利用如图装置,完成流程图中步骤①和②)
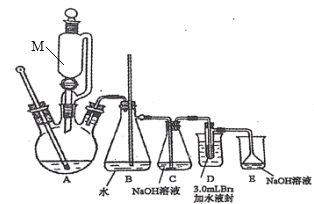
(i)在冰水冷却下,将24 mL浓硫酸注入12 mL乙醇中混合均匀。
(ii)向D装置的试管中加入3.0 mL液溴(0.10 mol),加入适量水液封,并向烧杯中加入冷却剂。
(ⅲ)连接仪器并检查装置的气密性。向三颈烧瓶中加入碎瓷片,通过M向三颈烧瓶中加入部分硫酸与乙醇的混合物,一部分留在M中。
(iv)先切断C、D的连接处,加热三颈烧瓶,待温度上升到120℃,连接C、D,待温度升到180℃~200℃,通过M慢慢滴入混合液。
(v)继续加热三颈烧瓶,待D中试管内的颜色完全褪去,切断C、D的连接,停止加热。
回答问题:
(1)图中仪器M的名称是_______。
(2)图中B装置中玻璃管的作用是_________。
(3)步骤ⅳ中“先切断C、D的连接处,再加热三颈烧瓶”的原因是______。
(4)装置D的烧杯中需加入冷却剂,下列冷却剂合适的为_______。
A. 冰水混合物 B. 5℃的水 C. 10℃的水
任务Ⅱ:1,2—二溴乙烷的纯化(流程图中步骤③④⑤)
步骤③冷却后,把装置D试管内的产物转移至分液漏斗,用1%的NaOH水溶液洗涤。
步骤④:用水洗涤至中性。
步骤⑤:向所得的有机层中加适量无水氯化钙,过滤,转移至蒸馏烧瓶中蒸馏,收集130℃~132℃的馏分,得到产品4.70 g。
(5)步骤③中加入1%的NaOH水溶液时,发生反应的化学方程式为________。
(6)步骤⑤中加入无水氯化钙的作用为_____。该实验所得产品的产率为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸二甲酯[(CH3O)2CO]是一种具有发展前景的“绿色”化工产品。电化学法合成碳酸二甲酯的工作原理如图所示。下列说法错误的是
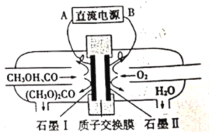
A.石墨I与直流电源正极相连
B.H+由石墨II通过质子交换膜向石墨I移动
C.石墨I上发生的电极反应为2CH3OH+CO-2e-=(CH3O)2CO+2H+
D.电解过程中,阴极和阳极消耗气体的物质的量之比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com