
【题目】根据如下能量关系示意图,下列说法正确的是
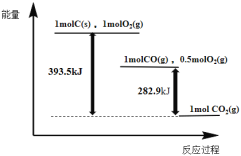
A.1 mol C(s)与1 mol O2(g)的能量之和为393.5 kJ
B.由C→CO的热化学方程式为:2C(s)+O2(g) = 2CO(g) ΔH= 221.2 kJmol1
C.反应2CO(g)+O2(g) =2CO2(g)中,生成物的总能量大于反应物的总能量
D.将1 mol C(s)磨成粉末后,反应更加剧烈,说明粉碎可以改变ΔH
【答案】B
【解析】
A.据图可知1 mol C(s)与1 mol O2(g)的能量之和比1molCO2(g)的能量多393.5kJ,并不是1 mol C(s)与1 mol O2(g)的能量之和为393.5kJ,故A错误;
B.据图可知:
i:C(s)+O2(g)=CO2(g) ΔH=393.5kJ/mol;
ii:CO(g)+![]() O2(g)=CO2(g) ΔH=282.9kJ/mol;
O2(g)=CO2(g) ΔH=282.9kJ/mol;
由盖斯定律(i- ii)×2可得2C(s)+O2(g)=2CO(g)的ΔH=[393.5kJ/mol(282.9kJ/mol)] ×2=221.2 kJmol1,故B正确;
C.据图可知1molCO(g)和0.5molO2(g)的能量高于1mol CO2(g),即反应物的总能量大于生成物的总能量,故C错误;
D.1 mol C(s)磨成粉末后,反应更加剧烈,但不能改变反应的焓变,故D错误;
故答案为B。


科目:高中化学 来源: 题型:
【题目】氟离子电池是一种前景广阔的新型电池,其能量密度是目前锂电池的十倍以上且不会因为过热而造成安全风险.如图是氟离子电池工作示意图,其中充电时 F-从乙电极流向甲电极,下列关于该电池的说法正确的是
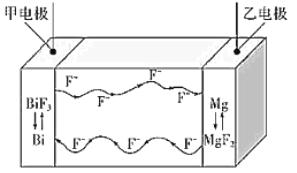
A.放电时,甲电极的电极反应式为 Bi-3e-+3F-=BiF3
B.充电时,导线上每通过1 mol e-,甲电极质量增加 19 g
C.放电时,乙电极电势比甲电极高
D.充电时,外加电源的正极与乙电极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加德罗常数的值,下列说法正确的是
A. 16.25gFeCl3水解形成的Fe(OH)3胶体粒子数为0.1NA
B. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
C. pH=1的H3PO4溶液中,含有0.1NA个H+
D. 10 g的D2O中含有的质子数与中子数分别为5NA和4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向铜片中加入某浓度的硫酸120ml,在加热条件下反应,待铜片全部溶解后,将其溶液稀释到500ml。再加入足量锌粉,使之充分反应,收集到标准状况下氢气2.24L,过滤残留固体,干燥后称量,质量减轻了7.50g。求:
(1)溶解的铜的质量。______
(2)原硫酸的物质的量浓度。(要求写出简要计算过程)_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混合酸,加入反应器中。
②向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀。
③在50~60℃下发生反应,直至反应结束。
④除去混合酸后,粗产品依次用H2O和5%NaOH溶液洗涤,最后再用H2O洗涤。
⑤将污水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
(1)配制一定比例浓硫酸与浓硝酸混合酸时,操作注意事项是_____________________________________。
(2)步骤③中,为了使反应在50~60℃下进行,可采用的方法是________________________________。
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是____________________;步骤④中粗产品用5%NaOH溶液洗涤的目的是__________________________________________________。
(4)实验室制备常用改进装置进行苯和溴的取代反应。如实验装置图,其中A为由具有支管的试管制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑粉。
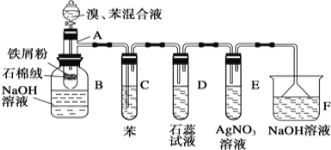
向反应容器A中逐滴加入溴和苯的混合液,几秒中内就发生反应。写出A中所发生反应的化学方程式:_________________________________________________。
(5)试管C中苯的作用是_________________________。反应开始后,观察D和E两试管,看到的现象为___________________________________,________________________________。
(6)反应2~3min后,在B中的NaOH溶液里可观察到的现象是_______________________________。
(7)同学甲认为,在上述整套装置中D和E两试管中的导管应插入液面下,实验现象更明显,请评价同学甲的改进建议:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于测定1mol氢气体积的操作中错误的是( )
A. 镁带称量后,用砂皮擦去表面的氧化层B. 保证装置不漏气
C. 用针筒注入硫酸后,拔出速度要快D. 镁带的质量要使产生的氢气足以计量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲醇(CH3OH)制备一些高附加值产品,是目前研究的热点。
(1)甲醇和水蒸气经催化重整可制得氢气,反应主要过程如下:
反应Ⅰ. CH3OH(g)+H2O(g)![]() 3H2(g)+CO2(g) △H1
3H2(g)+CO2(g) △H1
反应Ⅱ. H2(g)+CO2(g)![]() H2O(g)+CO(g) △H2= a kJ·mol-1
H2O(g)+CO(g) △H2= a kJ·mol-1
反应Ⅲ. CH3OH(g)![]() 2H2(g)+CO(g) △H3= b kJ·mol-1
2H2(g)+CO(g) △H3= b kJ·mol-1
反应Ⅳ. 2CH3OH(g)![]() 2H2O(g)+C2H4(g) △H4= c kJ·mol-1
2H2O(g)+C2H4(g) △H4= c kJ·mol-1
①△H1=______kJ·mol-1 。
②工业上采用CaO吸附增强制氢的方法,可以有效提高反应Ⅰ氢气的产率,如图1,请分析加入CaO提高氢气产率的原因:______。
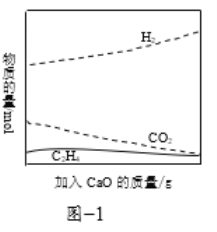
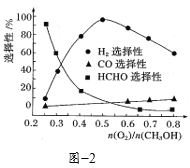
③在一定条件下用氧气催化氧化甲醇制氢气,原料气中![]() 对反应的选择性影响如题图2所示(选择性越大表示生成的该物质越多)。制备H2时最好控制
对反应的选择性影响如题图2所示(选择性越大表示生成的该物质越多)。制备H2时最好控制![]() =______,当
=______,当![]() = 0.25时,CH3OH和O2发生的主要反应方程式为______。
= 0.25时,CH3OH和O2发生的主要反应方程式为______。
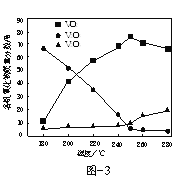
(2)以V2O5为原料,采用微波辅热-甲醇还原法可制备VO2,在微波功率1000kW下,取相同质量的反应物放入反应釜中,改变反应温度,保持反应时间为90min,反应温度对各钒氧化物质量分数的影响曲线如图3所示,温度高于250℃时,VO2的质量分数下降的原因是______。
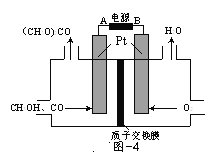
(3)以甲醇为原料,可以通过电化学方法合成碳酸二甲酯[(CH3O)2CO],工作原理如图4所示。
①电源的负极为______(填“A”或“B”)。
②阳极的电极反应式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe3O4中含有Fe(Ⅱ)、Fe(Ⅲ),以Fe3O4/Pd为催化材料,可实现用H2消除酸性废水中的致癌物NO2-,其反应过程如图所示。下列说法正确的是( )
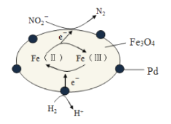
A.Pd作正极
B.Fe(Ⅱ)与Fe(Ⅲ)的相互转化起到了传递电子的作用
C.反应过程中NO2-被Fe(Ⅱ)氧化为N2
D.用该法处理后水体的pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列有关说法正确的是
A.60克的乙酸和葡萄糖混合物充分燃烧消耗O2分子数为2NA
B.5.8g熟石膏(2CaSO4·H2O)含有的结晶水分子数为0.04NA
C.把4.6g乙醇完全氧化变成乙醛,转移电子数为0.1NA
D.实验室制取氧气方法有多种,制取1molO2转移电子数均是4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com