
【题目】除去下列物质中的杂质,所用试剂和方法不正确的是( )
物质 | 杂质 | 除杂质所用试剂和方法 | |
A | KCl溶液 | I2 | CCl4 , 萃取分液 |
B | CO2 | HCl | 饱和NaHCO3溶液,洗气 |
C | Mg粉 | Al粉 | NaOH溶液,过滤 |
D | CaCO3 | CaO | 盐酸,过滤 |
A.A
B.B
C.C
D.D
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
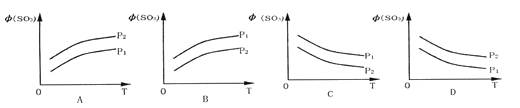
【题目】如图所示,反应2SO2(g)+O2(g)![]() 2SO3(g);△H<0,在不同温度、不同压强(P1>P2) 下达到平衡时,混合气中SO3的体积
2SO3(g);△H<0,在不同温度、不同压强(P1>P2) 下达到平衡时,混合气中SO3的体积![]() (SO3)随温度变化的曲线应为 ( )
(SO3)随温度变化的曲线应为 ( )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铜的制备实验是化学实验教学中一个必做实验,某学习小组设计了如下两个实验方案:
实验一:
因铜不能与稀硫酸反应,实验中用铜和浓硫酸加热使之完全反应,将溶液通过蒸发、结晶等操作得到硫酸铜晶体。
(1)根据上述实验和反应,比较浓硫酸与稀硫酸的性质,浓硫酸具有 。
(2)该反应的化学方程式为 。
实验二:
以空气为氧化剂的一步氧化法,将空气或氧气直接通入到铜粉与稀硫酸的混合物中,其反应原理为2Cu + O2 + 2H2SO4 = 2CuSO4 + 2H2O ,但反应速率太慢,当升高温度到80~90℃,反应仍然缓慢。如在铜粉和稀硫酸的混合物中加入少量Fe2(SO4)3溶液,则速率明显加快。
(3)Fe2(SO4)3的作用是 。
(4)得到的混合液可以用下列四种物质中的 调节溶液的pH =2~4,使Fe3+ 形成Fe(OH)3沉淀而除去:
A.NaOH B. CuO C. CuCO3 D.Fe
(5)请根据以上内容,对这两个实验方案进行评价,填下表:
实 验 (一) | 实 验 (二) | |
主要优点 | 操作简便 | (1)原料充分转化为产品 (2)没有有害气体排放 |
主要缺点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是( )
A. 由水溶液的酸性:HCl>HF,不能推断出元素的非金属性:Cl>F
B. 人们可以在周期表的过渡元素中寻找催化剂和耐腐蚀、耐高温的合金材料
C. 短周期元素正化合价数值和其族序数相同
D. 短周期元素形成的微粒X2-和Y2+核外电子排布相同,离子半径:X2->Y2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用价层电子对互斥理论预测H2S和BF3的空间构型,下列结论中正确的是( )
A. 直线形;三角锥形 B. V形;三角锥形
C. 正四面体;正四面体 D. V形;平面三角形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上曾经通过反应“3Fe+4NaOH![]() Fe3O4+2H2↑+4Na↑”生产金属钠。下列有关说法正确的是
Fe3O4+2H2↑+4Na↑”生产金属钠。下列有关说法正确的是
A. 不能用磁铁将Fe与Fe3O4分离
B. 将生成的气体在空气中冷却可获得钠
C. 该反应条件下铁的氧化性比钠强
D. 该反应中每生成2 mol H2,转移的电子数约为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时:
①HF(aq)+OH-(aq)=F-(aq)+H2O(l)ΔH1=-67.7kJ·mol-1
②H+(aq)+OH-(aq)=H2O(l)ΔH2=-57.3kJ·mol-1
③Ba2+(aq)+SO42—(aq)=BaSO4(s)ΔH3<0
下列说法正确的是( )
A. HF的电离方程式及热效应:HF(aq)![]() H+(aq)+F-(aq) ΔH>0
H+(aq)+F-(aq) ΔH>0
B. 在氢氧化钠溶液与盐酸的反应中,氢氧化钠溶液量越多,中和热越大
C. ΔH2=-57.3 kJ·mol-1是强酸和强碱在稀溶液中反应生成可溶盐的中和热
D. 稀硫酸与稀氢氧化钡溶液反应的热化学方程式为H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)ΔH=-114.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计如图所示装置进行实验,以探究苯与液溴发生反应的原理,并分离、提纯反应产物。
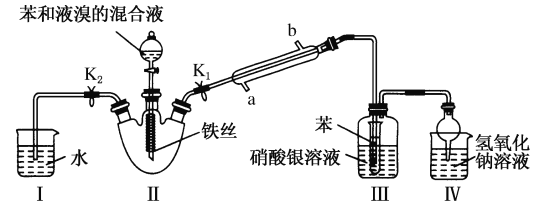
请回答下列问题:
(1)冷凝管所起的作用为________和________,冷凝水从________口进入(填“a”或“b”)。
(2)实验开始时,关闭K2、开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。装置Ⅲ中小试管内苯的作用是____________________________。
(3)能说明苯与液溴发生了取代反应的现象是_____________________。
(4)反应结束后,将装置I中的水倒吸入装置Ⅱ中。这样操作的目的是_______________________,
简述这一步骤的操作:_____________________________________。
(5)利用三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。
①用蒸馏水洗涤,振荡,分液 ②用5% NaOH溶液洗涤,振荡,分液 ③用蒸馏水洗涤,振荡,分液 ④加入无水CaCl2粉末干燥 ⑤________(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B. 25℃,1.01×105Pa,64gSO2中含有的原子数为3NA
C. 在常温常压下,11.2L Cl2含有的分子数为0.5NA
D. 标准状况下,11.2LH2O含有的分子数为0.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com