
·ÖĪö ¢Ła£®ĘĻĢŃĢĒŹĒµ„ĢĒ£¬²»ÄÜĖ®½ā£»
b£®µ°°×ÖŹĖ®½ā×īÖÕµĆµ½°±»łĖį£¬°±»łĖį²»ÄÜĖ®½ā£»
c£®ÓĶÖ¬ŹĒøß¼¶Ö¬·¾ĖįøŹÓĶõ„£»
¢Ś¼¦Ń¼ÓćČāÖŠø»ŗ¬µ°°×ÖŹ£¬µķ·ŪµÄ»ÆѧŹ½ĪŖ£ØC6H10O5£©n£¬Ī¬ÉśĖŲCÓÉC”¢H”¢OČżÖÖŌŖĖŲ¹¹³É£»
¢Ū°×É°ĢĒ”¢¾«ÖĘŃĪŹĒµ÷Ī¶¼Į£¬ÄūĆŹ»ĘŹĒ×ÅÉ«¼Į£¬±½¼×ĖįÄĘŹĒ·ĄøƼĮ£»
¢ÜĪøŹęĘ½ÓėĪøĖį·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖAl£ØOH£©3+3H+ØTAl3++3H2O£®
½ā“š ½ā£ŗ¢Ła£®ĘĻĢŃĢĒŹĒµ„ĢĒ£¬²»ÄÜĖ®½ā£»
b£®µ°°×ÖŹĖ®½ā×īÖÕµĆµ½°±»łĖį£¬°±»łĖį²»ÄÜĖ®½ā£»
c£®ÓĶÖ¬ŹĒøß¼¶Ö¬·¾ĖįøŹÓĶõ„£¬æÉĖ®½āµĆµ½øŹÓĶŗĶøß¼¶Ö¬·¾Ėį£»
¹Ź“š°øĪŖ£ŗc£»
¢Ś¼¦Ń¼ÓćČāŹĒ³£¼ūŹ³²Ä£¬ĖüĆĒø»ŗ¬µÄÓŖŃųĪļÖŹŹĒÓĶÖ¬ŗĶµ°°×ÖŹ£¬ø»ŗ¬µķ·ŪµÄĆęµćĄĻÉŁ½ŌŅĖ£¬µķ·ŪµÄ»ÆѧŹ½ŹĒ£ØC6H10O5£©n£¬Źß²ĖŗĶĖ®¹ūø»ŗ¬Ī¬ÉśĖŲC£¬×é³ÉĪ¬ÉśĖŲCµÄŌŖĖŲŹĒÓÉC”¢H”¢OČżÖÖŌŖĖŲ¹¹³É£¬
¹Ź“š°øĪŖ£ŗµ°°×ÖŹ£»£ØC6H10O5£©n£»C”¢H”¢O£»
¢ŪÄ³Ę·ÅĘ³ČÖÖŠŗ¬ÓŠ°×É°ĢĒ”¢¾«ÖĘŃĪ”¢ÄūĆŹ»ĘŗĶ±½¼×ĖįÄĘ£¬ĘäÖŠ°×É°ĢĒ”¢¾«ÖĘŃĪŹĒµ÷Ī¶¼Į£¬ÄūĆŹ»ĘŹĒ×ÅÉ«¼Į£¬±½¼×ĖįÄĘŹĒ·ĄøƼĮ£¬
¹Ź“š°øĪŖ£ŗÄūĆŹ»Ę£»
¢ÜĪøŹęĘ½[Ö÷ŅŖ³É·ÖĪŖAl£ØOH£©3]Ņ²ŹĒŅ»ÖÖÖĪĮĘĪøĖį¹ż¶ąµÄŅ©£¬ĪøŹęĘ½ÓėĪøĖį·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖAl£ØOH£©3+3H+ØTAl3++3H2O£¬
¹Ź“š°øĪŖ£ŗAl£ØOH£©3+3H+ØTAl3++3H2O£®
µćĘĄ ±¾Ģāæ¼²éĮĖČĖĢåÖŠµÄ»ł±¾ÓŖŃųĪļÖŹŗĶæ¹ĖįŅ©£¬ÄŃ¶Č²»“ó£¬ÕĘĪÕ»ÆѧÓėÉś»īÖŠµÄ»ł“”ÖŖŹ¶ŹĒøł±¾£¬×¢Ņā»ł“”ÖŖŹ¶µÄ»żĄŪ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ę»¹ū·ÅŌŚæÕĘųÖŠ¾ĆÖƱä»ĘŗĶÖ½ÕžĆÖƱä»ĘŌĄķĻąĖĘ | |
| B£® | øßĪĀ»ņČÕ³£ÓƵÄĻū¶¾¼ĮæÉŹ¹ĒŻĮ÷øŠ²”¶¾µ°°×ÖŹ±äŠŌ | |
| C£® | øÖĢśÖĘĘ·ŗĶĶÖĘĘ·¼ČÄÜ·¢ÉśĪüŃõøÆŹ“ÓÖÄÜ·¢ÉśĪöĒāøÆŹ“ | |
| D£® | ĪóŹ³ÖŲ½šŹōŃĪŅżĘšČĖĢåÖŠ¶¾£¬æÉŗČ“óĮæµÄŹ³ŃĪĖ®½ā¶¾ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO42- | B£® | OH- | C£® | Ag+ | D£® | Mg2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹čĖįÄĘæÉÓĆ×÷ľ²Ä·Ą»šĶæĮĻ | B£® | Fe2O3æÉÓĆ×÷ĶāĒ½ĶæĮĻ | ||
| C£® | ¹żŃõ»ÆÄĘæÉÓĆ×÷Ē±Ķ§¹©Ńõ¼Į | D£® | ĀĮÖĘČŻĘ÷æÉŅŌÖüŌĖĻ”ĻõĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
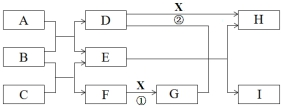
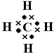 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
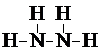 £®
£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÕōĮó | B£® | ·ÖŅŗ | C£® | ÖŲ½į¾§ | D£® | ¹żĀĖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com