
小明为验证NO2的氧化性和NO的还原性,设计了如下装置制取NO2和NO,并验证其性质,装置图如下:
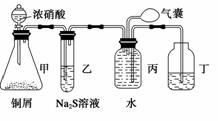
(1)写出甲中反应的离子方程式:______________________________________________
________________,乙中的现象是__________________________________________,
可证明NO2的氧化性;在丙中鼓入空气后现象是_______________________________
________________________________________________________________________,可证明NO的还原性。
(2)实验前丙中充满水的作用是_______________________________________________
________________________________________________________________________
(用反应方程式和简要文字回答)。
(3)小华对小明的实验设计提出了质疑,他认为乙中的现象不足以证明NO2的氧化性,他的理由是_________________________________________________________________
________________________________________________________________________。
你认为怎样才能准确证明NO2的氧化性?(简要回答出原理和现象即可)____________
____________________________________________________________。
科目:高中化学 来源: 题型:
某微粒的结构示意图为 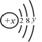 , 试回答:
, 试回答:
(1)当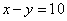 时,该微粒为 (填“原子”、“阳离子”或“阴离子”)。
时,该微粒为 (填“原子”、“阳离子”或“阴离子”)。
(2)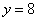 时,某中性原子对应的单质分子式为 。
时,某中性原子对应的单质分子式为 。
(3)写出金属铜与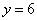 的中性原子的元素最高价氧化物对应水化物浓溶液发生反应的化学方程式 。
的中性原子的元素最高价氧化物对应水化物浓溶液发生反应的化学方程式 。
(4)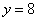 的负一价离子电子式为 ,用电子式表示该元素与氢组成化合物的形成过程 。
的负一价离子电子式为 ,用电子式表示该元素与氢组成化合物的形成过程 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)____HCl(浓)+____MnO2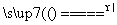 ____Cl2↑+____MnCl2+____H2O
____Cl2↑+____MnCl2+____H2O
(2)____Cu+____HNO3(稀)===____Cu(NO3)2+____NO↑+____H2O
(3)____KI+____KIO3+____H2SO4===____I2+____K2SO4+____H2O
(4)____MnO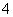 +____H++____Cl-===____Mn2++____Cl2↑+____H2O
+____H++____Cl-===____Mn2++____Cl2↑+____H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
(2013·新课标全国卷Ⅱ,27)氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌[含有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ)等杂质]的流程如下:
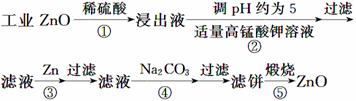
提示:在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是MnO2。
回答下列问题:
(1)反应②中除掉的杂质离子是__________,发生反应的离子方程式为__________;在加高锰酸钾溶液前,若pH较低,对除杂的影响是________________。
(2)反应③的反应类型为____________,过滤得到的滤渣中,除了过量的锌外还有______________。
(3)反应④形成的沉淀要用水洗,检验沉淀是否洗涤干净的方法是________________。
(4)反应④中产物的成分可能是ZnCO3·xZn(OH)2,取干燥后的滤饼11.2 g,煅烧后可得到产品8.1 g,则x等于__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
0.02 mol KMnO4固体加热一段时间后,收集到a mol甲气体,在反应后的残留固体中加入足量的浓盐酸,继续加热,又收集到b mol乙气体,设此时Mn元素全部以Mn2+存在于溶液中,则下列说法正确的是 ( )
A.甲、乙均为无色无味的气体
B.a的最大值为0.02
C.b的最小值为0.01
D.a+b的 最小值为0.04
最小值为0.04
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与化学反应能量变化相关的叙述正确的是
A.生成物总能量一定低于反应物总能量
B.放热反应的反应速率总是大于吸热反应的反应速率
C.同温同压下,H2(g)+Cl2(g) 2HCl(g)在光照和点燃条件下的△H不同
D.应用盖斯定律,可计算某些难以直接测量的反应焓变
查看答案和解析>>
科目:高中化学 来源: 题型:
在钢铁腐蚀过程中,下列五种变化可能发生的是
①Fe2+转化为Fe3+ ②O2被还原 ③产生H2 ④Fe(OH)3失水形成Fe2O3·H2O ⑤杂质碳被氧化
A.只有①和② B.只有②③④ C.①②③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
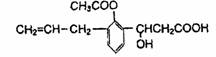
有机物的结构简式如下图:则此有机物可发生的反应类型有:
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和
A.①②③⑤⑥ B.②③④⑤⑥
C.①②③④⑤⑥⑦ D.②③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(1) 在这些元素中,化学性质最不活泼的是_____________ (填具体元素符号,下同)。
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______,碱性最强的化合物的化学式是_____________。
(3) 最高价氧化物是两性氧化物的元素是_____________;写出它的氧化物与氢氧化钠反应的离子方程式____________________________________________。
(4) 元素④与⑥形成的化合物属于__________________(填 “共价”或“离子”)化合物。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com