
美国海军海底战事中心与麻省理工大学共同研制成功了用于潜航器的镁-过氧化氢燃料电池系统。其工作原理如图所示。以下说法中 错误的是( )
错误的是( )

A.电池的负极反应为:Mg-2e-====Mg2+
B.电池工作时,H+向负极移动
C.电池工作一段时间后,溶液的pH增大
D.电池总反应式是:Mg+H2O2+2H+====Mg2++2H2O
科目:高中化学 来源: 题型:
下列关于铜电极的叙述不正确的是( )
A.在镀件上镀铜时镀件作阴极
B.在镀件上镀铜时可用金属铜作阳极
C.用电解法精炼粗铜时粗铜作阳极
D.用电解法精炼粗铜时纯铜作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,0.1 mol·L-1某一元酸HA)溶液中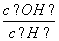 =1.0×10-8。下列叙述正确的是 )。
=1.0×10-8。下列叙述正确的是 )。
A.该溶液中由水电离出的cH+)=1.0×10-3mol·L-1
B.常温下HA的电离平衡常数为1.0×10-6
C.向该HA溶液加水稀释的过程中,cH+)逐渐增大
D.pH=3的HA溶液与pH=11的NaOH溶液等体积混合后,cA-)>cNa+)>cH+)>cOH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,对于反应N2(g)+3H2(g)2NH3(g) ΔH=-92.4 kJ·mol-1。N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是( )
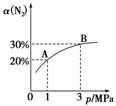
A.将1 mol N2、3 mol H2置于1 L密闭容器中发生反应,放出的热量为92.4 kJ
B.平衡状态由A变到B时,平衡常数K(A)<K(B)
C.上述反应在达到平衡后,增大压强(减小体积),H2的转化率增大
D.升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列四组原电池放电后,电解质溶液质量增加,且在正极上有单质生成的是( )
A.Cu、Ag、AgNO3溶液  B.Zn、Cu、稀硫酸
B.Zn、Cu、稀硫酸
C.Fe、Zn、CuSO4溶液 D.Fe、C、Fe2(SO4)3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
加碘食盐中的碘以碘酸钾 (KIO3)的形式存在。已知溶液中的IO3-和I-发生反应:IO
(KIO3)的形式存在。已知溶液中的IO3-和I-发生反应:IO 3-+5I-+6H+====3I2+3H2O。根据此反应,可用试纸和一些生活中常用的物质进行实验,证明食盐中存在IO3-,除食盐外可供选用的物质有:
3-+5I-+6H+====3I2+3H2O。根据此反应,可用试纸和一些生活中常用的物质进行实验,证明食盐中存在IO3-,除食盐外可供选用的物质有:
①自来水 ②蓝色石蕊试纸
③KI-淀粉试纸 ④淀粉
⑤白糖 ⑥食醋
⑦白酒
进行上述实验时必须使用的物质是( )
A.①③ B.③⑥
C.②④⑥ D.①②④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列物质中所含的少量杂质的方法正确的是( )
| 物质 | 杂质 | 试剂 | 提纯方法 | |
| A | BaSO4 | BaCO3 | 水 | 溶解、过滤、洗涤 |
| B | CO2 | SO2 | 饱和Na2CO3溶液 | 洗气 |
| C | 乙酸乙酯 | 乙酸 | 稀NaOH溶液 | 混合振荡、静置分液 |
| D | 蛋白质 | 葡萄糖 | 浓(NH4)2SO4溶液 | 盐析、过滤、洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 | |
| A | 稀硫酸 | Na2S | AgNO3与 AgCl的浊液 | Ksp(AgCl)> Ksp(Ag2S) | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可生成白色沉淀 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3 溶液 | 酸性:硝酸>碳酸>硅酸 |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物甲的分子式为C9H18O2,在酸性条件下,甲水解为乙和丙两种有机物,在相同温度和压强下,同质量的乙和丙的蒸气所占的体积相同,则甲可能的结构有(不考虑立体异构)( )
A.8种 B.14种
C.16种 D.18种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com