
����Ŀ��������(V)���仯�������Ź㷺����;����ش���������:
��1��������Һ�е���Ҫ�ۺ�״̬����Һ��pH��ϵ��ͼ1��ʾ��V2O74-��VԪ�صĻ��ϼ���_____����д����Һ��VO3-ת��ΪV2O74-�����ӷ���ʽ:____________��
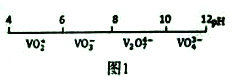
��2�����������γ�������ԭ�����ں��з�Ԫ�ص���Һ�м�����κ��γ�NH4VO3������ͼ2���ڹ�ҵ�����в�ͬpH�����³����ʵIJⶨֵ��ʵ�ʹ�ҵ�����г�ѡ��pH=7.5Ϊ�����������������pH����8.0ʱ�����ʽ��ͣ���ԭ������Һ��VO3-ת��ΪV2O74-��_______��(����д��һ��ԭ��)
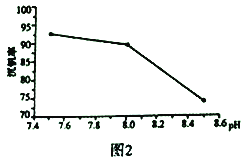
��3��NH4VO3�ڸ����·ֽ������V2O5����Ϊ���Ṥҵ��2SO2(g)+O2(g)![]() 2SO3(g) ��H=p�Ĵ��������ԭ����ͼ3��ʾ��
2SO3(g) ��H=p�Ĵ��������ԭ����ͼ3��ʾ��
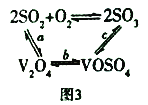
������a����b�Ļ�ѧ����ʽΪ:V2O5(s)+SO2(g)=V2O4(s)+SO3(g)��H=q��
V2O4(s)+O2(g)+2SO2(g)=2VOSO4(g)��H=r
��д������c���Ȼ�ѧ����ʽ:_________________��
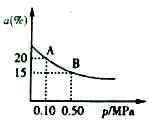
��t2���£���Ӧ:2SO3(g)![]() 2SO2(g)+O2(g)��H>0��SO3��ƽ��ת����(a)����ϵ��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ��t���£���2molSO3����10L�ܱ������У���Ӧ��ƽ�����ϵ��ѹǿΪ0.10MPa��B��Ļ�ѧƽ�ⳣ����ֵ��__________��
2SO2(g)+O2(g)��H>0��SO3��ƽ��ת����(a)����ϵ��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ��t���£���2molSO3����10L�ܱ������У���Ӧ��ƽ�����ϵ��ѹǿΪ0.10MPa��B��Ļ�ѧƽ�ⳣ����ֵ��__________��
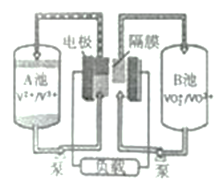
(4)ȫ��ҹ�������һ�ֿɳ���أ�װ����ͼ��ʾ�����ڷŵ��������H+��A������B�أ���:
���ŵ�����У������õ���_______��(����A������B��)��
���������У���������ʽΪ____________��
���𰸡� +5 2 VO3- + 2OH- ![]() V2O74- + H2O pH������Һ�е�NH4+��ת��ΪNH3��H2O 2VOSO4(s)=V2O5(s)+SO3(g)+SO2(g) ��H=p-q-r 0.00125 A�� VO2+ - e- +H2O = VO2+ + 2H+
V2O74- + H2O pH������Һ�е�NH4+��ת��ΪNH3��H2O 2VOSO4(s)=V2O5(s)+SO3(g)+SO2(g) ��H=p-q-r 0.00125 A�� VO2+ - e- +H2O = VO2+ + 2H+
�������������������1�����������л��ϼ۴����͵�������������ɼ���Ԫ�ػ��ϼ�������ͼʾ���ڼ�����Һ��VO3-ת��ΪV2O74-����2����pH����8.0ʱ����Һ��VO3-ת��ΪV2O74-����Һ�е�NH4+��ת��ΪNH3��H2O�����Ե��³����ʽ�������3�������ݸ�˹���ɼ������c���Ȼ�ѧ�����������á�����ʽ������ƽ�ⳣ����(4)�ŵ��������H+��A������B�أ�˵��A�Ǹ���![]() ��B������VO2+ + 2H++ e- = VO2+ +H2O������������������������ӵ�Դ������������������
��B������VO2+ + 2H++ e- = VO2+ +H2O������������������������ӵ�Դ������������������
��������V2O74-��VԪ�صĻ��ϼ���x����2x+(-2) ![]() 7=-4��x=+5������V2O74-��VԪ�صĻ��ϼ���+5������ͼʾ���ڼ�����Һ��VO3-ת��ΪV2O74-��ת�������ӷ���ʽ��2 VO3- + 2OH-
7=-4��x=+5������V2O74-��VԪ�صĻ��ϼ���+5������ͼʾ���ڼ�����Һ��VO3-ת��ΪV2O74-��ת�������ӷ���ʽ��2 VO3- + 2OH- ![]() V2O74- + H2O����2����pH����8.0ʱ����Һ��VO3-ת��ΪV2O74-����Һ�е�NH4+��ת��ΪNH3��H2O�����Ե��³����ʽ�������3����2SO2(g)+O2(g)
V2O74- + H2O����2����pH����8.0ʱ����Һ��VO3-ת��ΪV2O74-����Һ�е�NH4+��ת��ΪNH3��H2O�����Ե��³����ʽ�������3����2SO2(g)+O2(g)![]() 2SO3(g) ��H=p ����V2O5(s)+SO2(g)=V2O4(s)+SO3(g)��H=q����V2O4(s)+O2(g)+2SO2(g)=2VOSO4(g)��H=r�����ݸ�˹��������-��-�۵�2VOSO4(s)=V2O5(s)+SO3(g)+SO2(g) ��H=p-q-r ��
2SO3(g) ��H=p ����V2O5(s)+SO2(g)=V2O4(s)+SO3(g)��H=q����V2O4(s)+O2(g)+2SO2(g)=2VOSO4(g)��H=r�����ݸ�˹��������-��-�۵�2VOSO4(s)=V2O5(s)+SO3(g)+SO2(g) ��H=p-q-r ��
����A���

A���ƽ�ⳣ��![]() ��A��B�¶���ͬ��ƽ�ⳣ����ͬ������B���ƽ�ⳣ����0.00125��(4)���ݷŵ��������H+��A������B�أ�˵��A�Ǹ�����B���������ٷŵ�����У������õ���A�أ��ڳ�������������������ӵ�Դ������������������������ӦΪVO2+ - e- +H2O = VO2+ + 2H+��
��A��B�¶���ͬ��ƽ�ⳣ����ͬ������B���ƽ�ⳣ����0.00125��(4)���ݷŵ��������H+��A������B�أ�˵��A�Ǹ�����B���������ٷŵ�����У������õ���A�أ��ڳ�������������������ӵ�Դ������������������������ӦΪVO2+ - e- +H2O = VO2+ + 2H+��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���绯ѧ���ճ���������;�㷺����ͼ����þ����������ȼ�ϵ�ص�ʾ��ͼ������ܷ�ӦʽΪ��Mg+ClO-+H2O�TCl-+Mg(OH)2����ͼ���ǵ�ⷨ��ȥ��ҵ��ˮ�е�Cr2O72-������˵����ȷ����
A. ͼ����Cr2O72-���������缫�ƶ�����ü�������OH-���ת����Cr��OH��3��ȥ
B. ͼ���������ϵĵ缫��ӦʽΪ��Fe-3e-�TFe3+
C. ͼ���з�����������Ӧ�ǣ�ClO-+H2O+2e-�TCl-+2��OH��-
D. ��ͼ����7.2gþ�ܽ�����ĵ�������ͼ�ڷ�ˮ���������ۿɳ�ȥCr2O72-�����ʵ���Ϊ0.05mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij��84����Һ��ƿ�岿�ֱ�ǩ��ͼ��ʾ���á�84����Һ��ͨ��ϡ�� 100 �������֮�ȣ���ʹ�á���ش��������⣺

��1���á�84����Һ�������ʵ���Ũ��ԼΪ________ mol��L1������������ 2λ��Ч���֣���
��2��ijͬѧȡ 100mL �á�84����Һ����ϡ�ͺ�����������ϡ�ͺ����Һ�� c(Na��)��_______ mol��L1��
��3����ͬѧ���ĸá�84����Һ�����䷽������NaClO�������� 480mL��NaClO��������Ϊ25%������Һ������˵����ȷ����______������ĸ����
A����ͼ��ʾ�������У��������Dz���Ҫ�ģ�����Ҫһ�ֲ�������
B�� �������õ�NaClO�������ձ����ܽ��Ӧ����ת������ƿ����ˮ���̶���
C�� ����ʱ��������ƿ�̶��ᵼ��������ҺŨ��ƫ��
D����Ҫ���� NaClO���������Ϊ 143.0g

��4����ͬѧ������ƿ����ʹ�÷�������ʶ����ȷ����________
A������ƿ�ϱ����ݻ����¶Ⱥ�Ũ��
B������ƿ������ˮϴ���� ��Ҫ��ɺ���ʹ��
C��������Һ�����У�����ƿ��Һ��ֻ��Ҫһ��ҡ�ȹ���
D��ʹ��ǰҪ�������ƿ�Ƿ�©ˮ
��5����84����Һ����ϡ������ʹ�ÿ���ǿ����������ij����С����Ա�� 98%���ܶ�Ϊ1.84g��cm3����Ũ�������� 2L 2.3mol��L1��ϡ����������ǿ��84����Һ��������������
�������Ƶ�ϡ�����У�H�������ʵ���Ũ��Ϊ_______ mol��L1��
������Ũ��������Ϊ_______mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧһ-�л���ѧ����]�ڼ�������£��������������γɦ�һ�ʻ���,ͬʱʧȥһ���Ӵ�,�÷�Ӧ�ƿ���(R��L��Claisen)�����Ϸ�Ӧ,�䷴Ӧ�������£�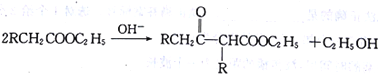 ������Claisen��Ӧ�Ʊ�������H��һ�ֺϳ�·������:
������Claisen��Ӧ�Ʊ�������H��һ�ֺϳ�·������:
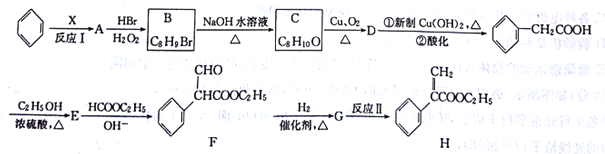
�ش���������:
(1)��Ӧ��ķ�Ӧ����������ʵ��ʽ����ͬ����X�Ľṹ��ʽΪ_____��A������Ϊ____��
(2)F�к��������ŵ�������_______����Ӧ��ķ�Ӧ������________��
(3)E![]() F��Ӧ�Ļ�ѧ����ʽΪ________��
F��Ӧ�Ļ�ѧ����ʽΪ________��
(4)B�ĺ��б�����ͬ���칹����____��(B��������)�����к˴Ź���������ʾ3���Ľṹ��ʽΪ__________��_________��
(5)��������������һ����Ҫ���л��ϳ�ԭ�ϣ�д�����Ҵ��Ʊ��������������ĺϳ�·��___________(���Լ��ν�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪pOH=-lgc(OH)��t��ʱ����50mL0.1mol/LMOH��Һ�μ�0.1mol/L��������ҺpH��pOH�������������ı仯����ͼ��ʾ������˵����ȷ����
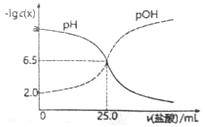
A. a=12
B. ������MOH��Һǡ���к�ʱ��ҺpH=6.5
C. �������������26.0mLʱ,��Һ����Ũ��c(Cl-)>c(H+)>c(M+)>c(MOH)>c(OH-)
D. t��ʱ��MOH��Kb>1.0��10-3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������к��зḻ�ĵ⡣Ϊ�˴Ӻ�������ȡ��,ij�о���ѧϰС����Ʋ�����������ʵ��:

����д���пհ�:
��1�����������պ���ʱ,����Ҫ���ż���,����Ҫ�õ���ʵ��������_________��������������ѡ�����������,�ñ����ĸ��д�հ״�����
A.�ձ�
B.����
C.������
D.������
E.�ƾ���
F.������
��2����������ʵ����������� ;��������Ŀ���ǴӺ���ı���Һ�з�������ʵ�ͻ��ձ�,�ò����ʵ����������� ��
��3����������Ӧ�����ӷ���ʽ�� ��
��4����������,ijѧ��ѡ���ñ�����ȡ��������� ��
��5�������һ�ּ�����ȡ����ˮ��Һ���Ƿ��е��ʵ�ļ���: ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ij��ѧ��ȤС��̽����ͬ�����»�ѧ��ת��Ϊ���ܵ�װ�á������ԭ���ԭ���ش����⣺
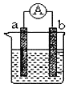
(1)���缫aΪZn���缫bΪCu���������ҺΪϡ���ᣬ��װ�ù���ʱ��SO42��_____��(��a��b)�ƶ��������ĵ缫��ӦʽΪ_______________________________��
(2)���缫aΪMg���缫bΪAl���������ҺΪ����������Һ����ԭ��ع���ʱ�����Ӵ�_____��(��a��b)������һ��ʱ�������Ӧת��3NA�����ӣ�������������Al��������________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʵ���ҿ�����ͼ��ʾװ����ȡ���������������й���������ȷ���ǣ� ��

A. ������������������������
B. ���������û����Һ�з������������
C. Na2CO3������Һ������֮һ������δ��Ӧ������
D. ����ĩ�˲����뱥��Na2CO3��Һ����Ϊ�˷�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��糧�ղ����ķ�ú�ҵ���Ҫ�ɷ�ΪSiO2��Al2O3��FeO��Fe2O3��MgO��TiO2�ȡ��о�С���������ۺϴ������������£�
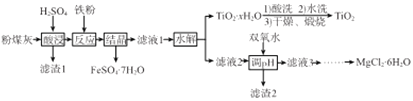
��֪���١������������Ҫ��TiOSO4��ʽ���ڣ�ǿ�����TiOSO4����Һ�н��ܵ���SO42-��һ��������
�������£�Ksp[Al(OH)3]=1.0��10-34��Ksp[Fe(OH)3]=4.0��10-38��Ksp[Mg(OH)2]=1.0��10-11
��ش��������⣺
(1)�������ʱTiO2������Ӧ�����ӷ���ʽΪ_______________��
(2)����Ӧ��ʱ�������۵�����Ϊ_______________��
(3)���ᾧ���������70�����ң��¶ȹ��ᵼ�µĺ��Ϊ_____________��
(4)��ˮ�⡱��Ӧ�����ӷ���ʽΪ______________������TiO2xH2O ����������ϴ��Ŀ��Ϊ____________��
(5)Ϊʹ����2������ȫ(��Һ������Ũ��С��10-5mol/L)���衰��pH����СΪ________��
(6)ʵ������MgCl2��Һ�Ʊ�MgCl26H2O������еIJ���Ϊ_____�����½ᾧ�����ˡ�ϴ�ӡ����
(7)FeSO47H2O��Ʒ���ȵIJⶨ��ȡa g��Ʒ����ˮ���bmL.��Һ�����ữ��cmol/LKMnO4����Һ�ζ����ﵽ�ζ��յ�ʱ���ı�Һ�����ΪdmL����Ʒ��FeSO47H2O����������Ϊ____ ���ô���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com