
| A. | 煤的气化、液化和干馏是物理变化 | |
| B. | 通过石油分馏得到的汽油是纯净物 | |
| C. | 石油裂解是为了得到乙烯、丙烯等气态短链烃 | |
| D. | 干馏的产物能提取出苯、甲苯等芳香烃,因为煤中含有苯和甲苯 |
分析 A.有新物质生成的是化学变化;
B.汽油是多种烃的混合物;
C.石油催化裂化的目的是为了提高汽油等轻质油的产量,而裂解的目的则是为了得到乙烯、丙烯、丁二烯等短链不饱和烃;
D.苯和甲苯是煤在干馏过程中经过复杂的反应生成的.
解答 解:A.煤干馏可以得到煤焦油,煤焦油中含有甲烷、苯和氨等重要化工原料,属于化学变化;煤的气化是将其转化为可燃气体的过程,主要反应为碳与水蒸气反应生成H2、CO等气体的过程,有新物质生成,属于化学变化,故A错误;
B.石油分馏得到的汽油中含有多种饱和烃和不饱和烃,是混合物,故B错误;
C.裂解的目的则是为了得到乙烯、丙烯、丁二烯等短链不饱和烃,故C正确;
D.煤本身不含苯和甲苯,是在干馏过程中经过复杂的反应生成的,故D错误.
故选C.
点评 本题考考查了煤和石油的加工,题目难度不大,注意石油催化裂化和裂解的区别.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 保存浓硝酸时,通常用棕色瓶并放在阴凉处 | |
| B. | 用锌与硫酸反应制取氢气时,适当增大硫酸溶液的浓度 | |
| C. | 合成氨的反应中,选择“铁触媒”作催化剂 | |
| D. | 在试管中进行铝和氢氧化钠溶液反应时,稍微加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的颜色不再改变的状态 | |
| B. | 生成NO、O2的速率之比为2:1 | |
| C. | NO2、NO、O2的物质的量浓度比为2:2:1 | |
| D. | 混合气体的密度不再改变的状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 金刚石比石墨稳定 | B. | 1mol石墨比1mol金刚石的总能量低 | ||
| C. | 石墨比金刚石稳定 | D. | 1mol石墨比1mol金刚石的总能量高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
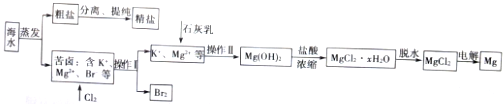
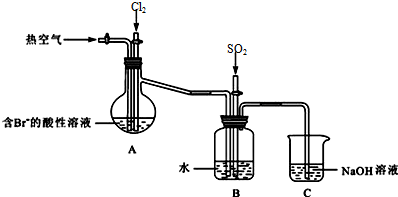
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com