
����Ŀ��ȡ6��������6֧�ɾ����Թܼ��������ϣ���ͼ��ʾ��
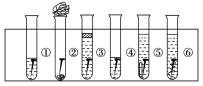
�Թܢٷ���һ����������ע������ˮ��ʹ�����Ϳ�����ˮ�Ӵ���
�Թܢ����Թܵײ�����轺(��һ�ָ����)���ٷ��������������Ŷ�ס�Թܿڣ�ʹ������������Ӵ���
�Թܢ��ȷ���һ�����������ȵ�����е�����ˮ(�Ѹϳ�ԭ���ܽ�������ˮ�еĿ���)��û�������ټ���һ��ֲ���ͣ�ʹ�������ܸ������Ӵ���
�Թܢ��з�������ע��ʳ��ˮ��ʹ�����Ϳ�����ʳ��ˮ�Ӵ���
�Թܢݷ���������������пƬ��ע������ˮ����û������пƬ��
�Թܢ���������������ͭ˿��ע������ˮ����û������ͭ˿��
��6֧�Թܷ����Թܼ��ϣ������۲���������ʴ�������
��1������ʵ�������������˵绯ѧ��ʴ����____(���Թ����)���ڵ绯ѧ��ʴ�У�������Ӧ��____��������Ӧ��______��
��2������������ʴ�������֪����ʹٽ���������ʴ��������_________��
��3��Ϊ��ֹ������ʴ����ҵ���ձ���õķ�����____________(�����ַ���)��
���𰸡��٢ܢ� 2Fe��4e��=2Fe2�� O2��2H2O��4e��=4OH�� ˮ���������������Һ�Ͳ����ý������ʵĴ��� �ڱ���Ϳ�����ᡢ�´ɡ�����Ȼ���ϲ�������ĺϽ����������������������(����������ּ���)
��������
��1�����ݵ绯ѧ��ʴ�������������������绯ѧ��ʴ�У�����������������ʴ��������ʧ���ӷ���������Ӧ�����������õ��ӷ�����ԭ��Ӧ��
��2����ʵ��ó����ۣ�
��3������ӱ�������ߵ绯ѧ�����ĽǶȿ��ǡ�
��1����������ˮ�������Ӵ����γ�ԭ��أ������绯ѧ��ʴ���ڡ��������Թܲ��߱�����ԭ��ص����������ܷ����绯ѧ��ʴ����������ʳ��ˮ�������Ӵ����γ�ԭ��أ������绯ѧ��ʴ���ݾ��ܾ߱�����ԭ��ص���������п�������ã���ԭ�������������ʹ����Ϊ��������δ����ʴ�������Ļ����Դ���ͭ������ԭ��صĸ����������绯ѧ��ʴ�������˵绯ѧ��ʴ���Ǣ٢ܢޣ��ڵ绯ѧ��ʴ�У�������Ӧ��Fe-2e-=Fe2+�����������������õ��ӵĻ�ԭ��ӦO2+2H2O+4e���T4OH�����ʴ�Ϊ���٢ܢޣ�2Fe��4e��=2Fe2����O2��2H2O��4e��=4OH����
��2������������ʴ�������֪����ʹٽ���������ʴ���γ�ԭ��أ�����������������ˮ���������������Һ�Ͳ����ý������ʵĴ��ڣ�
��3������ԭ���ԭ��������ԭ�����ӱ�����ķ������ɷ�ֹ������ʴ����ҵ���ձ���õķ������ڱ���Ϳ�����ᡢ�´ɡ�����Ȼ���ϲ�������ĺϽ�����������������������ȡ�


 ʱ�����������ҵԭ���ܳ�����ϵ�д�
ʱ�����������ҵԭ���ܳ�����ϵ�д� ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ĩ X �п��ܺ��� Fe2O3��CuO��MnO2��CaO��NaCl �� K2CO3 �е������֡�Ϊȷ���ù����ĩ�ijɷ֣�����������ʵ��(�����Լ�������)��

���н�����ȷ���ǣ�
A. �����ĩ��һ���� K2CO3B. X �п��ܴ��� Fe2O3
C. ���� M һ���� AgClD. ���� Y �в�һ������ MnO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�آ�~�������ڱ��е�λ�������ʾ���Իش��������⡣
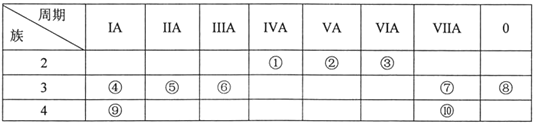
��1������10��Ԫ���У���ѧ��������õ���___(��Ԫ�ط��ţ���ͬ)����ˮ��Ӧ��ҵĽ���Ԫ����___��
��2��Ԫ�آ����������Ľṹʽ��___��Ԫ�آڵļ���̬�⻯��ĵ���ʽ��___������10��Ԫ���У�������������Ӧˮ�����������ǿ��������___(�ѧʽ)��
��3���٢ڢ�Ԫ�ص�ԭ�Ӱ뾶��С�����˳��Ϊ___(��Ԫ�ط��ű�ʾ)��
��4������һ����ѧ����ʽ(�����ӷ���ʽ)˵��Ԫ�آߺ͢�ǽ����Ե�ǿ����___��
��5���ܺ͢���Ԫ�ص�����������Ӧ��ˮ�������Ӧ�����ӷ���ʽ��___��
��6��Ϊ��֤���ݺ͢�����Ԫ�صĽ�����ǿ��������˵����ʵ�����ṩ֤�ݵ���___��
A.�Ƚ�����Ԫ�صĵ��ʵ��۵㡢�е�ߵ�
B.����ĥ������״����С��ͬ������Ԫ�صĵ��ʷֱ����ˮ���ã��������̪��Һ
C.�Ƚ�����Ԫ�ص�����������Ӧ��ˮ�������ǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�Һϳɳ���һ���»������ͼ��ʾ��������W��X��Y��ZΪͬһ������Ԫ�أ�X��Y��ԭ��ϵ��С1��Z����������������X�����������һ�롣����������ȷ����

A.Yԭ�����γ��ĺ�18���ӵĵ����Է���
B.Ԫ�طǽ����Ե�˳��ΪX>Y>Z
C.W�ĵ�����������Ӧ���ܲ��������ۼ��Ļ�����
D.���»�������Y�����������8�����ȶ��ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25�棬101kPaʱ��ǿ����ǿ���ϡ��Һ�����кͷ�Ӧ���к���Ϊ57.3kJ/mol�������ȼ����Ϊ5518kJ/mol�������Ȼ�ѧ����ʽ��д��ȷ���ǣ� ��
A. 2H��(aq)��SO42-(aq)��Ba2��(aq)��2OH��(aq)=BaSO4(s)��2H2O(l) ��H����57.3kJ/mol
B. KOH(aq)��![]() H2SO4(aq)=
H2SO4(aq)=![]() K2SO4(aq)��H2O(l) ��H����57.3kJ/mol
K2SO4(aq)��H2O(l) ��H����57.3kJ/mol
C. C8H18(l)��![]() O2(g)=8CO2(g)��9H2O(g) ��H����5518kJ/mol
O2(g)=8CO2(g)��9H2O(g) ��H����5518kJ/mol
D. 2C8H18(g)��25O2(g)=16CO2(g)��18H2O(1) ��H����5518kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������������������Ҫ�����á���ش��������⣺
(1)����������H2N2O2��һ�ֶ�Ԫ���ᣬ��ˮ��Һ�л����ֽ⣬��ֽ�ԭ����̼��ֽ�ԭ�����ƣ���д������������ֽ�Ļ�ѧ����ʽ_________________________��
(2)��һϡ�����ϡ����Ļ���ᣬ����H2SO4��HNO3�����ʵ���Ũ�ȷֱ���3 mol��L��1��1 mol��L��1��ȡ100 mL�˻���ᣬ�����м�����������ۣ�����Ӧ�����ɲ�����״���µ���������Ϊ____________ (�跴Ӧ��HNO3����ԭ��NO)��
(3)����ͭ��һ����Ũ���ᷴӦ�õ�����ͭ��Һ��NO2��N2O4��NO�Ļ�����壬��Щ������1.5 molO2��Ϻ�ͨ��ˮ�У�����������ȫ��ˮ�����������ᣬ������������ͭ��Һ�м���NaOH��Һ��Cu2+ǡ����ȫ��������������Һ��NaOH�����ʵ���Ϊ____________mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�0.2 mol��L��1��һԪ��HA���Ũ��NaOH��Һ�������Ϻ�������Һ�в�������ּ�Ũ����ͼ��ʾ������˵����ȷ����(����)

A. HAΪǿ��
B. �û����ҺpH��7.0
C. �û����Һ�У�c(A��)��c(Y)��c(Na��)
D. ͼ��X��ʾHA��Y��ʾOH����Z��ʾH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��1 mol O2(g)�еĻ�ѧ����Ҫ����498 kJ�����������������仯ʾ��ͼ������˵������ȷ����
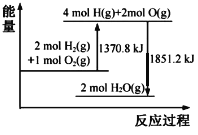
A.2H2(g)��O2(g)��2H2O(l) ��H����480.4 kJ��mol��1
B.H2O(g)��H2(g)��![]() O2(g) ��H��240.2 kJ��mol��1
O2(g) ��H��240.2 kJ��mol��1
C.��1 mol H2(g)�еĻ�ѧ����Ҫ����436.4 kJ������
D.H2(g)��O2(g)�γ�H2O(g)�е�1 mol H��O���ų�462.8 kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��һ��������ij����H2�����ʵ���֮��1:2�ӳ�����C2H5CH (CH3)2��������Ľṹ��ʽΪ(��д1��)______________________��
��2������ʽΪC4H8�������˴Ź�������ͼ�����������շ壬�������Ϊ3:1����д������������2�����ʵĽṹ��ʽ___________________��_____________________��
��3���л���Ľṹ��ʽ���£�����ͨ����ͬ�Ļ�ѧ��Ӧ�ֱ��Ƶýṹ��ʽΪ�ҡ��������ʡ�

��ش��������⣺
���ڼס������������У���Ϊͬ���칹�����_________________�����ţ���ͬ�����ɿ����������___________________��
��д���ɼ����ɸ߷��ӻ�����ķ���ʽ��_______________________________________
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com