
关于室温下下列溶液的说法不正确的是

A.水的电离程度:①=②=③=④
B.分别加水稀释10倍,溶液的pH:①>②>③>④
C.①、③两溶液等体积混合:
D.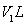 溶液②与
溶液②与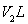 溶液③混合,若
溶液③混合,若 ,则混合溶液pH=4(忽略溶液体积变化)
,则混合溶液pH=4(忽略溶液体积变化)
C
【解析】
试题分析:A、氨水、NaOH溶液的pH为11,则OH?浓度为10-3mol?L?1,pH=3的盐酸和醋酸溶液中H+浓度为10-3mol?L?1,对水的电离影响相同,正确;B、加水稀释,弱电解质的电离平衡向右移动,所以溶液的pH:①>②>③>④,正确;C、①、③两溶液等体积混合,氨水大量过量,溶液溶质为NH3?H2O和NH4Cl,溶液显碱性,离子浓度大小顺序为:c(NH4+) > c(Cl?)>c(OH?)>c(H+),错误;D、HCl过量,混合溶液c(H+)=(V2?10-3mol—V1?10-3mol)/( V1+ V2)= 10-4mol?L?1,所以pH=4,正确。
考点:本题考查酸碱中和反应、离子浓度比较、水的电离、pH的计算。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、相同浓度的氨水和NaOH溶液,能分别与相同浓度的盐酸恰好中和 | B、加水稀释0.10mol?L?1的氨水,溶液中n(OH-)减小 | C、若温度不变,在氨水中加入少量NH4Cl固体,NH3?H2O的电离平衡常数变小 | D、氨水中的离子浓度关系满足:c(OH-)=c(H+)+c(NH+4) |
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com