
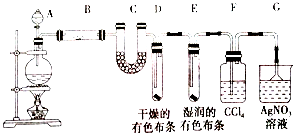
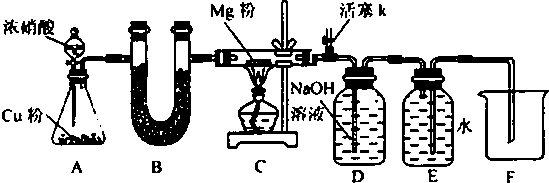
分析 加热条件下浓盐酸和二氧化锰发生氧化还原反应生成氯气,生成的氯气中含有氯化氢和水,B为硫酸铜,可用于检验水,C为氯化钙,可用于吸收水,D中干燥的有色布条不褪色,E中湿润的有色布条可褪色,F用于吸收氯气,G可用于检验氯化氢,溶液变浑浊,生成氯化银沉淀,因此解答该题.
解答 解:(1)浓盐酸与足量MnO2反应制取Cl2,反应消耗氯化氢,同时反应需要加热,浓盐酸易挥发而损害,随反应的不断进行浓盐酸的浓度逐渐变稀,稀盐酸不反应不与MnO2反应,
故答案为:加热时浓盐酸因挥发而损失,随着反应的进行或挥发浓度变稀以后,将不再反应;
(2)①无水硫酸铜与水反应生成蓝色五水硫酸铜晶体,可用来检验水,
故答案为:无水硫酸铜;白色固体变为蓝色;
②D中干燥的布条不褪色,E中湿润的布条褪色说明干燥的氯气无漂白性,潮湿的氯气(或次氯酸)有漂白性,
故答案为:干燥的氯气无漂白性,潮湿的氯气(或次氯酸)有漂白性;
③氯气易溶于四氯化碳,用四氯化碳吸收氯气,防止干扰F中氯气中含有的氯化氢的检验,
故答案为:吸收氯气;
④F装置用来检验HCl气体,反应的离子方程式为:Ag++Cl-=AgCl↓,
故答案为:Ag++Cl-=AgCl↓;
(3)氯气、氯化氢通入到硝酸银都会产生沉淀,为了确保实验结论的可靠性,应在装置E和F之间增加一个盛有湿润的淀粉碘化钾试纸或者湿润的有色布条,如果湿润的淀粉碘化钾试纸不变蓝或者湿润的有色布条不褪色,则氯气被完全吸收,
故答案为:F;G;湿润的淀粉KI试纸(或湿润的有色布条).
点评 本题考查性质实验方案的设计,题目难度中等,涉及了氯气的制备、氯气的性质、氯离子检验,明确实验的目的与原理是解题的关键,注意掌握氯气的化学性质及检验方法,试题侧重考查了学生的分析、理解能力及化学实验能力.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:选择题
| A. | 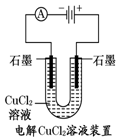 装置中阳极上析出红色固体 | |
| B. | 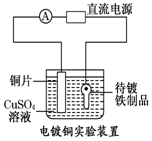 装置的待镀铁制品应与电源正极相连 | |
| C. | 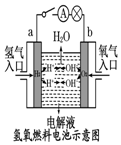 装置中外电路电子由a极流向b极 | |
| D. | 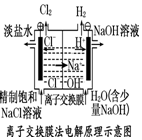 装置的阳极反应为:2H++2e-=H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+Cl-CO32- Cu2+ | B. | Na+Cl-K+ SO42- | ||
| C. | SO42- Mg2+ Ba2+ Cl- | D. | Na+Cl-K+ HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
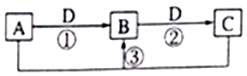 短周期元素W、X、Y、Z、Q的原子序数依次增大,已知A、B、C、D是它们两种或三种元素间形成的化合物,且A、B、C均含有Z元素.A的焰色反应呈黄色,水溶液呈弱碱性;B是两性氢氧化物;D是由W与Q形成的化合物,0.1mol•L-1D溶液的pH为1.在一定条件下它们之间的相互转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z、Q的原子序数依次增大,已知A、B、C、D是它们两种或三种元素间形成的化合物,且A、B、C均含有Z元素.A的焰色反应呈黄色,水溶液呈弱碱性;B是两性氢氧化物;D是由W与Q形成的化合物,0.1mol•L-1D溶液的pH为1.在一定条件下它们之间的相互转化关系如图所示.下列说法正确的是( )| A. | X、Y、Z元素的离子半径大小是X>Y>Z | |
| B. | x元素的氢化物沸点比同主族元素的氢化物低 | |
| C. | Y与Q和W与Q元素形成的化合物化学键类型相同 | |
| D. | q的最高价氧化物对应的水化物和氢化物的酸性在同主族元素中是最强的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3$\stackrel{O_{2}}{→}$NO2 $\stackrel{H_{2}O}{→}$HNO3 | B. | SiO2$\stackrel{HCl}{→}$SiCl4$\stackrel{H_{2}/高温}{→}$Si | ||
| C. | Al2O3$\stackrel{NaOH(aq)}{→}$NaAlO2$\stackrel{CO_{2}}{→}$Al(OH)3 | D. | Na$\stackrel{O_{2}}{→}$ Na2O2$\stackrel{CO_{2}}{→}$Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
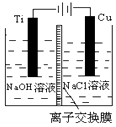 纳米级Cu2O由于具有优良的催化性能而备受关注,下表为制取纳米级Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而备受关注,下表为制取纳米级Cu2O的三种方法: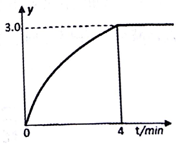
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
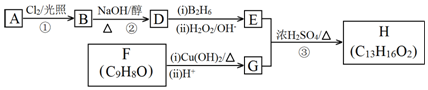
 $→_{(ii)H_{2}O_{2}/OH-}^{(i)B_{2}H_{6}}$
$→_{(ii)H_{2}O_{2}/OH-}^{(i)B_{2}H_{6}}$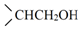
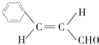 .
.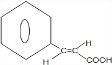 +(CH3)2CHCH2OH$?_{△}^{浓硫酸}$H2O+
+(CH3)2CHCH2OH$?_{△}^{浓硫酸}$H2O+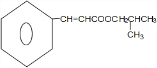 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两者H+浓度可能均为0.01 mol/L | |
| B. | 两者的浓度均为0.01 mol/L | |
| C. | 醋酸中H+浓度一定大于盐酸中H+浓度 | |
| D. | 盐酸浓度一定大于醋酸浓度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com