
| A. | 高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA | |
| B. | 3.2 g O2和O3的混合气体中氧原子数为0.2NA | |
| C. | 标准状况下,5.6 L CO2与足量Na2O2反应转移的电子数为0.5NA | |
| D. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.1NA |
分析 A、铁与水蒸气反应生成四氧化三铁,产物中铁元素的平均化合价为$\frac{8}{3}$,根据电子守恒计算出生成氢气的物质的量;
B、氧气和臭氧均由氧原子构成;
C、求出二氧化碳的物质的量,然后根据过氧化钠与二氧化碳反应时,当1mol二氧化碳参与反应时反应转移1mol电子来分析;
D、用过氧化钠制取氧气,氧元素的价态由-1价变为0价.
解答 解:A.铁在高温下与水蒸气反应生成四氧化三铁,四氧化三铁中铁元素的化合价为$\frac{8}{3}$,0.2mol铁完全反应失去电子数为:0.2mol×($\frac{8}{3}$-0)=$\frac{8}{15}$mol,根据电子守恒,生成氢气的物质的量为:$\frac{\frac{8}{15}mol}{2}$=$\frac{4}{15}$mol,生成的H2分子数为$\frac{4}{15}$NA,故A错误;
B、氧气和臭氧均由氧原子构成,故3.2g混合物中含有的氧原子的物质的量为n=$\frac{3.2g}{16g/mol}$=0.2mol,个数为0.2NA个,故B正确;
C、标况下5.6L二氧化碳的物质的量为0.25mol,而过氧化钠与二氧化碳反应时,当1mol二氧化碳参与反应时反应转移1mol电子,故当0.25mol二氧化碳反应时转移0.25mol电子即0.25NA个,故C错误;
D、用过氧化钠制取氧气,氧元素的价态由-1价变为0价,故当生成0.1mol氧气时转移0.2mol电子即0.2NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
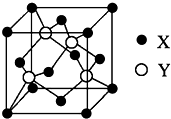 ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
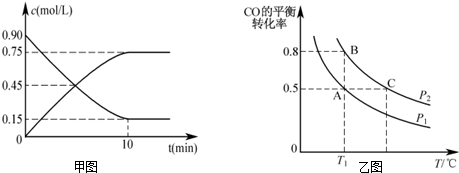
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
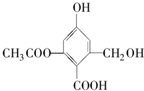
| A. | X的化学式为C10H10O6 | |
| B. | X在一定条件下能与FeCl3溶液发生显色反应 | |
| C. | 1mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3mol、5mol、1mol | |
| D. | X既可以和乙醇又可以和乙酸发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.53g | B. | 5.30g | C. | 10.6g | D. | 11.7g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入一定量C,平衡逆向移动 | |
| B. | 保持温度不变,容器容积压缩到原来的一半,物质B的浓度变为原来的1.8倍,则平衡正向移动 | |
| C. | 恒温恒压,再充入1mol氦气(不参与反应),A的转化率增大,则m<n | |
| D. | 恒温恒压,再加入2mol的A,气体的平均相对分子质量变为原来的2倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鉴别碳酸钠和碳酸氢钠溶液,用澄清石灰水 | |
| B. | 除去碳酸氢钠溶液中的碳酸钠,用稀盐酸 | |
| C. | 除去MgCl2溶液中的FeCl3,加NaOH调pH | |
| D. | 检验FeCl2溶液中混有的FeCl3,可用NH4SCN溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
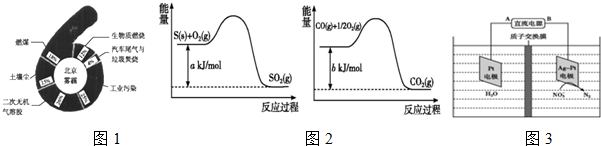
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 1 | 2 | 3 | 4 | 5 | 6 |
| CH4O | C2H4O2 | C4H8O2 | C5H12O | C6H12O2 |
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com