
����Ŀ���ܵ�����������Ũ��ˮ��������ܵ��Ƿ�©����ij��ѧ��ȤС��������ͼװ��̽�������백��֮��ķ�Ӧԭ��������A��F�ֱ�Ϊ�����������ķ���װ�ã�CΪ�����백���ķ�Ӧװ�á�
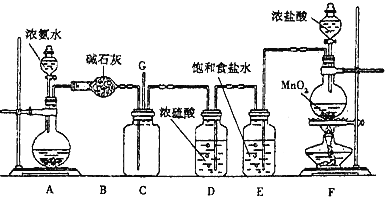
��ش��������⣺
(1)װ��A�е���ƿ�ڹ������ѡ��______(ѡ�����)��
A���������� B����ʯ�� C������������
(2)װ��F�з�����Ӧ�����ӷ���ʽΪ__________________________________��װ��E��������______________________________��
(3)ͨ��װ��C������������߽ϳ����ұ߽϶̣�Ŀ����________________________��
(4)װ��C�ڳ���Ũ��İ��̲��������ڱ����ᣬ��һ�������ǿ�������Ҫ�ɷ�֮һ����д����Ӧ�Ļ�ѧ����ʽ��_____________________________________________���÷�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ_________����װ��C��G���ݳ���β���п��ܺ��л���ɫ���ж����壬��δ���?__________��
���𰸡� B 4H��+2Cl-+MnO2![]() Mn2��+Cl2��+2H2O ��ȥ�����е��Ȼ��� ʹ�ܶȽϴ��Cl2���ܶȽ�С��NH3�Ͽ�ػ�Ͼ��� 8NH3+3Cl2�T6NH4Cl+N2 3��2 ��β��ͨ��NaOH��Һ�л�ͨ��װ�м�ʯ�ҵĸ���ܣ����������ҵ��ռ���
Mn2��+Cl2��+2H2O ��ȥ�����е��Ȼ��� ʹ�ܶȽϴ��Cl2���ܶȽ�С��NH3�Ͽ�ػ�Ͼ��� 8NH3+3Cl2�T6NH4Cl+N2 3��2 ��β��ͨ��NaOH��Һ�л�ͨ��װ�м�ʯ�ҵĸ���ܣ����������ҵ��ռ���
��������(1)װ��A�е���ƿ�����Ʊ�������װ����װ��A�е���ƿ�ڹ����Ǽ�ʯ������ˮ����������ܽ����ʹ�����ų���
(2)��ʯ��������ˮ���������ﰱ��������ʳ��ˮ�dz�ȥ�����е��Ȼ�������,Ũ���������������е�ˮ������
(3)����������ܶȴ�С��ϵ��ܵij�������������֮���ϵij�̶ֳ���
(4)�������̿��Ժ�Ũ�����ڼ�����������������,�������ӷ���ʽ����д��������д��
(5)������������Ӧ�����Ȼ�狀͵�����
(6)����������������ȷ��β�������ķ�����
��1��װ��A�е���ƿ�����Ʊ�������װ�ã�����������Ũ��ˮ����Ӧ��A��������ʯ���к����������ƺ������ƣ���ˮ�����ʯ���ܽ���ȣ������ų���B��ȷ����������������ˮ���������������һˮ�ϰ���Ӧ���������ɰ�����C������ȷѡ��B��
(2) װ��F�ж���������Ũ������ȷ�Ӧ�����Ȼ�����������ˮ����Ӧ�����ӷ���ʽΪ4H��+2Cl-+MnO2![]() Mn2��+Cl2��+2H2O �������к����Ȼ������������������ñ���ʳ��ˮ��ȥ�Ȼ�����װ��E�������dz�ȥ�����е��Ȼ�������ȷ����4H��+2Cl-+MnO2
Mn2��+Cl2��+2H2O �������к����Ȼ������������������ñ���ʳ��ˮ��ȥ�Ȼ�����װ��E�������dz�ȥ�����е��Ȼ�������ȷ����4H��+2Cl-+MnO2![]() Mn2��+Cl2��+2H2O�� ��ȥ�����е��Ȼ�����
Mn2��+Cl2��+2H2O�� ��ȥ�����е��Ȼ�����
��3���������ܶ�С���������ܶȸ���Cװ�õ���������߳����ұ߶̣������������������ֽӴ�����Ӧ����ȷ����ʹ�ܶȽϴ��Cl2���ܶȽ�С��NH3�Ͽ�ػ�Ͼ�����
(4)������������Ӧ�����Ȼ��������������ͬʱ���ɵ�������Ӧ�Ļ�ѧ����ʽ��8NH3+3Cl2�T6NH4Cl+N2����Ԫ�ػ��ϼ���-3�����ߵ�0�ۣ�����ԭ������Ԫ����0�۽��͵�-1�����������������8molNH3��2molNH3����������˸÷�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ3��2�������ж������ԺͼӦ����˿�����NaOH��Һ��װ�м�ʯ�ҵĸ���ܽ������գ���ȷ�𰸣�8NH3+3Cl2�T6NH4Cl+N2��3��2 ����β��ͨ��NaOH��Һ�л�ͨ��װ�м�ʯ�ҵĸ���ܣ����������ҵ��ռ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������մ���Һ���������Ժͽ�ǿ�Ļ�ԭ�ԣ�����֯��Ư������ȼ������������еĻ�ԭ������������ƣ�Na2S2O3�������������ƺ����ͨ�����Ϸ�Ӧ�Ƶã�װ����ͼI��ʾ��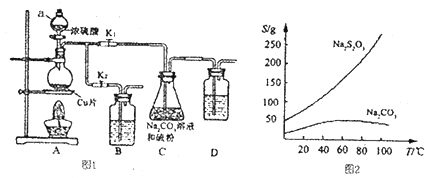
��֪��Na2S2O3��������Һ�в����ȶ����ڣ��й����ʵ��ܽ��������ͼ2��ʾ��
��1��Na2S2O35H2O���Ʊ���
����1����ͼ���Ӻ�װ�ú�δװҩƷ�������A��Cװ�������ԵIJ�����_ ��
����2������ҩƷ����K1���ر�K2�����ȣ�װ��B��D�е�ҩƷ��ѡ�����������е������ţ���
A��NaOH��Һ B��ŨH2S04C������KMnO4��Һ D������NaHCO3��Һ
����3��C�л��Һ��������������Ӧһ��ʱ�����۵������٣�
����4������C�еĻ��Һ������Һ��������Ũ�������ȹ��ˣ��ٽ���Һ���ˡ�ϴ�ӡ���ɣ��õ���Ʒ��
��2��Na2S2O3���ʵļ��飺��������������ˮ�еμ�����Na2S2O3��Һ����ˮ��ɫ��dz����鷴Ӧ����Һ�к����������д���÷�Ӧ�Ļ�ѧ����ʽ ��
��3������Na2S2O3��Һ�ⶨ��ˮ��Ba2+Ũ�ȣ��������£�ȡ��ˮ25.00mL�������ʵ�����ȼ�������K2Cr2O7��Һ����BaCrO4���������ˡ�ϴ�Ӻ�������ϡ�����ܽ⣮��ʱCr42��ȫ��ת��ΪCr2O72�����ټӹ���KI��Һ����ַ�Ӧ���������Һ��ָʾ������0.010molL��1��Na2S2O3��Һ���еζ�����Ӧ��ȫʱ������Na2S2O3��Һ18.00mL�����ַ�Ӧ�����ӷ���ʽΪ��Cr2O72��+6I��+14H+�T2Cr3++3I2+7H2O��I2+2S2O32���TS4O62��+2I�� �� ��÷�ˮ��Ba2+�����ʵ���Ũ��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�������е�һ����Ҫ��Ӧ��SO2��400��500���µĴ�������2SO2+O2![]() 2SO3������һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���д������
2SO3������һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���д������
A. �����������£�SO2������100%��ת��ΪSO3
B. ʹ�ô�����Ϊ�˼ӿ췴Ӧ���ʣ��������Ч��
C. Ϊ�����SO2��ת���ʣ�Ӧ�ʵ����O2��Ũ��
D. �ﵽƽ��ʱ��SO2��Ũ����SO3��Ũ��һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȥ���������ڵ����ʣ������Լ��Ͳ�������ȷ���ǣ� ��
ѡ�� | ����ӵ����� | �Լ� | ���� |
A | NaCl��Na2CO3�� | ϡ���� | �����ᾧ |
B | CO2��HCl�� | ����Na2CO3��Һ | ϴ�� |
C | Cl2��H2O�� | ��ʯ�� | ϴ�� |
D | CO2��CO�� | ���� | ��ȼ |
A.A
B.B
C.C
D.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʷ����У�ǰ�߰������ߵ���
A.�����������B.����������
C.��Һ������D.��Һ����ɢϵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NԪ���γɵĻ�����ḻ��ʣ��Իش��������⣺
(1)������ͭ��Һ����μ��백ˮ�Ȳ���������������ܽ�Ϊ����ɫ��Һ,�����Ҵ���������ɫ���塣
�ٻ�̬ͭԭ�ӵĺ�������Ų�ʽΪ________________��
��1mol����ɫ������������к��еĦҼ�����ĿΪ___________��
�ۼ�Ҫ����Ϊʲô�����Ҵ����о�������_____________________________��
(2)��֪���ǻ������ĽṹʽΪ![]() ���Ƚϣ����ǻ������ķе�_____________���ǻ������ķе�(����ڡ��� �����ڡ��� ����ȷ����);���̷��¼��е������������谷���ṹ��ʽΪ
���Ƚϣ����ǻ������ķе�_____________���ǻ������ķе�(����ڡ��� �����ڡ��� ����ȷ����);���̷��¼��е������������谷���ṹ��ʽΪ![]() ���÷����е�ԭ�ӵ��ӻ���ʽΪ________________;����Ͷ������������Nһ����������,�ṹ��ʽΪ
���÷����е�ԭ�ӵ��ӻ���ʽΪ________________;����Ͷ������������Nһ����������,�ṹ��ʽΪ![]() ,��÷������漰�ĵڶ�����Ԫ�ص�һ��������С�����˳��Ϊ____________________��
,��÷������漰�ĵڶ�����Ԫ�ص�һ��������С�����˳��Ϊ____________________��
(3)��֪CuN3�е���������CO2��Ϊ�ȵ����壬CuN3����ľ������Ȼ��Ƶľ������ơ�
����д��CuN3�е������ӵĵ���ʽ__________________��
����֪�þ��徧���߳�a,b,c,��ϵΪa=b___________����
(4)��֪NH3,NF3,N(CH3)3��������ͭ�������������ӡ�
���ȶ���[Cu(NH3)4]2+__________[Cu(NF3)4]2+��(����ڡ�, �����ڡ�,����ȷ���� )
����֪�ȶ���[Cu(NH3)4]2+����[Cu[N(CH3)3]4]2+,���Ҫ����ԭ��_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ʷֱ�ע��ˮ�У����ã��ֲܷ㸡��ˮ�����(����)
�ٱ������������������Ҵ��������ᡡ����֬�������Ȼ�̼
A. �٢ڢ� B. �٢ۢ� C. �٢ڢ� D. �٢ڢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л����У�ʵ��ʽ��ͬ���ҼȲ���ͬϵ��ֲ���ͬ���칹�����( )
A. 1-��ϩ��3-��-1-��ϩ B. ������Ȳ
C. 1-�ȱ����2-�ȱ��� D. �ױ����ұ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��C��N��O��Al��Si��Cu�dz���������Ԫ�أ�
��1��Siλ��Ԫ�����ڱ������ڵ��壮
��2��Nԭ�ӵ�ԭ�ӽṹʾ��ͼΪ��Cu�ĵͼ����������ɫΪ ��
��3���á�����������գ�
ԭ�Ӱ뾶 | �縺�� | �۵� | �е� |
AlSi | NO | ���ʯ����� | CH4SiH4 |
��4�������£�����ȥ��������Ĥ��Al��CuƬ����ŨHNO3�����ԭ��أ�ͼ1�������ԭ��صĵ���ǿ�ȣ�I����ʱ�䣨t���ı仯��ͼ2��ʾ����Ӧ�������к���ɫ���������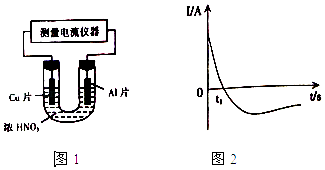
0��t1ʱ��ԭ��صĸ�����AlƬ����ʱ�������ĵ缫��Ӧʽ�� �� ��Һ�е�H+�����ƶ���t1ʱ��ԭ����е��������������ı䣬��ԭ���� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com