
下列离子方程式书写正确的是( )
A.用FeCl3溶液腐蚀铜线路板:Cu + Fe3+ = Cu2+ + Fe2+
B.Na2O2与H2O反应产生O2 :2Na2O2 + 2H2O = 4Na+ + 4OH- + O2↑
C.将铁溶于稀盐酸: 2Fe + 6H+ = 2Fe3+ + 3H2↑
D.向氯化铝溶液中加入过量的氨水:Al3+ + 4NH3·H2O = AlO2- + 4NH4+ + 2H2O
 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源:2016-2017学年河北省高一上9月月考化学试卷(解析版) 题型:选择题
将4g NaOH溶解在10mL水中,再稀释成IL溶液,从中取出10mL,这10mL溶液的物质的量浓度为( )
A.1mol·L-1 B.0.1mol·L-1 C.0.01mol·L-1 D.10mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高二上第一次月考化学试卷(解析版) 题型:选择题
反应2SO2+O2  2SO3,经过一段时间后,SO3的浓度增加了0.4 mol/L,在这段时间内用O2表示的反应速率为0.04 mol/(L·s),则这段时间为 ( )
2SO3,经过一段时间后,SO3的浓度增加了0.4 mol/L,在这段时间内用O2表示的反应速率为0.04 mol/(L·s),则这段时间为 ( )
A.5s B.2.5s C.0.1s D.10s
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上学期开学模拟化学试卷(解析版) 题型:选择题
将4gNaOH和0.1mol Na2CO3混合并配成溶液,向溶液中滴加1. 0mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是 ( )
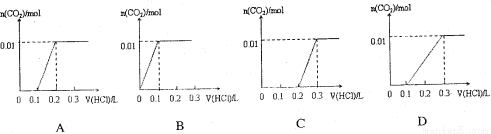
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上学期开学模拟化学试卷(解析版) 题型:选择题
下列物质中,既含有共价键又含有离子键的是 ( )
A.HCl B.Na2S C.MgCl2 D.NaOH
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高二上学期期初考试化学试卷(解析版) 题型:推断题
某烃A是有机 化学工业的基本原料,其 产量可以用来衡量一个国家的石油化工发展水平, A还是一种植物生长调节 剂,A可发生如图所示的 一系列化学反应,其中①②③属于同种反应类型。根据图回答下列问题:
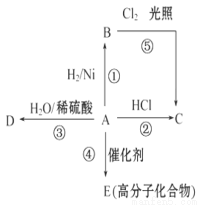
(1)写出A、B、C、D的结构简式:
A_______________,B______________________,
C_______________,D______ ___。
(2)写出②、⑤两步反应的化学方程式,并注明反应类型:
②_________________________,反应类型_______。
⑤_________________________,反应类型_______。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高二上学期期初考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.石油是混合物,汽油是纯净物
B.沸点:汽油>煤油>柴油>润滑油
C.分馏汽油和裂化汽油成分完全相同
D.石油的分馏是物理过程,而裂化和裂解属于化学过程
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上学期定时训练6化学试卷(解析版) 题型:实验题
烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,并用于烟气脱硫研究。
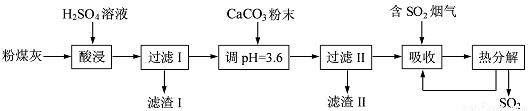
(1)酸浸时反应的化学方程式为___________;滤渣I的主要成分为____________(填化学式)。
(2)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Al2(SO4)x(OH)6-2x。滤渣II的主要成分为___________(填化学式);若溶液的pH偏高,将会导致溶液中铝元素的含量降低,其原因是___________________(用离子方程式表示)。
(3)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是____________;与吸收SO2前的溶液相比,热分解后循环利用的溶液的pH将__________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省十堰市高一上9月月考化学试卷(解析版) 题型:选择题
某温度下,反应2A(g) 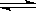 B(g)+C(g)的平衡常数为1,在容积为2L的密闭容器中加入A(g)。20s时测得各组分的物质的量如下表:下列说法正确的是( )
B(g)+C(g)的平衡常数为1,在容积为2L的密闭容器中加入A(g)。20s时测得各组分的物质的量如下表:下列说法正确的是( )
物质 | A(g) | B(g) | C(g) |
物质的量/mol | 1.2 | 0.6 | 0.6 |
A.反应前20s的平均速率为v(A)=0.6mol·L-1·S-1
B.20s时,正反应速率等于逆反应速率
C.达平衡时,A(g)的转化率为100%
D.若升高温度,平衡常数将变为0.5,则反应的△H<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com