
���� ��1����۸����������ʣ�ʳ�ξ�����ζ������Ϊ��ζ����ţ�⸻�������ʣ�����������֬��
��2�����������ڵ��ǣ�����ˮ�⣬����û��������ά�ص�ø����ά���������в���ֱ�ӱ��������գ�������ˮ�����ɰ����ᣬ��֬ˮ�����ɸ�֬������ͣ�
��3����˾ƥ���ǽ�����ʹҩ����ù���ǿ����أ�ʹ��ǰҪ����Ƥ�������Բ��Ե�ҩ�θ��ƽ�ǿ���ҩ����Ƽ���д̼����������ã��ǹ��ʰ�ί���Ͻ��˶�Ա���õ�ҩ�
��� �⣺��1����۸������ۣ������������ʣ�ʳ�ξ�����ζ������Ϊ��ζ����ţ�⸻�������ʣ�����������֬��
�ʴ�Ϊ���ܣ��ۣ��ڣ�
��2�����������ڵ��ǣ����ܷ���ˮ�ⷴӦ������û��������ά�ص�ø����ά���������в���ֱ�ӱ��������գ�������ˮ�����ɰ����ᣬ��֬ˮ�����ɸ�֬������ͣ�
�ʴ�Ϊ���ۣ��ܣ��������֬������ͣ�
��3��a��ijͬѧθ����࣬Ӧѡ�õ�ҩ���ǿ���ҩθ��ƽ��
�ʴ�Ϊ���ۣ�
b����Ƽ���д̼����������ã��ǹ��ʰ�ί���Ͻ��˶�Ա���õ�ҩ�
�ʴ�Ϊ���ܣ�
c����ù���ǿ����أ�ʹ��ǰҪ����Ƥ�������Բ��ԣ��Է�������Ӧ��
�ʴ�Ϊ���ڣ�
���� ���⿼��Ӫ�����ʺ����彡���Ĺ�ϵ���漰����Ӫ�����ʡ�ʳƷ���Ӽ�������ҩ���֪ʶ���ѶȲ���ע�����֪ʶ�Ļ��ۣ�


 ����ͬ�����Ծ�ϵ�д�
����ͬ�����Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
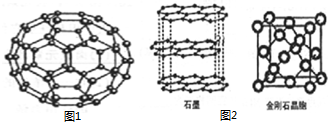 C60���ṹģ����ͼ1��ʾ���ķ����ǻ�ѧ��Ĵ���֮һ��C60������ػ�������K3C60���г����ԣ�
C60���ṹģ����ͼ1��ʾ���ķ����ǻ�ѧ��Ĵ���֮һ��C60������ػ�������K3C60���г����ԣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
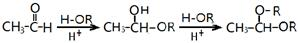

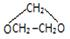 ��
��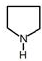 ��F
��F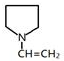 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 11.2mL | B�� | 44.8mL | C�� | 22.4mL | D�� | 44.8L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
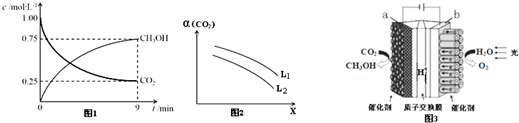
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͨ�����ʯ��ˮ | B�� | ��Ʒ����Һ | ||
| C�� | ��ʪ�����ɫʯ����ֽ | D�� | ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ƻ��˽����� | B�� | �ƻ��˹��ۼ� | C�� | �ƻ������Ӽ� | D�� | �γ��˹��ۼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
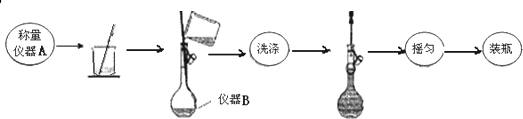

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com