
(7分)试回答下列(1)、 (2)两小题
(1)白磷的着火点为40℃,在室温或夏天正常取出时,就可观察到其被氧化而冒”白烟”,请简单说明将如何将大块的白磷切变成小块的白磷。
(2)某学生在实验报告中写出以下的实验操作或实验数据,你认为合理的是 (填代号A、B……)
A.用托盘天平称取29.25g的食盐;
B.将浓硫酸沿容器器壁缓缓地倒入酒精中,并不断搅拌;
C.用酸式滴定管量取已知浓度的KMn04溶液20.00mL;
D.用湿润的pH试纸测得某溶液的pH为10
E.做中和滴定实验时,锥形瓶用待测液润洗
科目:高中化学 来源: 题型:阅读理解
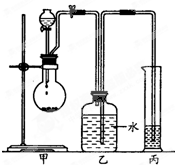 某化学小组探究液体有机物样品A(C3H8O2)的结构,进行如下实验.
某化学小组探究液体有机物样品A(C3H8O2)的结构,进行如下实验.| 实验编号 | 有机样品的体积 | 有机样品的质量 | 生成气体的体积(标准状况下) | I | 3.65mL | 3.8g | 1120mL | II | 7.30mL | 7.6g | 2240mL | III | 14.60mL | 15.2g | 4000mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
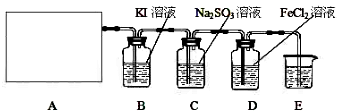
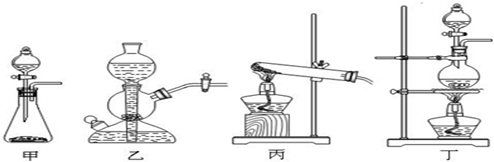
查看答案和解析>>
科目:高中化学 来源: 题型:
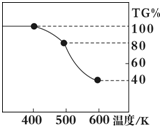 Ⅰ.某溶液中仅含如表离子中的5种离子(不考虑水的电离及离子的水解),且离子的物质的量均为1mol.
Ⅰ.某溶液中仅含如表离子中的5种离子(不考虑水的电离及离子的水解),且离子的物质的量均为1mol.| 阴离子 | SO42-、NO3-、Cl- |
| 阳离子 | Fe3+、Fe2+、NH4+、Cu2+、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 性质 |
A | B | C | D | E | F | G | H | I | J |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |

查看答案和解析>>
科目:高中化学 来源: 题型:
2008年6月,国家质检总局对参与救灾安置重建工作的各类建材进行了抽查,根据抽查结果显示,除建筑防水卷材、新型墙体材料外,合格率均在90%以上。其中铝合金建筑型材抽检合格率为96.7%,比2007年(约90%)有了较大提高。已知国家行业标准中铸造铝合金的各成分的质量分数为:Si:4.5%~5.5%,Cu:1.0%~1.5%,Mg:0.4%~0.6%,其余为Al。
现对某品牌的铸造铝合金中所含的四种成分作如下的实验检测:
①称取18.0 g铸造铝合金样品,分成等质量的A、B两份。向A份加入足量NaOH溶液,B份加入足量的稀盐酸。(已知:Si+2NaOH+ H2O====Na2SiO3 +2H2↑)
②待两份反应物都充分反应之后,称得滤渣质量相差0.512 g,收集得到的两份气体的体积相差851.2 mL(标准状况下)。
试回答下列问题:
(1)样品中Si和Mg的物质的量分别是多少?
(2)通过计算判断该品牌的铸造铝合金是否为合格产品(一项不达标即为不合格产品)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com