
 有A、B、C、D、E五种元素.其相关信息如下:
有A、B、C、D、E五种元素.其相关信息如下:| 元素 | 相关信息 |
| A | A原子的1s轨道上只有一个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道有三个未成对电子 |
| D | D为主族元素,且与E同周期,其最外层上有两个运动状态不同的电子 |
| E | E能形成红色(或砖红色)的E2O和EO两种氧化物 |
分析 A原子的1s轨道上只有一个电子,则A是H元素;
B是电负性最大的元素,则B为F元素;
C的基态原子2p轨道有三个未成对电子,则C是N元素;
E能形成红色(或砖红色)的E2O和EO两种氧化物,则E为Cu元素;
D为主族元素,且与E同周期,其最外层上有两个运动状态不同的电子,则D最外层有两个电子,且为主族元素,为Ca元素;
(1)E是Cu元素,其原子核外有29个电子,根据构造原理书写Cu元素原子基态时的电子排布式;
(2)同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素;
(3)根据价层电子对互斥理论确定原子杂化方式;
(4)含有空轨道和含有孤电子对的原子之间形成配位键,不同非金属元素之间易形成极性键;
若[Cu(NH3)4]2+具有对称的空间构型,且当[Cu(NH3)4]2+中的两个NH3被两个Cl-取代时,能得到两种不同结构的产物,则[Cu(NH3)4]2+平面正方形;
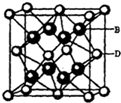
(5)F与Ca可形成离子化合物,根据晶胞结构知,Ca 2+的配位数为8;该晶胞中氟离子个数为8、钙离子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,该晶胞的体积=$\frac{\frac{M}{{N}_{A}}×4}{ρ}$.
解答 解:A原子的1s轨道上只有一个电子,则A是H元素;
B是电负性最大的元素,则B为F元素;
C的基态原子2p轨道有三个未成对电子,则C是N元素;
E能形成红色(或砖红色)的E2O和EO两种氧化物,则E为Cu元素;
D为主族元素,且与E同周期,其最外层上有两个运动状态不同的电子,则D最外层有两个电子,且为主族元素,为Ca元素;
(1)E是Cu元素,其原子核外有29个电子,根据构造原理知,Cu元素原子基态时的电子排布式1s22s22p63s23p63d104s1,故答案为:1s22s22p63s23p63d104s1;
(2)同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素,N和O元素位于同一周期且N元素位于第VA族、O元素位于第VIA族,所以第一电离能N>O,故答案为:大;
(3)NH3分子中N原子价层电子对个数是4且含有一个孤电子对,所以N的杂化轨道类型是sp3,故答案为:sp3;
(4)[Cu(NH3)4]2+中铜离子与氮原子之间形成配位键,氨气分子中N原子与H原子之间形成极性键;[Cu(NH3)4]2+中的两个NH3被两个Cl-取代能得到两种不同结构的产物,[Cu(NH3)4]2+的空间构型为平面正方形,
故答案为:①③;a;
(5)F与Ca可形成离子化合物,根据晶胞结构知,Ca 2+的配位数为8;该晶胞中氟离子个数为8、钙离子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,该晶胞的体积=$\frac{\frac{M}{{N}_{A}}×4}{ρ}$=$\frac{\frac{78}{{N}_{A}}×4}{a}$cm3,
故答案为:8;$\frac{\frac{78}{{N}_{A}}×4}{a}$.
点评 本题考查物质结构和性质,涉及晶胞计算、配合物、原子核外电子排布、电离能等知识点,侧重考查学生知识运用、计算及空间想象能力,难点是晶胞计算及配位数计算,题目难度中等.


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:选择题
| 组号 | 温度(℃) | CaCO3的状态 | 盐酸浓度(mol/L) |
| A | 20 | 块状 | 3 |
| B | 30 | 小颗粒 | 2 |
| C | 30 | 块状 | 4 |
| D | 30 | 小颗粒 | 4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氨是化肥工业和基础化工的重要原料.请回答下列问题:
氨是化肥工业和基础化工的重要原料.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
; ;25℃、101kPa时该气态氢化物热值为5×104kJ•kg-1,则其标准燃烧热为-1300kJ/mol;
;25℃、101kPa时该气态氢化物热值为5×104kJ•kg-1,则其标准燃烧热为-1300kJ/mol;查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N元素的电负性较大,但N2的化学性质很稳定 | |
| B. | 稀有气体一般难发生反应 | |
| C. | HF比H2O稳定 | |
| D. | HF、HCl、HBr、HI的稳定性逐渐减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| R | ||
| X | Y | Z |
| A. | Y的氢化物比Z的氢化物稳定 | |
| B. | 原子半径大小顺序是X>Y>R | |
| C. | Y、R形成的化台物YR3能使酸性KMnO4溶液褪色 | |
| D. | 四种元素中最高价氧化物的水化物的酸性最强的是Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 决定反应速率的因素只有催化剂 | |
| B. | 食物放在冰箱中会减慢食物变质的速率 | |
| C. | 锌与稀硫酸反应时,加入少量水能加快产生氢气的速率 | |
| D. | 增大压强一定能使化学反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素 | H | Li | Be | B | C | O | F |
| X的数值 | 2.20 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 |
| 元素 | Na | Mg | Al | Si | P | S | Cl |
| X的数值 | 0.93 | 1.31 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com