


 +HO-NO2$→_{△}^{浓H_{2}SO_{4}}$
+HO-NO2$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O. .
. (写出其中一种的结构简式).
(写出其中一种的结构简式).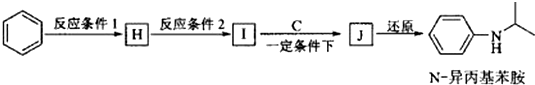
 .
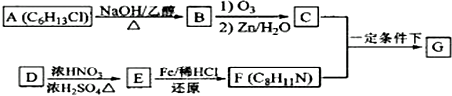
. 分析 A的分子式为C6H13Cl,为己烷的一氯代物,在氢氧化钠醇溶液、加热条件下发生消去反应得到B为烯烃,1mol B发生信息①中氧化反应生成2mol C,且C不能发生银镜反应,B为对称结构烯烃,且不饱和C原子没有H原子,故B为(CH3)2C=C(CH3)2,C为(CH3)2C=O,逆推可知A为(CH3)2CH-CCl(CH3)2.D属于单取代芳烃,其相对分子质量为106,D含有一个苯环,侧链式量=106-77=29,故侧链为-CH2CH3,D为 ,核磁共振氢谱显示F苯环上有两种化学环境的氢,故D发生乙基对位取代反应生成E为
,核磁共振氢谱显示F苯环上有两种化学环境的氢,故D发生乙基对位取代反应生成E为 ,由F的分子式可知,E中硝基被还原为-NH2,则F为
,由F的分子式可知,E中硝基被还原为-NH2,则F为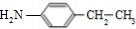 ,C与F发生信息⑤中反应,分子间脱去1分子水形成N=C双键得到G,则G为
,C与F发生信息⑤中反应,分子间脱去1分子水形成N=C双键得到G,则G为 ,据此解答.
,据此解答.
解答 解:A的分子式为C6H13Cl,为己烷的一氯代物,在氢氧化钠醇溶液、加热条件下发生消去反应得到B为烯烃,1mol B发生信息①中氧化反应生成2mol C,且C不能发生银镜反应,B为对称结构烯烃,且不饱和C原子没有H原子,故B为(CH3)2C=C(CH3)2,C为(CH3)2C=O,逆推可知A为(CH3)2CH-CCl(CH3)2.D属于单取代芳烃,其相对分子质量为106,D含有一个苯环,侧链式量=106-77=29,故侧链为-CH2CH3,D为 ,核磁共振氢谱显示F苯环上有两种化学环境的氢,故D发生乙基对位取代反应生成E为
,核磁共振氢谱显示F苯环上有两种化学环境的氢,故D发生乙基对位取代反应生成E为 ,由F的分子式可知,E中硝基被还原为-NH2,则F为
,由F的分子式可知,E中硝基被还原为-NH2,则F为 ,C与F发生信息⑤中反应,分子间脱去1分子水形成N=C双键得到G,则G为
,C与F发生信息⑤中反应,分子间脱去1分子水形成N=C双键得到G,则G为 .
.
(1)由A生成B的化学方程式为:(CH3)2CH-CCl(CH3)2+NaOH$→_{△}^{乙醇}$(CH3)2C=C(CH3)2+NaCl+H2O,属于消去反应,
故答案为:(CH3)2CH-CCl(CH3)2+NaOH$→_{△}^{乙醇}$(CH3)2C=C(CH3)2+NaCl+H2O;消去反应;
(2)由上述分析可知,E为 ,由D生成E的化学方程式为:
,由D生成E的化学方程式为: +HO-NO2$→_{△}^{浓H_{2}SO_{4}}$
+HO-NO2$→_{△}^{浓H_{2}SO_{4}}$ +H2O,
+H2O,
故答案为: +HO-NO2$→_{△}^{浓H_{2}SO_{4}}$
+HO-NO2$→_{△}^{浓H_{2}SO_{4}}$ +H2O;
+H2O;
(3)由上述分析可知,G的结构简式为 ,
,
故答案为: ;
;
(4)F为 ,含有苯环同分异构体中,核磁共振氢谱为4组峰,且面积比为6:2:2:1,说明含有2个-CH3,可以是
,含有苯环同分异构体中,核磁共振氢谱为4组峰,且面积比为6:2:2:1,说明含有2个-CH3,可以是 ,D为
,D为 ,K是芳烃D的同系物,并且碳原子数比D多一个,即为含9个碳的苯的同系物,其结构为苯环上连有三个甲基,根据定二动一的原则有3种,也可以是连一个甲基和一个乙基,有邻间对三种,也可以是丙基或异丙基,有2种结构,所以共有8种,
,K是芳烃D的同系物,并且碳原子数比D多一个,即为含9个碳的苯的同系物,其结构为苯环上连有三个甲基,根据定二动一的原则有3种,也可以是连一个甲基和一个乙基,有邻间对三种,也可以是丙基或异丙基,有2种结构,所以共有8种,
为: ;8;
;8;
(5)由苯与浓硝酸、浓硫酸在加热条件下得到H为硝基苯,硝基苯在Fe粉/盐酸条件下还有得到I为 ,再与(CH3)2C=O反应得到
,再与(CH3)2C=O反应得到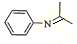 ,最后加成反应还原得到
,最后加成反应还原得到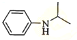 ,
,
故反应条件1所选用的试剂为:浓硝酸、浓硫酸,反应条件2所选用的试剂为:Fe粉/稀盐酸,I的结构简式为  ,
,
故答案为:浓硝酸、浓硫酸;Fe粉/盐酸; .
.
点评 本题考查有机物推断与合成,需要学生对给予的信息进行运用,能较好的考查学生自学能力,要充分利用合成路线中有机物的分子式,关键是确定A与D的结构,再利用正、逆推法相结合进行推断,(4)中同分异构体问题为易错点,难度中等.


 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:选择题
| A. | 溴水中:Na+、K+、SiO32-、CO32- | |
| B. | pH=13的溶液:Ba2+、Na+、I-、ClO- | |
| C. | 苯酚钠溶液中:HSO3-、K+、Na+、AlO2- | |
| D. | 加入淀粉碘化钾溶液显蓝色:Na+、NH4+、SO42-、CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn为电池的负极,被氧化 | B. | O2为负极,被还原 | ||
| C. | 该电池的总反应是2Zn+O2=2ZnO | D. | 该电池是将化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某中学化学兴趣小组同学为探究元素周期律,设计了如下一系列实验.
某中学化学兴趣小组同学为探究元素周期律,设计了如下一系列实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(SO2)=0.1mol/L | B. | c(O2)=0.05mol/L | C. | c(SO3)=0.5mol/L | D. | c(SO2)=0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜时,若转移了NA个电子,则阴极析出32 g铜 | |
| B. | 标准标况下,33.6 L三氧化硫中含有1.5NA个三氧化硫分子 | |
| C. | 1 mol Cl2与过量的铁反应,转移3NA个电子 | |
| D. | 1 mol FeCl3跟水反应,完全转化为氢氧化铁胶体后,其中胶体粒子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
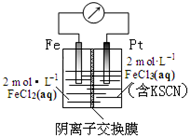
| A. | 电子由铁极经溶液向铂极迁移 | |
| B. | 放电过程中交换膜右侧溶液颜色逐渐变浅 | |
| C. | 正极的电极反应式为Fe3++3e?=Fe | |
| D. | 若转移1mol e-,交换膜左侧溶液中则减少1 molCl- |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com