
| 17.4g |
| 87g/mol |
| ||
| 22.4L��0.2mol |
| 1mol |
| ||
| 4mol��0.2mol |
| 1mol |
| n |
| c |
| 0.8mol |
| 10mol/L |
| ||
| 0.2mol |
| 0.2L |


 ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ij�л���Ľṹ��ʽ��ͼ��ʾ��
ij�л���Ľṹ��ʽ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� ��ֹˮ�йرգ�����ӳ���©��עˮ���������ڼ���װ�õ������� |
B��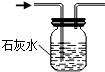 �����ڳ�ȥCO�л��е�����CO2 |
C�� �����ڴӺ�ˮ�еõ���ˮ |
D�� �������ſ����ռ�CO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ | B������ | C����Һ | D����ȡ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ձ� | B�������� |
| C����Һ©�� | D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ɭ����ҿ��ķ����ƻ�����̬ƽ�� |
| B����ҵ�ϴ���ȼ�պ���ȼ�� |
| C���������Ĵ����ŷ� |
| D�������ж�����̼�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com