
(1)下列事实能说明氯元素原子得电子能力比硫元素原子强的是________(填序号)。
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强 ③HCl的稳定性比H2S大 ④HCl的还原性比H2S弱⑤HClO4的酸性比H2SO4强 ⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑦Cl2能与H2S反应生成S ⑧在周期表中Cl处于S同周期的右侧 ⑨还原性:Cl-<S2-
(2)有三种金属元素A、B、C,在相同条件下,B的最高价氧化物的水化物的碱性比A的最高价氧化物的水化物的碱性强;若将A、C相连后投入稀硫酸中,发现C表面有明显气泡产生。则这三种金属元素的原子失电子能力由强到弱的顺序是________。
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
关于键长、键能和键角的说法中不正确的是( )
A.键角是描述分子立体结构的重要参数
B.键长的大小与成键原子的半径和成键数目有关
C.键能越大,键长就越长,共价化合物也就越稳定
D.键角的大小与键长、键能的大小无关
查看答案和解析>>
科目:高中化学 来源: 题型:
一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通入乙烷(C2H6)和氧气,其中某一电极反应式为C2H6+18OH--14e-===2CO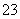 +12H2O。有关此电池的推断不正确的是( )
+12H2O。有关此电池的推断不正确的是( )
A.通入氧气的电极为正极
B.参加反应的O2与C2H6的物质的量之比为7∶2
C.放电一段时间后,KOH的物质的量浓度将下降
D.放电一段时间后,正极区附近溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)甲、乙是元素周期表中同一主族相邻周期的两种元素(其中甲在上一周期),若甲的原子序数为x,则乙的原子序数可能是________________。
(2)若甲、乙分别是同一周期的ⅡA族和ⅦA族元素,原子序数分别为m和n,则m和n的关系为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)原子的最外层有2个电子的元素一定是ⅡA族元素( )
(2)元素所在的主族序数与最外层电子数之比为1的元素都是金属元素( )
(3)原子及离子的核外电子层数等于该元素所在的周期数( )
(4)原子最外层电子数大于3(小于8)的元素一定是非金属元素( )
(5)某元素的离子的最外层与次外层电子数相同,该元素一定位于第3周期( )
(6)最外层电子数等于或大于3(小于8)的一定是主族元素( )
(7)最外层有1个或2个电子,则可能是ⅠA、ⅡA族元素,也可能是副族、Ⅷ族元素或0族元素氦( )
(8)最外层电子数比次外层电子数多的元素一定位于第2周期( )
(9)某元素阴离子最外层电子数与次外层相同,该元素位于第3周期;若为阳离子,则位于第4周期( )
(10)电子层结构相同的离子,若电性相同,则位于同周期,若电性不同,则阳离子位于阴离子的下一周期——“阴上阳下”规律( )
查看答案和解析>>
科目:高中化学 来源: 题型:
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是( )
| X | Y | ||
| W | Z | ||
| T |
A.X、Y、Z三种元素最低价氢化物的沸点依次升高
B.由X、Y和氢三种元素形成的化合物中只有共价键
C.物质WY2、W3X4、WZ4均有熔点高、硬度大的特性
D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素。

请用化学用语回答下列问题:
(1)D元素在周期表中的位置:____________。
(2)A、D、E元素简单离子半径由大到小的顺序为______>______>______。(填微粒符号)
(3)F与D同主族且相邻,二者气态氢化物稳定性的大小关系为______>______。(填微粒符号)
(4)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,试写出该阳离子的电子式______,该阳离子中存在的化学键有______。
(5)C元素的简单氢化物与E元素的最高价氧化物的水化物反应,生成化合物K,则K的水溶液显______(填“酸性”、“碱性”或“中性”),用离子方程式表示其原因____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是某蛋白质的结构片段:
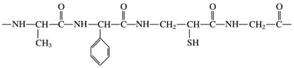
(1)上述蛋白质结构片段的水解产物中不属于α氨基酸的结构简式为________________________________________________________________________。
(2)上述蛋白质结构片段水解后的氨基酸中,某氨基酸碳氢原子数比值最大。
①该氨基酸与NaOH溶液反应的化学方程式为________________________________________________________________________
________________________________________________________________________。
②该氨基酸两分子缩合形成环状结构物质的分子式为
________________________________________________________________________
________________________________________________________________________。
③该氨基酸的同分异构体中,属于硝基化合物且苯环上只有甲基的同分异构体有________种。
(3)已知上述蛋白质结构片段的相对分子质量为364,则水解生成的各种氨基酸的相对分子质量之和为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com