
【题目】在一定温度下,向a L密闭容器中加入1 mol O2和2 mol NO,发生如下反应:O2(g)+2NO(g)![]() 2NO2(g),表明此反应不一定达平衡的是( )
2NO2(g),表明此反应不一定达平衡的是( )
A.容器内O2、NO、NO2的浓度之比为1∶2∶2
B.容器内压强不随时间变化
C.容器内各物质的浓度不随时间变化
D.单位时间内生成1 mol O2,同时生成2 mol NO2
【答案】A
【解析】
可逆反应达到平衡状态时,正反应速率等于逆反应速率,体系中各个物质的物质的量、浓度、百分含量以及由此引起的一系列物理量不发生变化,由此分析。
A. 当容器内O2、NO、NO2的浓度之比为1∶2∶2时,该反应可能达到平衡状态,也可能不是平衡状态,A项正确;
B. 该反应不是等体积反应,当容器内压强不随时间变化时,正反应速率等于逆反应速率,反应达到平衡状态,B项错误;
C. 容器内各物质的浓度不随时间变化时,正反应速率等于逆反应速率,反应达到平衡状态,C项错误;
D. 单位时间内生成1 mol O2,同时生成2 mol NO2,说明正反应速率等于逆反应速率,反应达到平衡状态,D项错误;
答案选A。
化学反应 | mA(g)+nB(g) | 是否平衡 |
正、逆反 应速率之 间的关系 | ①单位时间内消耗了m mol A,同时也生成了m mol A | 平衡 |
②单位时间内消耗了n mol B,同时也消耗了p mol C | 平衡 | |
③v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q | 不一定平衡 | |
④单位时间内生成了n mol B,同时也消耗了q mol D | 不一定平衡 |


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:
【题目】白藜芦醇 广泛存在于食物(例如桑椹、花生,尤其是葡萄)中,它可能具有抗癌性。
广泛存在于食物(例如桑椹、花生,尤其是葡萄)中,它可能具有抗癌性。
(1)能够跟1 mol该化合物起反应的Br2或H2的最大用量分别是________。
A.1 mol,1 mol
B.3.5 mol,7 mol
C.3.5 mol,6 mol
D.6 mol,7 mol
(2)下列不能与白藜芦醇反应的是________。
A.Na2CO3溶液
B.FeCl3溶液
C.NaHCO3溶液
D.酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,用0. 100 mol·L—1盐酸滴定50. 0mL Na2CO3溶液(不考虑CO2从溶液中逸出).滴定曲线如图所示:
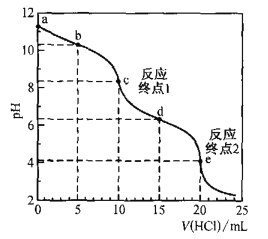
下列说法错误的是
A.a点溶液中:c(Na2CO3)=0.020 mol·L—1
B.b点溶液中:c(Na+)>c(HCO3— )>c(CO32—)
C.c点溶液中:c(Na+)+c(H+)=2c(CO32—) +c(HCO32—)+c(OH—)
D.室温时,H2CO3的一级电离平衡常数Kal的数量级为10—7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.10molL-1盐酸滴定0.10molL-1氨水,滴定过程中NH3H2O、NH4+(假设:溶液中的含氮微粒只有NH3H2O和NH4+)的物质的量分数随pH的变化关系如图所示[例如:δ(NH3H2O)=![]() ]。下列判断正确的是( )
]。下列判断正确的是( )
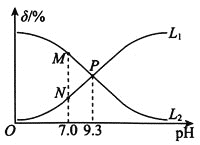
A.曲线L1代表δ(NH4+)与pH的变化关系
B.NH3H2O的电离常数Ka(NH3H2O)=1.0×10-4.7
C.水的电离程度:P>M
D.P点时混合溶液中存在:c(Cl-)=c(NH3H2O)+c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用N2O4通过电解法制备N2O5,反应方程式为N2O4+2HNO3=2N2O5+H2↑,工作原理如图所示,下列叙述正确的是
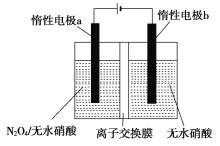
A.惰性电极a上发生还原反应
B.离子交换膜为阴离子交换膜
C.阳极区反应式为N2O4+2HNO3-2e-=2N2O5+2H+
D.反应时质子由右向左移动通过隔膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL未知浓度盐酸(酚酞作指示剂)的滴定曲线。下列说法正确的是( )

A.指示剂变色时,说明盐酸与NaOH恰好完全反应
B.当滴加NaOH溶液10.00 mL时,该混合液的pH=1+lg3
C.水电离出的氢离子浓度:a>b
D.盐酸的物质的量浓度为0.010 0 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是( )
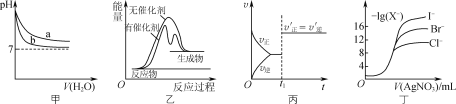
A. 图甲表示pH相同的NaOH溶液与氨水稀释过程pH的变化,曲线a对应氨水
B. 图乙表示某放热反应分别在有、无催化剂的情况下,反应过程中的能量变化
C. 图丙表示CO(g)+Cl2(g)![]() COCl2(g)的反应速率随时间的变化,在t1时改变的条件是加入催化剂
COCl2(g)的反应速率随时间的变化,在t1时改变的条件是加入催化剂
D. 图丁表示用0.0100mol·L-1的硝酸银标准溶液滴定浓度均为0.1000mol·L-1 Cl-、Br-及I-的混合溶液时,先沉淀的是Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三草酸合铁酸钾晶体{K3[Fe(C2O4)3]·3H2O}易溶于水,难溶于乙醇,可用于摄影和蓝色印刷.以铁屑为原料的制备流程如下:
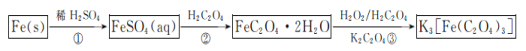
回答下列问题:
(1)流程中“①”加入的稀硫酸需稍过量,其目的是________________;若要从所得溶液中得到绿矾FeSO4·7H2O,必须进行的实验操作是________(按顺序填写)。
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
(2)流程中“②”需过滤分离,则加入H2C2O4发生反应的化学方程式为__________。
(3)流程中“③”需控制溶液温度不高于40 ℃,理由是________________;该步反应的化学方程式为________________________;得到K3[Fe(C2O4)3]溶液后,加入乙醇,然后进行过滤,加入乙醇的理由是________________________________。
(4)所得晶体中C2O42-含量的测定可用酸性KMnO4标准溶液滴定。滴定过程中发现,开始时滴入1滴KMnO4标准溶液,紫红色褪去很慢,滴入一定量后,紫红色很快褪去,原因可能是______。
(5)三草酸合铁酸钾晶体在110 ℃可完全失去结晶水,继续升高温度可发生分解反应。
①分解得到的气体产物用如下装置进行实验:
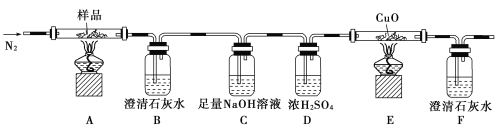
检查装置气密性后,先通一段时间的N2,其目的是____________________;结束实验时,先熄灭酒精灯再通入N2至常温。实验过程中观察到B、F中澄清石灰水都变浑浊,E中有红色固体生成,则分解得到的气体产物是______________。
②分解得到的固体产物含有K2CO3、FeO、Fe,加水溶解、过滤、洗涤、干燥,得到含铁样品。现设计下列两种实验方案对该样品进行铁元素含量测定:
(甲)
(乙)![]() 酸性KMnO4溶液V mL
酸性KMnO4溶液V mL
你认为以上________(填“甲”或“乙”)方案可确定样品的组成,测得铁元素的含量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组在实验室用下图所示装置探究氮氧化物气体与烧碱溶液的反应。实验过程中将胶头滴管中的液体挤入烧瓶,碱液可快速、充分吸收氮氧化物气体。下列叙述正确的是( )
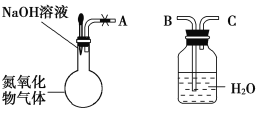
A.若将A与B连接,打开止水夹,则广口瓶中长导管口有气泡产生
B.若将A与C连接,打开止水夹,水沿导管由广口瓶进入烧瓶中
C.无论A连接B还是C,打开止水夹,均无明显现象
D.若将NaOH溶液换为水,可以用这套装置验证氨易溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com