
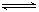 2NO2 ��ƽ
2NO2 ��ƽ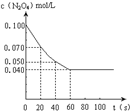
| T/ K | 323 | 373 |
| Kֵ | 0.022 | �� |
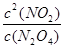 ��Kֵ= 0.36 ����1��0.003mol?L��1?s��1��
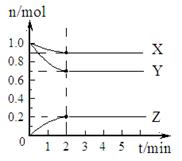
��Kֵ= 0.36 ����1��0.003mol?L��1?s��1��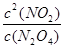 ������ͼ���֪��ƽ��ʱN2O4��Ũ��Ϊ0.040mol/L����ʼʱN2O4��Ũ��Ϊ0.100mol/L��������Ũ�ȱ仯��Ϊ0.060mol/L�����ƽ��ʱNO2��Ũ��Ϊ0.12mol/L������ƽ�ⳣ��Ϊ
������ͼ���֪��ƽ��ʱN2O4��Ũ��Ϊ0.040mol/L����ʼʱN2O4��Ũ��Ϊ0.100mol/L��������Ũ�ȱ仯��Ϊ0.060mol/L�����ƽ��ʱNO2��Ũ��Ϊ0.12mol/L������ƽ�ⳣ��Ϊ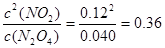 ��
��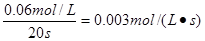 ��
��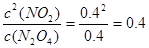 ��0.36����˵����ʱ�淴Ӧ���ʴ�������Ӧ���ʣ���Ӧ���淴Ӧ�����ƶ���
��0.36����˵����ʱ�淴Ӧ���ʴ�������Ӧ���ʣ���Ӧ���淴Ӧ�����ƶ���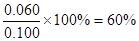 ����Ϊ��Ӧ���������Ŀ��淴Ӧ����������ѹǿ��ƽ�����淴Ӧ�����ƶ���ת���ʼ�С��
����Ϊ��Ӧ���������Ŀ��淴Ӧ����������ѹǿ��ƽ�����淴Ӧ�����ƶ���ת���ʼ�С��

 �����ƻ���ĩ��̶�100��ϵ�д�
�����ƻ���ĩ��̶�100��ϵ�д� �ܿ���ȫ��100��ϵ�д�
�ܿ���ȫ��100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| A������Fe2O3��Ͷ���� |
| B������������������䣬����H2�������� |
| C������N2������������ѹǿ���� |
| D������N2����������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ѧƽ���������ǿ��淴Ӧ |
| B�����淴Ӧ�ﵽ��ѧƽ��״̬ʱ�������淴Ӧ���ʶ�Ϊ0 |
| C�����淴Ӧ�ﵽ��ѧƽ��״̬ʱ��v������=v���棩��0 |
| D�����淴Ӧ�ﵽ��ѧƽ��״̬ʱ������ɳɷ�Ũ�ȱ��ֲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g)��D(g)����һ���¶ȡ�����̶����ܱ������н��У�������������˵��������Ӧ�ﵽƽ��״̬����
2C(g)��D(g)����һ���¶ȡ�����̶����ܱ������н��У�������������˵��������Ӧ�ﵽƽ��״̬�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2HI��g����H����9.48 kJ/mol
2HI��g����H����9.48 kJ/mol  2HI��g����H����26.48 kJ/mol
2HI��g����H����26.48 kJ/mol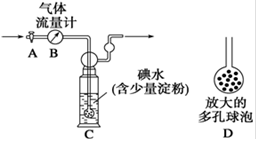
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 C(g)+2D(g)�Ѵﵽƽ��״̬�ı�־��
C(g)+2D(g)�Ѵﵽƽ��״̬�ı�־���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2SO3.5min��ﵽƽ��,�����������SO31.6mol.
2SO3.5min��ﵽƽ��,�����������SO31.6mol.| A��v����(SO2)=v����(SO3) | B����������ƽ����Է����������ٸı� |
| C�����������ܶȲ��ٸı� | D������������������ʵ������ٱ仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
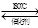 2N2(g)+3H2O(g) ��H��0���ں��ݵ��ܱ������У������й�˵����ȷ���ǣ� ( )
2N2(g)+3H2O(g) ��H��0���ں��ݵ��ܱ������У������й�˵����ȷ���ǣ� ( )| A��ƽ��ʱ�������������䣬����NH3��Ũ�ȣ���Ӧ���ʻή�� |
| B����λʱ��������NO��N2�����ʵ�����Ϊ1��2ʱ����Ӧ�ﵽƽ�� |
| C�������������䣬���뺤������ѧ��Ӧ���ʲ��䡣 |
| D��ƽ��ʱ�������������䣬�����¶ȿ�ʹ�÷�Ӧ��ƽ�ⳣ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com