
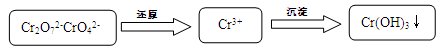
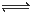 Cr2O72- + H2O
Cr2O72- + H2O
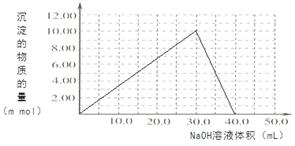 ��
��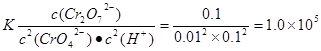 ����2����������Һ��ͨSO2��Cr2O72-��ԭΪCr3+�����ݵ����غ㼰����غ㡢ԭ���غ�ɵ÷�Ӧ�����ӷ���ʽΪ3SO2 + Cr2O72- + 2H+ = 2Cr3+ + 3SO42- + H2O��������Ksp��Cr(OH)3�� =10-32, c(Cr3+)=10-5mol/L,c3(OH-)=10-32��10-5=10-27������c(OH-)=10-9mol/L����c(H+)=Kw��c(OH-)=10-5mol/L,���pH=5����3����ԭ�������õ�������Fe2+��Cr2O72-��ԭΪCr3+�����װ�����õĵ缫������̼������Ƭ��������Ƭ��Ҫʧȥ���ӱ�ΪFe2+������ƬҪ���Դ���������ӡ�Cr(OH)3��ϡ���ᷴӦ��ѧ����ʽΪ2Cr(OH)3 + 3H2SO4 = 2Cr2(SO4)3 + 3H2O��n(Cr3+)=0��1L��0��100mol/L=0��01mol�������Һ�м���NaOH���ȷ�����Ӧ��Cr3����3OH-��Cr(OH)3����n(NaOH)= 0��03mol����NaOH�����Ϊ30mlʱ�����ﵽ���ֵ���ټ���NaOH��Һ��������Ӧ��Cr(OH)3+ OH-= CrO2-+ 2H2O����ʱ������NaOH�����ʵ���Ϊ0��01mol,��������10ml�����ﵽ40mlʱ��������ȫ�ܽ⡣֮���ٵμ�NaOH��Һ��Ҳ���ᷢ����Ӧ�����ɳ��������ʵ��������NaOH��Һ����Ĺ�ϵͼΪ
����2����������Һ��ͨSO2��Cr2O72-��ԭΪCr3+�����ݵ����غ㼰����غ㡢ԭ���غ�ɵ÷�Ӧ�����ӷ���ʽΪ3SO2 + Cr2O72- + 2H+ = 2Cr3+ + 3SO42- + H2O��������Ksp��Cr(OH)3�� =10-32, c(Cr3+)=10-5mol/L,c3(OH-)=10-32��10-5=10-27������c(OH-)=10-9mol/L����c(H+)=Kw��c(OH-)=10-5mol/L,���pH=5����3����ԭ�������õ�������Fe2+��Cr2O72-��ԭΪCr3+�����װ�����õĵ缫������̼������Ƭ��������Ƭ��Ҫʧȥ���ӱ�ΪFe2+������ƬҪ���Դ���������ӡ�Cr(OH)3��ϡ���ᷴӦ��ѧ����ʽΪ2Cr(OH)3 + 3H2SO4 = 2Cr2(SO4)3 + 3H2O��n(Cr3+)=0��1L��0��100mol/L=0��01mol�������Һ�м���NaOH���ȷ�����Ӧ��Cr3����3OH-��Cr(OH)3����n(NaOH)= 0��03mol����NaOH�����Ϊ30mlʱ�����ﵽ���ֵ���ټ���NaOH��Һ��������Ӧ��Cr(OH)3+ OH-= CrO2-+ 2H2O����ʱ������NaOH�����ʵ���Ϊ0��01mol,��������10ml�����ﵽ40mlʱ��������ȫ�ܽ⡣֮���ٵμ�NaOH��Һ��Ҳ���ᷢ����Ӧ�����ɳ��������ʵ��������NaOH��Һ����Ĺ�ϵͼΪ ��
��

 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3OH��g����H1����116 kJ��mol��1
CH3OH��g����H1����116 kJ��mol��1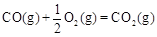 ��H2����283 kJ��mol��1
��H2����283 kJ��mol��1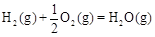 ��H3����242 kJ��mol��1
��H3����242 kJ��mol��1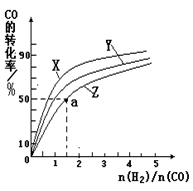
 CH3OH��g����ƽ�ⳣ��K= ��
CH3OH��g����ƽ�ⳣ��K= �� | | 0min | 5min | 10min |
| CO | 0.1 | | 0.05 |
| H2 | 0.2 | | 0.2 |
| CH3OH | 0 | 0.04 | 0.05 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
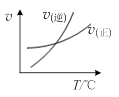
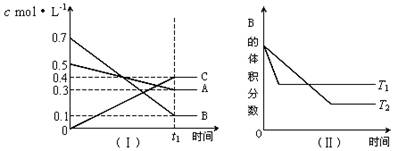
| A����ͼ�ױ�ʾ�ķ�Ӧ�������¶ȱ仯�Ĺ�ϵ��֪�÷�Ӧ�Ħ�H��0 |
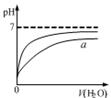
| B��ͼ�ұ�ʾpH��ͬ������������зֱ����ˮ����ҺpH�ı仯����������a��Ӧ���Ǵ��� |
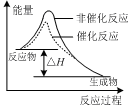
| C��ͼ����ʾ�÷�ӦΪ���ȷ�Ӧ���Ҵ����ܸı䷴Ӧ���ʱ� |
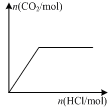
| D��ͼ����ʾ��Na2CO3��Һ����εμ�ϡ���ᣬ����CO2�������������ʵ����Ĺ�ϵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
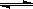 ��2(t��BuNO) �����¶��¸÷�Ӧ��CCl4�ܼ��е�ƽ�ⳣ��Ϊ1.4��
��2(t��BuNO) �����¶��¸÷�Ӧ��CCl4�ܼ��е�ƽ�ⳣ��Ϊ1.4�� 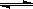 2(t��BuNO) ��������ȷ���ǣ� ��
2(t��BuNO) ��������ȷ���ǣ� ��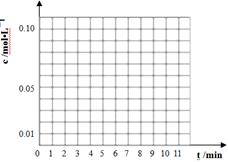
| ʱ�䣨min�� | 0 | 1 | 3 | 5 | 7 | 9 | 11 |
| c(t��BuNO)2 mol/L | 0.05 | 0.03 | 0.01 | 0.005 | 0.003 | 0.002 | 0.002 |
| c(t��BuNO) mol/L | 0 | 0.04 | 0.08 | 0.07 | 0.094 | 0.096 | 0.096 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3��g�� ��H��0��2min��Ӧ�ﵽƽ�⣬����SO3Ϊ1.4mol,ͬʱ�ų�����Q kJ�������з�����ȷ����
2SO3��g�� ��H��0��2min��Ӧ�ﵽƽ�⣬����SO3Ϊ1.4mol,ͬʱ�ų�����Q kJ�������з�����ȷ����| A���ڸ������£���Ӧǰ���ѹǿ֮��Ϊ6��5.3 |
| B������Ӧ��ʼʱ�������Ϊ2L����v(SO3)��0.35mol/(L��min) |
| C�����ѡ����º�ѹ�¡���Ϊ����ѹ���������¡���Ӧ��ƽ���n(SO3)��1.4mol |
| D�����ѡ����º�ѹ�¡���Ϊ�����º����¡���Ӧ����ƽ��ʱ�ų���������Q kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3(g)+ CO2(g)������˵���÷ֽⷴӦ�ﵽƽ��״̬���� �� ��
2NH3(g)+ CO2(g)������˵���÷ֽⷴӦ�ﵽƽ��״̬���� �� ��

| A����λʱ��������1 mol CO2��ͬʱ����2 mol NH3 |
| B���γ�6��N��H����ͬʱ��2��C=O������ |
| C��������CO2��NH3�����ʵ���֮�ȱ��ֲ��� |
| D�����������ܶȲ��ٸı��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���

 CH3OH��g��+H2O��g����H<0������6mo1 CO2��8mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯����������ͼ��ʾ��ʵ�ߣ���
CH3OH��g��+H2O��g����H<0������6mo1 CO2��8mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯����������ͼ��ʾ��ʵ�ߣ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 cP(g)��dQ(g)�ﵽƽ��ʱ��M���������y(M)�뷴Ӧ�����Ĺ�ϵ��ͼ��ʾ������z��ʾ��Ӧ��ʼʱN�����ʵ�����M�����ʵ���֮�ȣ�����˵����ȷ����(����)
cP(g)��dQ(g)�ﵽƽ��ʱ��M���������y(M)�뷴Ӧ�����Ĺ�ϵ��ͼ��ʾ������z��ʾ��Ӧ��ʼʱN�����ʵ�����M�����ʵ���֮�ȣ�����˵����ȷ����(����)
| A��ͬ��ͬѹͬzʱ�����������ƽ��ʱQ������������� |
| B��ͬѹͬzʱ�������¶ȣ�ƽ��ʱQ������������� |
| C��ͬ��ͬzʱ������ѹǿ��ƽ��ʱQ������������� |
| D��ͬ��ͬѹʱ������z��ƽ��ʱQ������������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com